1. 领域背景与文献引入
文献英文标题:Reliable detection of CNS lymphoma-derived circulating tumor DNA in cerebrospinal fluid using multi-biomarker NGS profiling: insights from a real-world study;发表期刊:Biomarker Research;影响因子:未公开;研究领域:中枢神经系统淋巴瘤液体活检与生物标志物研究
中枢神经系统淋巴瘤(CNSL)分为原发性(PCNSL)和继发性(SCNSL),是一类罕见但侵袭性极强的淋巴瘤亚型,约占所有脑肿瘤的6-7%,患者预后极差——PCNSL患者中位生存期仅3-4年,SCNSL复发患者中位生存期仅2-3个月。领域发展关键节点方面,传统诊断依赖有创脑组织活检、磁共振成像(MRI)及脑脊液细胞分析,但活检存在手术创伤、解剖位置限制导致的取材失败风险;MRI对微小浸润病灶辨识度不足,易出现假阴性;脑脊液流式细胞术受肿瘤细胞稀疏分布影响,灵敏度仅约21%。2010年后,液体活检尤其是循环肿瘤DNA(ctDNA)技术的兴起为CNSL诊断提供了非侵入性途径,但早期研究多局限于单靶点检测(如MYD88 L265P突变)、样本量较小、缺乏真实世界临床数据,存在检测灵敏度不足、样本类型选择(血浆vs脑脊液)争议、技术成本高昂难以常规化等未解决核心问题。当前研究热点聚焦于多靶点下一代测序(NGS)技术在CNSL液体活检中的应用,旨在平衡检测灵敏度、特异性与临床可行性。结合领域现状,本研究针对现有研究的局限性,通过真实世界大样本队列,系统评估多靶点NGS panel在脑脊液和血浆ctDNA检测中的性能,对比传统诊断方法,探索临床可行的CNSL非侵入性诊断策略,为CNSL的精准诊断提供循证依据。
2. 文献综述解析
作者按诊断技术的发展维度(传统有创/影像学方法→单靶点液体活检→多靶点NGS技术)对领域内现有研究进行分类评述,明确不同技术路线的优势与局限性,进而凸显本研究的创新价值。
传统诊断方法中,脑组织活检是CNSL诊断的金标准,但存在手术创伤、解剖位置限制导致的取材失败风险;MRI作为影像学常规手段,对微小浸润病灶的分辨率不足,易出现假阴性;脑脊液流式细胞术依赖肿瘤细胞的直接捕获,受肿瘤细胞稀疏分布影响,灵敏度仅约20%。单靶点ctDNA检测以MYD88 L265P为核心标志物,具有较高特异性,但因CNSL的遗传异质性,灵敏度仅约46%,无法覆盖所有患者;部分研究采用超灵敏NGS技术提升检测灵敏度,但该方法成本高昂、操作复杂,难以在常规临床实践中推广。现有研究的共同局限性包括样本量较小、多为回顾性研究、缺乏真实世界场景下的系统对比数据,且未明确最优样本类型和检测策略。
本研究通过真实世界前瞻性队列(56例患者,164份样本),采用常规可负担的多靶点NGS panel(LYNX),同时分析基因变异、染色体畸变及抗原受体重排三类标志物,首次在真实临床场景中系统对比脑脊液与血浆ctDNA检测性能,证明脑脊液ctDNA检测灵敏度(91%)远高于流式细胞术(21%,P<0.001),多靶点检测灵敏度(90%)显著优于单靶点MYD88检测(46%,P=0.001),解决了现有研究中样本类型争议和技术可行性问题,为CNSL的非侵入性诊断提供了临床可落地的方案。
3. 研究思路总结与详细解析
本研究以“评估常规多靶点NGS在CNSL液体活检中的临床性能,明确最优诊断策略”为核心目标,针对“如何在常规临床实践中实现CNSL高灵敏度非侵入性诊断”这一科学问题,采用“真实世界队列样本收集→多维度核酸检测→传统方法对比→临床关联分析”的闭环技术路线,系统验证脑脊液ctDNA多靶点检测的诊断价值。
3.1 真实世界队列构建与样本采集
实验目的是建立具有代表性的CNSL患者队列,获取匹配的液体活检和组织样本以支持多维度分析。方法细节:纳入2021-2023年捷克布尔诺大学医院的56例CNSL患者(25例PCNSL,31例SCNSL),其中16例为复发患者,收集61份脑脊液、61份血浆及42份福尔马林固定石蜡包埋(FFPE)组织样本;脑脊液采集中位数体积10ml,血浆4ml,28例患者接受过糖皮质激素治疗(地塞米松8mg每日3次,中位疗程5天);样本采集遵循临床常规流程,FFPE组织样本回顾性从生物库获取。结果解读:队列中位年龄67岁,中位随访14个月,覆盖初诊、复发及不同治疗阶段患者,样本类型全面,为真实世界研究提供了可靠的临床数据基础;糖皮质激素治疗未显著影响脑脊液cfDNA和ctDNA水平(P<0.14和P<0.98),排除了治疗干扰对检测结果的影响。产品关联:文献未提及具体样本采集产品,领域常规使用STRECK cfDNA保存管用于液体活检样本收集。
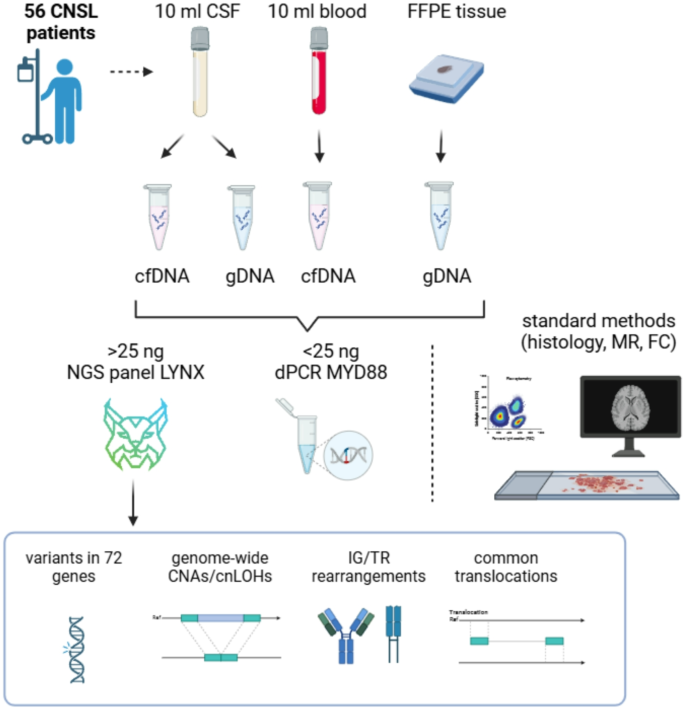
3.2 样本处理与核酸提取
实验目的是获取高质量的游离DNA(cfDNA)和基因组DNA(gDNA),为后续检测提供合格的核酸模板。方法细节:血浆样本经两次离心(300g 20min、5000g 10min)分离,脑脊液样本离心分离上清(用于cfDNA提取)和沉淀(用于gDNA提取);cfDNA采用QIAamp Circulating Nucleic Acids试剂盒提取,gDNA分别采用QIAamp DNA Blood Mini Kit(脑脊液沉淀)和QIAamp DNA FFPE tissue kit(FFPE组织)提取;通过Agilent cfDNA ScreenTape检测cfDNA质量,Qubit荧光定量仪检测核酸浓度。结果解读:脑脊液cfDNA中位数浓度低于血浆,但ctDNA检测性能更优;脑脊液cfDNA与ctDNA水平呈正相关(P<0.003),血浆中两者也呈正相关(P<0.001),提示cfDNA浓度可作为ctDNA检测的初步评估指标。产品关联:实验所用关键产品:Qiagen的QIAamp Circulating Nucleic Acids试剂盒、QIAamp DNA Blood Mini Kit、QIAamp DNA FFPE tissue kit;Agilent的cfDNA ScreenTape assay;Thermo Fisher Scientific的Qubit fluorimeter。
3.3 多靶点NGS与数字PCR检测
实验目的是对比多靶点与单靶点检测的灵敏度,明确不同样本类型的ctDNA检测性能。方法细节:使用定制LYNX NGS panel(覆盖1.13Mb目标区域,可检测基因变异、染色体畸变、抗原受体重排,检测限5%)对cfDNA样本进行分析,当cfDNA量不足25ng时采用数字PCR(dPCR)检测MYD88 L265P突变;ctDNA水平以单倍体基因组当量/毫升(hGE/ml)表示,阳性定义为至少一个标志物高于检测限。结果解读:多靶点NGS检测CNS浸润的阳性率达90%,远高于单靶点MYD88检测的46%(P=0.001);脑脊液ctDNA检测阳性率为91%,显著高于血浆(仅SCNSL患者中部分阳性),且远高于流式细胞术的21%(P<0.001);联合分析脑脊液cfDNA和gDNA可进一步提升检测阳性率。产品关联:实验所用关键产品:定制LYNX NGS panel;数字PCR平台(文献未明确品牌,领域常规使用Bio-Rad或Thermo Fisher Scientific的dPCR系统)。
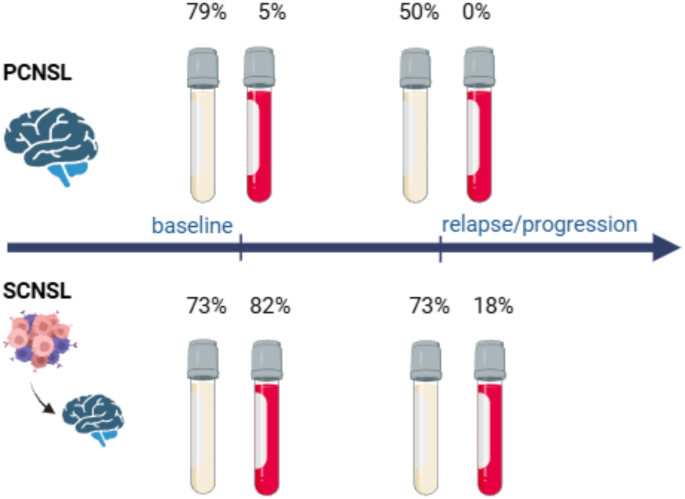
3.4 流式细胞术检测与统计学分析
实验目的是对比脑脊液ctDNA检测与传统细胞检测方法的性能,明确临床应用价值。方法细节:采用8色流式细胞术panel(CD3、CD10、CD19、CD20、CD45等抗体)检测脑脊液中的淋巴瘤细胞,使用BD FACSCanto II流式细胞仪采集数据,FACSDiva软件分析;统计学分析采用Fisher精确检验比较分类变量,Mann-Whitney U检验比较连续变量,Spearman相关分析评估相关性,Kaplan-Meier法进行生存分析。结果解读:流式细胞术仅检测出21%的CNS浸润病例,远低于脑脊液ctDNA的91%(P<0.001);生存分析未发现ctDNA水平与患者预后的显著关联,推测与队列样本量较小、患者异质性较高有关。产品关联:实验所用关键产品:BD的FACSCanto II流式细胞仪、FACSDiva软件;CD3、CD10等流式抗体(文献未明确品牌,领域常规使用BD、BioLegend等品牌的流式抗体)。
4. Biomarker研究及发现成果解析
本研究聚焦CNSL的ctDNA生物标志物,通过多靶点NGS技术筛选并验证了一系列基因变异、染色体畸变及抗原受体重排标志物,明确了脑脊液ctDNA作为CNSL诊断生物标志物的核心价值,为临床非侵入性诊断提供了可靠依据。
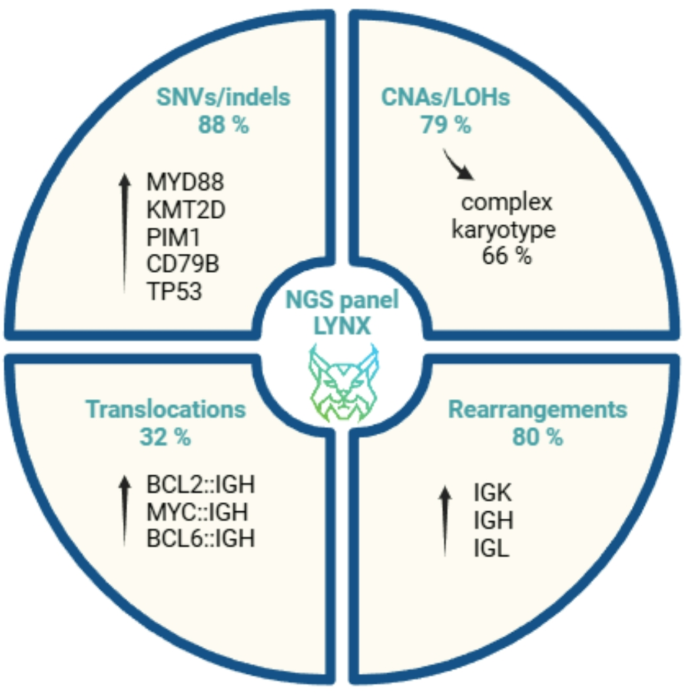
Biomarker定位:本研究涉及的Biomarker包括三类:一是基因变异标志物(MYD88、PIM1、KMT2D、CD79B等),二是染色体畸变标志物(拷贝数变异、杂合性缺失等),三是抗原受体重排标志物(免疫球蛋白IG、T细胞受体TR重排);筛选与验证逻辑为:基于领域内已知的CNSL驱动基因和分子特征,通过多靶点NGS panel在真实世界队列中进行全景式检测,经FFPE组织样本验证标志物的一致性,对比传统流式细胞术的性能以明确诊断价值。
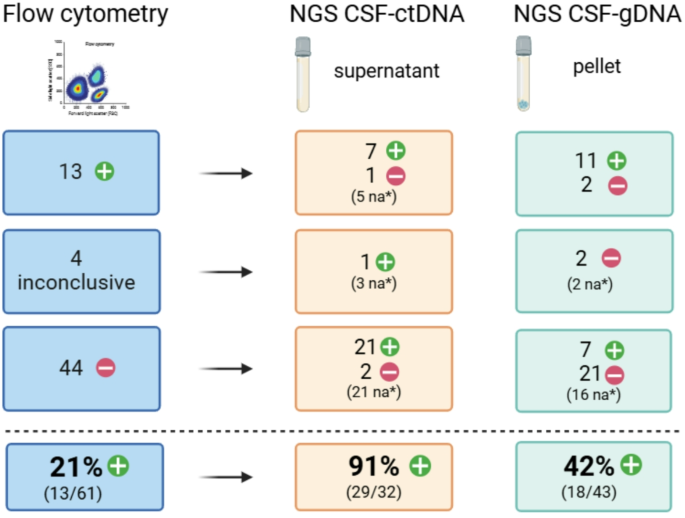
研究过程详述:Biomarker来源为患者脑脊液、血浆的cfDNA和gDNA,以及FFPE组织样本;验证方法包括多靶点NGS、dPCR、流式细胞术;特异性与敏感性数据:多靶点NGS检测脑脊液ctDNA的灵敏度为90%,单靶点MYD88检测灵敏度为46%(P=0.001);脑脊液ctDNA检测的灵敏度91%,显著高于流式细胞术的21%(P<0.001);真实世界队列中,7例流式细胞术阴性的患者经脑脊液ctDNA检测发现亚临床CNS浸润,提示其具有较高的临床预测价值,ROC曲线数据文献未明确提供。
核心成果提炼:本研究明确CNSL最常见的基因变异为MYD88(50%,n=28)、PIM1(36%,n=20)、KMT2D(36%,n=20),染色体畸变发生率达79%(n=44),且84%的畸变患者为复杂核型(≥5个缺陷);首次在真实世界场景中证明多靶点NGS检测脑脊液ctDNA的灵敏度远高于传统方法,可发现亚临床CNS浸润,为患者早期干预提供依据;脑脊液是CNSL ctDNA检测的最优样本类型,常规NGS方法即可实现高灵敏度检测,无需依赖超灵敏技术;统计学结果显示,脑脊液ctDNA与流式细胞术的检测率差异具有显著统计学意义(P<0.001),多靶点与单靶点检测的差异也具有显著统计学意义(P=0.001)。