1. 领域背景与文献引入
文献英文标题:PET-based radiomics visualizes tumor-infiltrating CD8 T cell exhaustion to optimize radiotherapy/immunotherapy combination in mouse models of lung cancer;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肺癌放疗与免疫治疗联合策略、肿瘤免疫微环境、PET放射组学生物标志物
领域共识:晚期非小细胞肺癌(NSCLC)是全球癌症死亡的主要原因之一,2010年后免疫检查点抑制剂(ICI)的问世显著改善了患者预后,2019年PEMBRO-RT研究证实立体定向体部放疗(SBRT)后7天内联合帕博利珠单抗可使晚期NSCLC患者的客观缓解率翻倍,确立了放疗与免疫治疗联合的临床价值。当前领域研究热点聚焦于联合治疗的最优时机筛选、疗效预测生物标志物开发,核心未解决问题包括:消融放疗后肿瘤浸润CD8+T细胞的整体浸润及耗竭亚群的动态变化规律尚未明确,临床中无法通过重复活检实现实时监测,导致联合治疗时机的选择缺乏精准依据。本研究针对这一空白,旨在系统描绘放疗后CD8+T细胞耗竭的动态图谱,并开发非侵入性PET放射组学方法可视化耗竭状态,为优化肺癌放疗与免疫治疗联合策略提供关键支撑。
2. 文献综述解析
作者围绕“放疗与免疫治疗联合的临床潜力- CD8+T细胞作为ICI疗效标志物的价值- T细胞耗竭亚群的功能差异- 现有监测方法的局限性”的逻辑展开综述,对领域内研究进行分类整合。现有研究已证实,肿瘤浸润CD8+T细胞的丰度是ICI治疗反应及患者预后的潜在生物标志物,其中早期耗竭CD8+T细胞(PD-1int)可被ICI重新激活,而终末耗竭CD8+T细胞(PD-1hi)对ICI无反应,二者的比例与NSCLC患者预后密切相关;放疗领域的研究显示,消融剂量放疗(15-25Gy)可大量释放肿瘤抗原和损伤相关分子模式(DAMP),激活抗肿瘤免疫反应,但不同剂量分割方案对肿瘤免疫微环境的影响存在差异,低剂量放疗可逆转免疫沙漠化,但现有研究未明确放疗后CD8+T细胞耗竭亚群的动态变化。现有技术的优势在于放疗能系统性增强免疫治疗的抗肿瘤效应,但局限性在于联合治疗的最优时机仍不明确,且侵入性活检无法实现动态监测。本研究的创新价值在于首次系统描绘了消融放疗后CD8+T细胞浸润及耗竭亚群的动态变化规律,并首次将PET放射组学与T细胞耗竭状态关联,开发了非侵入性的监测方法,填补了领域内的核心空白。
3. 研究思路总结与详细解析
本研究的核心目标是明确消融放疗后肿瘤浸润CD8+T细胞耗竭亚群的动态变化规律,开发并验证非侵入性PET放射组学方法以可视化T细胞耗竭状态,进而优化放疗与免疫治疗联合的时机;核心科学问题为“消融放疗后CD8+T细胞浸润及耗竭亚群的动态演化规律是什么?如何通过PET放射组学特征非侵入性评估T细胞耗竭状态?”;技术路线遵循“模型构建→干预处理→多组学分析→成像特征筛选→模型验证→结论推导”的闭环逻辑。
3.1 肿瘤小鼠模型构建与干预处理
实验目的:构建肺癌小鼠模型,分别模拟放疗和ICI治疗的临床场景,为后续分析CD8+T细胞的动态变化提供实验载体。
方法细节:将小鼠Lewis肺癌(LLC)细胞和B16黑色素瘤细胞分别接种于C57BL/6N小鼠右侧flank,待肿瘤体积达到200mm³时(接种后10天,定义为D0)进行分组处理:放疗组(RT组)给予单次20Gy消融放疗;ICI组给予5次抗PD-L1抗体(10F.9G2)腹腔注射,每3天1次。每个时间点每组3只小鼠,重复3次独立实验。
结果解读:LLC模型对ICI治疗耐药,B16模型对ICI治疗敏感,两种模型的T细胞耗竭基线水平存在差异(LLC模型终末耗竭T细胞比例约40%,B16模型约20%),为后续构建异质性耗竭状态提供了基础。
产品关联:实验所用关键产品:BioXcell的抗PD-L1抗体(货号10F.9G2)、Miltenyi Biotec的肿瘤解离试剂盒、BioLegend的CD45、CD3、CD4、CD8、PD-1、TIM-3流式抗体、eBioscience的TOX抗体、BD的TCF-1抗体、Siemens Preclinical Solution的Inveon micro-PET/CT扫描仪。
3.2 放疗后肿瘤免疫微环境动态分析
实验目的:明确消融放疗后肿瘤浸润CD8+T细胞及其他免疫细胞的动态变化规律。
方法细节:在放疗后D0、D3、D7、D14、D21五个时间点收集LLC肿瘤组织,采用CIBERSORT分析免疫细胞亚群的浸润比例,同时通过流式细胞术检测CD8+T细胞的耗竭亚群比例(PD-1int早期耗竭、PD-1hi终末耗竭)及PD-1的平均荧光强度(MFI)。
结果解读:CIBERSORT分析显示,放疗后3-14天CD8+T细胞及其他免疫促进细胞(活化NK细胞、M1巨噬细胞)的浸润比例显著增加,14天后降至基线以下(n=3,#P<0.1);流式细胞术结果显示,终末耗竭CD8+T细胞比例在放疗后7-14天显著占主导(69.44%~76.35%,n=3,***P<0.001),提示放疗后3-7天是给予ICI治疗的潜在最优窗口。
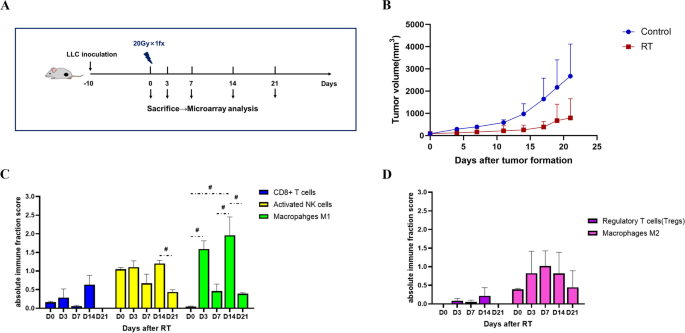
产品关联:实验所用关键产品:BioLegend的流式抗体、BD Fortessa流式细胞仪、CIBERSORTx在线分析工具。
3.3 ICI处理对T细胞耗竭的影响分析
实验目的:验证ICI治疗对不同耗竭状态CD8+T细胞的重塑作用,构建异质性T细胞耗竭模型,为放射组学特征筛选提供训练集。
方法细节:对LLC和B16小鼠模型给予5次抗PD-L1抗体治疗,在治疗前后通过流式细胞术检测CD8+T细胞的早期/终末耗竭比例、PD-1的MFI。
结果解读:LLC模型(基线终末耗竭比例约40%)经ICI治疗后,早期耗竭T细胞比例及PD-1 MFI无显著变化(n=3,P>0.05),提示耐药;B16模型(基线终末耗竭比例约20%)经ICI治疗后,早期耗竭T细胞比例显著降低,PD-1 MFI显著下降(n=3,***P<0.001),提示T细胞耗竭被有效逆转,验证了早期耗竭T细胞对ICI的反应性。
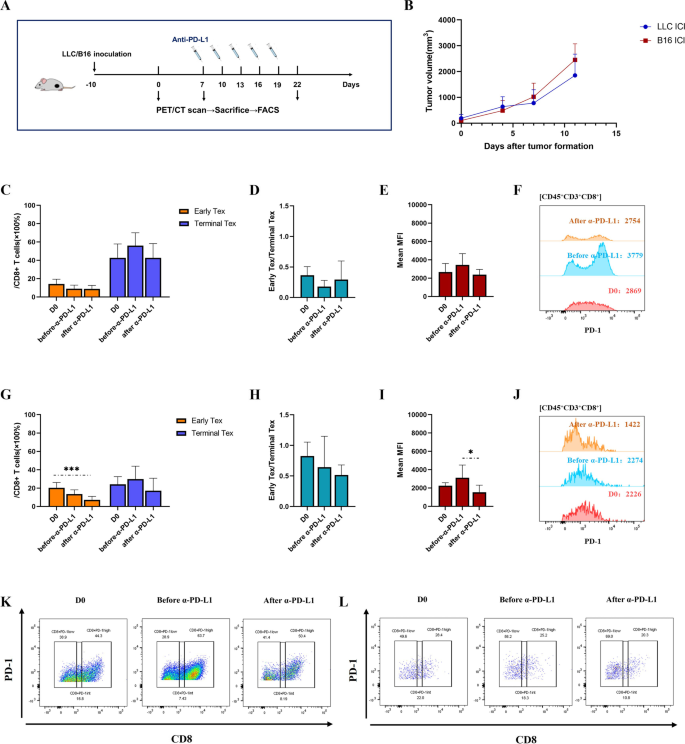
产品关联:实验所用关键产品:BioXcell的抗PD-L1抗体、BioLegend的流式抗体、BD Fortessa流式细胞仪。
3.4 PET放射组学模型构建与验证
实验目的:开发并验证基于PET图像的放射组学模型,实现非侵入性评估T细胞耗竭状态。
方法细节:对放疗组和ICI组小鼠进行多时间点micro-PET/CT成像,注射18F-FDG后1小时扫描,手动勾画肿瘤感兴趣区(ROI),提取57个CT特征和61个PET特征;通过重测分析筛选具有良好鲁棒性的特征(CT特征CCC>0.75,PET特征CCC>0.65);以ICI组为训练集,采用LASSO逻辑回归筛选与T细胞耗竭相关的特征,构建二元逻辑回归模型;以放疗组为验证集,采用C-index、Brier score、校准曲线评估模型的区分度和拟合度。
结果解读:筛选得到3个PET特征(GLCM逆方差、GLCM同质性2、强度直方图峰度)构建模型,训练集C-index为0.818,Brier score为0.156;验证集C-index为0.776,Brier score为0.111,校准曲线显示预测值与实际值拟合良好;进一步可视化显示,PET图像的异质性纹理(局部同质性降低)与终末耗竭T细胞比例正相关,提示可通过PET图像的纹理特征判断T细胞耗竭状态。
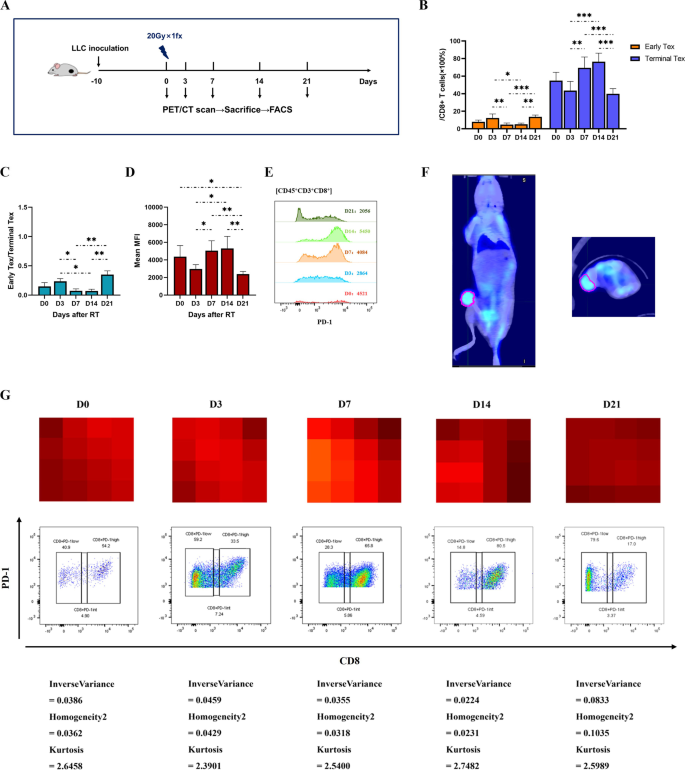
产品关联:实验所用关键产品:Siemens Preclinical Solution的Inveon micro-PET/CT扫描仪、MIM Maestro Version 7.1.4图像分析软件、Imaging biomarker explorer(IBEX)特征提取工具。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker为基于18F-FDG PET图像的放射组学特征组合,属于成像学生物标志物,其筛选与验证逻辑为“ICI处理模型构建异质性耗竭状态→放射组学特征筛选→LASSO回归构建模型→放疗组外部验证→临床转化潜力分析”。
该Biomarker的来源为肺癌小鼠模型的肿瘤18F-FDG PET/CT图像,验证方法包括重测分析评估特征鲁棒性、LASSO回归筛选与T细胞耗竭相关的特征、二元逻辑回归构建模型,通过C-index、Brier score、校准曲线验证模型的性能;特异性与敏感性数据显示,训练集(ICI组)的C-index为0.818(文献未明确提供95%CI),验证集(放疗组)的C-index为0.776,Brier score分别为0.156和0.111,提示模型具有良好的区分度和拟合度。
核心成果方面,该放射组学模型可准确区分T细胞的耗竭状态,PET图像的异质性纹理特征与终末耗竭CD8+T细胞比例呈负相关(局部同质性越低,终末耗竭比例越高);创新性在于首次将PET放射组学特征与T细胞耗竭状态关联,实现了非侵入性监测放疗后肿瘤免疫微环境的动态变化,同时明确了放疗后3-7天是ICI治疗的潜在最优窗口,临床研究提示该窗口内治疗可翻倍缓解率,但文献未明确提供风险比(HR)数据。此外,该Biomarker为临床实时评估肿瘤免疫反应性、优化联合治疗时机提供了非侵入性的解决方案,具有重要的转化潜力,未来需在NSCLC患者中进一步验证其临床价值。
