1. 领域背景与文献引入
文献英文标题:Arginine methylation in cancer: mechanisms and therapeutic implications;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤表观遗传学与靶向治疗
精氨酸甲基化是关键的蛋白质翻译后修饰类型,于20世纪60年代首次被发现,1996年蛋白质精氨酸甲基转移酶1(PRMT1)的克隆推动了领域的快速发展。当前,PRMT家族介导的精氨酸甲基化已成为肿瘤表观遗传学研究的热点,其通过调控蛋白质稳定性、酶活性、亚细胞定位等参与肿瘤发生发展的多个核心环节。领域发展的关键节点包括:2010年后PRMT在肿瘤标志中的系统研究,2016年发现甲基硫代腺苷磷酸化酶(MTAP)缺失与PRMT5的合成致死关系,2020年后蛋白降解靶向嵌合体(PROTAC)等新型PRMT靶向技术的出现。当前研究热点集中于PRMT亚型在不同肿瘤中的特异性作用机制、PRMT介导的甲基化与其他表观修饰的交互调控网络,以及靶向PRMT的新型抑制剂开发。未解决的核心问题包括:部分PRMT亚型(如PRMT8、PRMT9)的肿瘤功能研究相对匮乏,PRMT介导的甲基化与其他翻译后修饰的协同调控机制尚未完全阐明,临床PRMT抑制剂存在选择性不足、毒性较大等问题,部分抑制剂的临床疗效有限。
结合领域现状,本综述针对PRMT家族在肿瘤中的作用机制缺乏系统整合的研究空白,全面总结了PRMT的分类、结构功能、上游调控、肿瘤标志关联及靶向治疗进展,为PRMT靶向的精准肿瘤治疗提供了理论基础与转化方向。
2. 文献综述解析
本综述以PRMT家族的研究脉络为主线,从分类与结构、生物学功能、肿瘤标志关联、靶向治疗进展四个维度对现有研究进行系统综述,明确了PRMT在肿瘤发生发展中的核心作用及临床转化潜力。
现有研究的关键结论包括:PRMT家族通过调控转录、RNA加工、信号通路等多个层面参与肿瘤持续增殖、细胞逃逸死亡、侵袭转移、代谢重编程等核心标志;不同PRMT亚型具有独特的结构特征与底物特异性,决定了其在肿瘤中的差异化功能;MTAP缺失与PRMT5存在合成致死效应,为PRMT5靶向治疗提供了精准筛选依据。技术方法优势在于:结构生物学解析了PRMT的催化结构域与底物结合模式,多组学技术鉴定了大量PRMT底物与下游调控网络,细胞和动物实验验证了PRMT在肿瘤中的功能。现有研究的局限性包括:PRMT8、PRMT9等亚型的肿瘤功能研究不足,PRMT介导的甲基化与其他表观修饰的交互调控网络尚未完全解析,临床PRMT抑制剂的选择性和毒性问题待解决,部分抑制剂的临床疗效有限。
本综述的创新价值在于:系统整合了PRMT在肿瘤中的多层面作用机制,涵盖从分子结构到临床转化的全链条研究进展;重点突出了最新的PRMT靶向治疗技术,包括MTA协同抑制剂、PROTAC降解剂等,为临床转化提供了全面的参考框架;同时,明确了PRMT作为肿瘤Biomarker的潜在价值,为精准肿瘤治疗的患者筛选提供了依据。
3. 研究思路总结与详细解析
本综述以“PRMT家族基础特征→生物学功能调控→肿瘤标志关联机制→靶向治疗进展”为逻辑框架,系统梳理了PRMT在肿瘤中的作用机制及临床转化潜力,为PRMT靶向的精准肿瘤治疗提供了系统的理论支撑。
3.1 PRMT家族分类与结构特征
实验目的:明确PRMT家族的分类依据、结构特征及底物特异性,为理解其生物学功能奠定基础。
方法细节:现有研究采用结构生物学技术(如X射线晶体学、冷冻电镜)解析PRMT的催化结构域与辅助结构域,通过肽库筛选、质谱鉴定等方法分析PRMT的底物结合基序。
结果解读:PRMT家族分为I、II、III型,各亚型具有保守的催化结构域(包含Motif I、Post-I、Motif II、III等核心基序),同时具有独特的非催化结构域(如PRMT2的Src同源3(SH3)结构域、PRMT3的锌指结构域),决定了其底物特异性。例如,PRMT1、PRMT3等偏好甲基化甘氨酸-精氨酸富集(GAR)基序的底物,PRMT4偏好精氨酸相邻脯氨酸-甘氨酸-甲硫氨酸(PGM)基序,PRMT7偏好RxR基序。
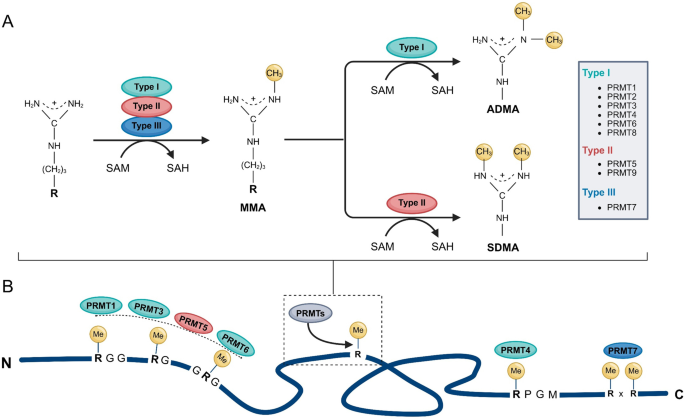
产品关联:文献未提及具体实验产品,领域常规使用重组PRMT蛋白、底物肽库、质谱分析平台等。
3.2 PRMT的生物学功能调控
实验目的:阐明PRMT在细胞内的生物学功能调控机制,包括转录、RNA加工、信号通路等层面。
方法细节:现有研究采用染色质免疫沉淀测序(ChIP-seq)、RNA测序(RNA-seq)、RNA免疫沉淀测序(RIP-seq)等多组学技术分析PRMT对转录组和RNA加工的调控,通过免疫共沉淀、蛋白质免疫印迹(Western blot)等方法验证PRMT与底物的相互作用。
结果解读:PRMT通过甲基化组蛋白调控转录(如PRMT1催化组蛋白H4精氨酸3不对称二甲基化(H4R3me2a)促进转录激活,PRMT5催化H4R3对称二甲基化(H4R3me2s)抑制转录);通过甲基化剪接因子调控RNA可变剪接(如PRMT5甲基化Sm蛋白参与小核核糖核蛋白(snRNP)组装);通过甲基化信号通路蛋白调控细胞信号(如PRMT1甲基化表皮生长因子受体(EGFR)增强其信号活性)。此外,PRMT还通过非催化机制参与细胞功能调控,如PRMT8具有内在磷脂酶活性,可同时作为甲基转移酶和脂质修饰酶发挥作用。
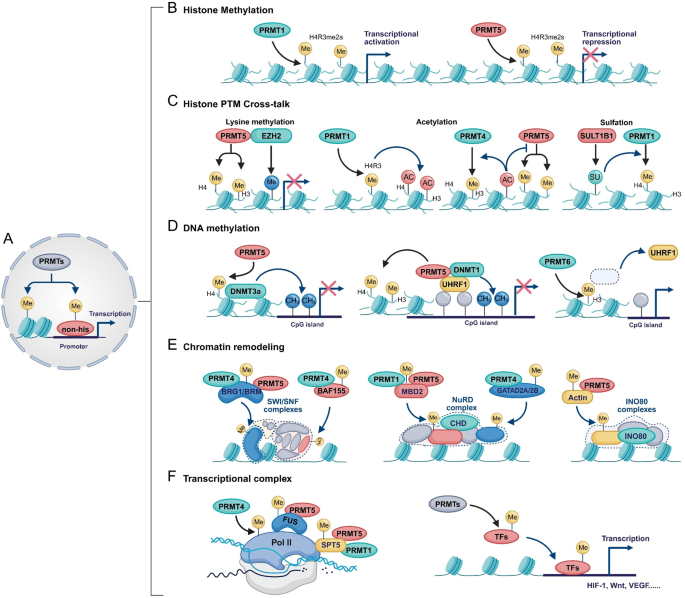
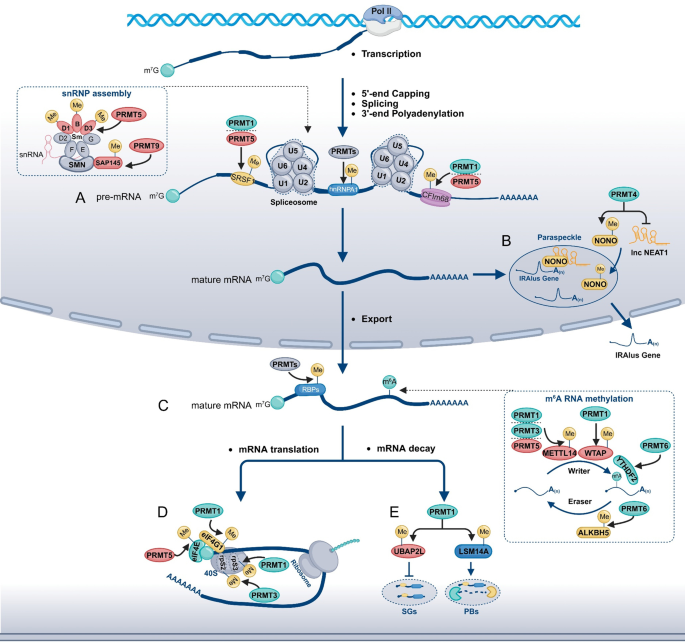
产品关联:文献未提及具体实验产品,领域常规使用ChIP试剂盒、RNA-seq文库构建试剂盒、Western blot抗体等。
3.3 PRMT与肿瘤标志的关联机制
实验目的:解析PRMT在肿瘤各标志中的作用机制,包括持续增殖、细胞逃逸死亡、侵袭转移、代谢重编程等。
方法细节:现有研究采用细胞系敲低/过表达实验、异种移植动物模型、临床样本分析等方法,结合多组学技术鉴定PRMT调控的下游靶基因与通路。
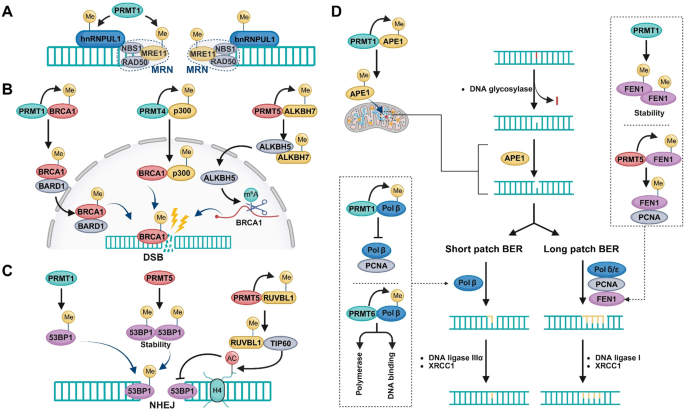
结果解读:PRMT通过调控细胞周期相关基因(如PRMT4激活E2F1促进细胞增殖)、抗凋亡蛋白(如PRMT1甲基化热休克蛋白70(HSP70)稳定BCL2抑制凋亡)、上皮间质转化(EMT)相关转录因子(如PRMT5抑制E-钙粘蛋白促进侵袭转移)、代谢酶(如PRMT6甲基化乳酸脱氢酶A(LDHA)促进糖酵解)等参与肿瘤多个标志。此外,PRMT还参与肿瘤免疫逃逸,如PRMT1甲基化环GMP-AMP合成酶(cGAS)抑制干扰素基因刺激蛋白(STING)通路激活,削弱抗肿瘤免疫应答。
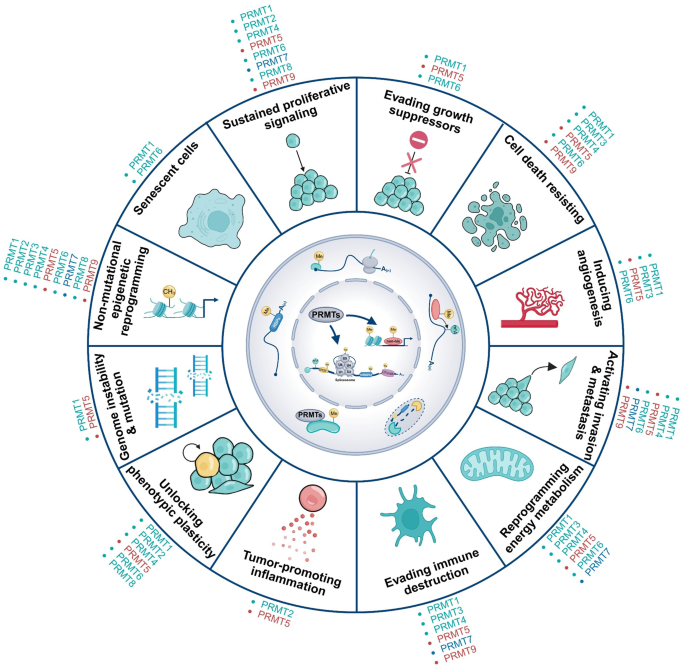
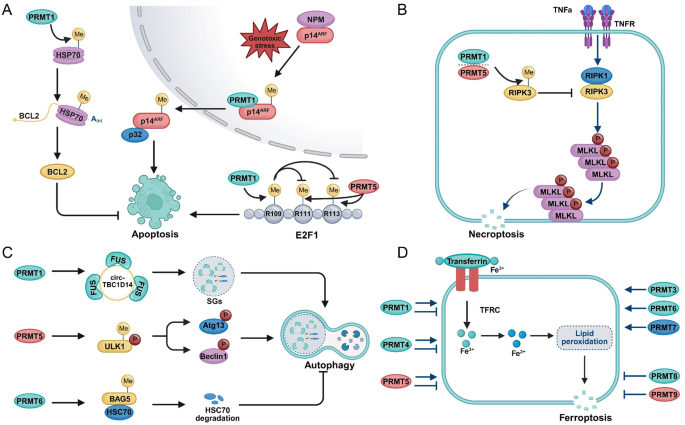
产品关联:文献未提及具体实验产品,领域常规使用CRISPR/Cas9基因编辑工具、肿瘤异种移植模型、免疫组化检测试剂盒等。
3.4 PRMT靶向治疗策略进展
实验目的:总结PRMT靶向治疗的研究进展,包括抑制剂开发、PROTAC技术、联合治疗策略等。
方法细节:现有研究采用高通量筛选、结构生物学辅助药物设计、细胞和动物模型验证抑制剂疗效,临床研究评估抑制剂的安全性和有效性。
结果解读:PRMT抑制剂分为I型、II型、III型抑制剂,其中II型PRMT5抑制剂研究最为深入,包括第一代非选择性抑制剂(如GSK3326595)和第二代MTA协同抑制剂(如MRTX1719、AMG193),后者在MTAP缺失肿瘤中具有合成致死效应,临床研究显示其在MTAP缺失的黑色素瘤、胆囊癌等患者中具有客观缓解。此外,PROTAC等新型技术已应用于PRMT降解剂开发(如YZ-836P、MS4322),联合治疗策略(如PRMT抑制剂与免疫检查点抑制剂联合)显示出良好的抗肿瘤效果,可增强细胞毒性T细胞浸润与抗肿瘤免疫应答。
产品关联:实验所用关键产品:PRMT5抑制剂MRTX1719、AMG193,PRMT降解剂YZ-836P、MS4322。
4. Biomarker研究及发现成果解析
Biomarker定位
本综述中涉及的Biomarker包括PRMT家族成员作为肿瘤预后Biomarker,以及MTAP缺失作为PRMT5抑制剂的伴随诊断Biomarker。筛选与验证逻辑为:PRMT家族成员通过临床样本表达分析结合预后关联统计确定预后价值;MTAP缺失通过基因组分析结合合成致死实验验证其作为PRMT5抑制剂的预测价值,后续通过临床研究进一步确认疗效相关性。
研究过程详述
PRMT1在胰腺癌、乳腺癌等多种肿瘤中高表达,与患者不良预后相关(文献未明确提供具体样本量与统计学数据);PRMT5在MTAP缺失肿瘤中具有合成致死效应,临床研究显示MRTX1719在MTAP缺失的黑色素瘤、胆囊癌、间皮瘤等患者中具有客观缓解(文献未明确提供敏感性与特异性数据);PRMT7在慢性髓系白血病干细胞中调控甘氨酸代谢,可作为白血病干细胞的潜在Biomarker,其缺失可导致甲基乙二醛积累,选择性清除白血病干细胞。此外,PRMT介导的组蛋白甲基化修饰(如H4R3me2a、H4R3me2s)可作为肿瘤表观遗传学Biomarker,反映肿瘤的表观调控状态。
核心成果提炼
PRMT家族成员可作为多种肿瘤的预后Biomarker,其中PRMT1高表达提示不良预后;MTAP缺失可作为PRMT5抑制剂的伴随诊断Biomarker,为PRMT靶向治疗的患者筛选提供依据,其临床转化已进入早期临床试验阶段。此外,PRMT介导的底物甲基化修饰可作为肿瘤表观遗传学Biomarker,为肿瘤的分子分型与预后评估提供参考。目前部分Biomarker的统计学数据(如风险比HR、ROC曲线AUC值)尚未在综述中明确提供,需后续临床研究进一步验证。
