1. 领域背景与文献引入
文献英文标题:The CDK9 inhibitor enitociclib overcomes resistance to BTK inhibition and CAR-T therapy in mantle cell lymphoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:血液肿瘤(套细胞淋巴瘤)治疗耐药机制及靶向治疗。
套细胞淋巴瘤(MCL)是一类侵袭性极高的非霍奇金淋巴瘤亚型,近十年来,Bruton酪氨酸激酶(BTK)抑制剂(如伊布替尼、阿卡替尼等)及靶向CD19的嵌合抗原受体T细胞(CAR-T)治疗为MCL患者带来了突破性的生存获益,成为临床治疗的核心方案。然而,随着临床应用的推广,BTK抑制剂耐药及BTK抑制剂-CAR-T双重耐药导致的疾病复发已成为亟待解决的临床难题。领域共识:现有研究表明,MYC通路的异常激活是MCL耐药发生的关键分子机制之一,但针对该通路的靶向治疗策略仍存在特异性不足、疗效有限等问题,亟需探索新的耐药靶点及治疗方案。在此背景下,本研究聚焦于转录延伸关键因子细胞周期蛋白依赖性激酶9(CDK9),通过体内外实验验证其选择性抑制剂Enitociclib在MCL耐药模型中的疗效及作用机制,为耐药患者提供新的治疗选择。
2. 文献综述解析
作者以MCL治疗的技术进展及耐药机制为分类维度,系统评述了现有研究的成果与局限性。
现有研究中,BTK抑制剂及CD19 CAR-T治疗是MCL领域的范式转变,显著改善了复发难治性患者的预后,但临床数据显示,约30%-50%的患者会在治疗后出现耐药复发,且双重耐药患者的预后极差。耐药机制研究方面,单细胞转录组分析显示MYC靶点基因集在耐药样本中显著富集,提示MYC介导的转录重编程是耐药的核心特征;针对CDK9的靶向治疗在其他血液肿瘤(如弥漫大B细胞淋巴瘤)中已显示出一定疗效,但选择性CDK9抑制剂Enitociclib在MCL耐药模型中的作用尚未被报道。本研究通过对比现有耐药治疗方案的空白,首次将CDK9作为MCL双重耐药的潜在靶点,验证Enitociclib的疗效,为MCL耐药治疗提供了新的方向。
3. 研究思路总结与详细解析
本研究的核心目标是验证CDK9抑制剂Enitociclib在MCL耐药模型中的抗肿瘤活性及作用机制,核心科学问题为CDK9是否通过调控MYC等短寿命蛋白的转录合成介导MCL治疗耐药,技术路线遵循“靶点筛选→体外机制验证→体内疗效验证”的闭环逻辑。
3.1 耐药样本转录组特征分析与靶点筛选
实验目的为明确MCL耐药发生的关键分子特征,筛选潜在的治疗靶点。研究采用单细胞RNA测序技术,对BTK抑制剂敏感、BTK抑制剂耐药及BTK抑制剂-CAR-T双重耐药的MCL患者样本进行转录组分析,通过基因集富集分析(GSEA)及差异基因表达对比,发现MYC靶点基因集在耐药样本中呈渐进式富集,且CDK9在双重耐药样本中的表达水平显著高于单纯BTK抑制剂耐药样本。该结果提示CDK9可能是介导MCL双重耐药的关键分子,为后续靶向实验提供了依据。文献未提及具体实验产品,领域常规使用单细胞测序平台、生物信息学分析软件等。
3.2 Enitociclib体外抗淋巴瘤活性验证
实验目的为检测Enitociclib对MCL细胞的体外抑制活性。研究采用细胞活力检测实验,在9株MCL细胞系、5株弥漫大B细胞淋巴瘤细胞系及原代MCL细胞中检测Enitociclib的半数抑制浓度(IC₅₀),结果显示其IC₅₀范围为32-172 nM,表明Enitociclib对淋巴瘤细胞具有高度的体外抑制活性;进一步通过流式细胞术检测发现,Enitociclib以剂量和时间依赖的方式诱导MCL细胞凋亡,且在耐药细胞系中的活性与敏感细胞系无显著差异。文献未提及具体实验产品,领域常规使用细胞活力检测试剂盒、流式细胞仪等。
3.3 Enitociclib作用机制的分子验证
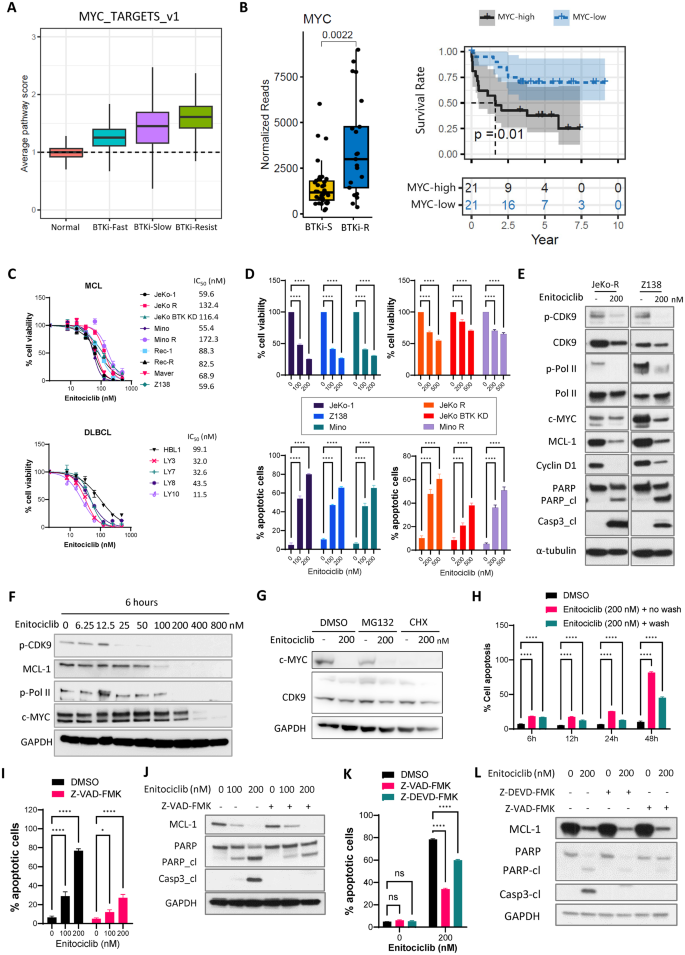
实验目的为明确Enitociclib通过抑制CDK9调控下游信号通路的具体机制。研究采用蛋白质免疫印迹技术,检测Enitociclib处理后CDK9磷酸化水平、RNA聚合酶II(Pol II)Ser2位点磷酸化水平及下游短寿命蛋白的表达变化,结果显示处理6小时后,CDK9及Pol II Ser2的磷酸化水平显著降低,c-MYC、MCL-1、Cyclin D1的表达呈剂量依赖性下调;通过加入翻译抑制剂环己酰亚胺(CHX)及蛋白酶体抑制剂MG132,发现CHX可模拟Enitociclib的作用降低c-MYC表达,而MG132无法逆转Enitociclib诱导的c-MYC下调,表明Enitociclib通过抑制蛋白的新合成而非促进降解发挥作用。同时,蛋白质免疫印迹及凋亡检测实验显示,Enitociclib可激活caspase-3介导的凋亡通路,泛caspase抑制剂Z-VAD-FMK及caspase-3特异性抑制剂Z-VEAD-FMK可显著抑制Enitociclib诱导的细胞凋亡(n=3,P<0.01),证实凋亡依赖于caspase-3的激活。文献未提及具体实验产品,领域常规使用蛋白质免疫印迹试剂盒、caspase抑制剂等。
3.4 体内异种移植模型疗效验证
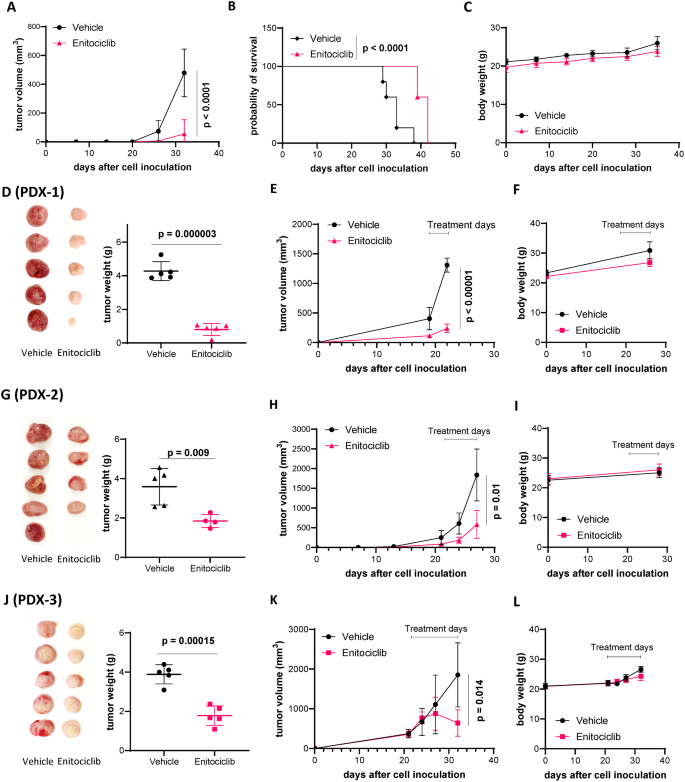
实验目的为验证Enitociclib在体内MCL耐药模型中的抗肿瘤活性及安全性。研究首先构建JeKo-1细胞系异种移植模型(CDX),给予Enitociclib(10mg/kg,静脉注射,每周2次),结果显示Enitociclib显著抑制肿瘤生长(P<0.0001),延长小鼠生存期(P<0.0001),且未导致小鼠体重显著下降,提示其具有良好的体内安全性。进一步构建3例患者来源异种移植模型(PDX),分别对应BTK抑制剂耐药、BTK抑制剂-维奈克拉双重耐药、BTK抑制剂-CAR-T双重耐药的临床样本,Enitociclib在所有PDX模型中均显著抑制肿瘤生长,其中BTK抑制剂耐药模型的肿瘤生长抑制率对应的P值为0.00015,BTK抑制剂-维奈克拉双重耐药模型为0.009,BTK抑制剂-CAR-T双重耐药模型为0.000003,且所有模型中小鼠体重均无显著变化,证实Enitociclib可有效克服多种类型的MCL治疗耐药。文献未提及具体实验产品,领域常规使用免疫缺陷小鼠(NSG)、肿瘤体积测量工具等。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为CDK9,作为MCL治疗耐药的潜在预测Biomarker及治疗靶点,其筛选与验证逻辑为通过单细胞转录组分析耐药与敏感样本的差异表达,结合功能实验验证其调控耐药的机制。
CDK9的来源为MCL患者的耐药样本转录组数据,研究通过体外细胞实验验证Enitociclib抑制CDK9活性后,可下调MYC、MCL-1等短寿命蛋白的表达,诱导细胞凋亡;体内异种移植模型进一步证实,针对CDK9的靶向治疗可有效抑制耐药肿瘤的生长。目前研究尚未提供CDK9表达水平与MCL患者临床耐药结局的相关性数据,其作为预测Biomarker的特异性与敏感性仍需大样本临床研究验证。核心成果方面,CDK9被证实为MCL治疗耐药的关键调控靶点,Enitociclib通过抑制CDK9介导的转录延伸,下调MYC通路活性,诱导caspase-3依赖的凋亡,有效克服BTK抑制剂及CAR-T治疗的耐药性;该研究的创新性在于首次在MCL双重耐药模型中验证了选择性CDK9抑制剂的疗效,为复发难治性MCL患者提供了新的治疗策略,同时为CDK9作为Biomarker的临床转化奠定了基础。
