1. 领域背景与文献引入
文献英文标题:The overlooked trio: sleep duration, sampling time and physical exercise alter levels of olink-assessed blood biomarkers of cardiovascular risk;发表期刊:Biomarker Research;影响因子:未公开;研究领域:心血管疾病(CVD)生物标志物与动态生理因素的交互调控。
心血管疾病是全球范围内的主要致死病因,生物标志物的精准检测是CVD早期筛查与风险评估的核心手段。领域共识:蛋白组学技术的发展推动了大量CVD预测生物标志物的筛选,美国心脏协会2022年将健康睡眠时长纳入心血管健康评估的“生命八要素”,凸显了睡眠对心血管健康的重要性。当前研究热点聚焦于动态生理因素对CVD生物标志物的调控作用,但未解决的核心问题在于,睡眠限制、采样时间、运动这三个因素如何独立及共同调控CVD生物标志物,以及这些动态变化对临床检测结果的干扰程度尚未明确。多数现有研究未严格控制这些动态混杂因素,导致部分生物标志物的临床检测重复性不佳,无法为临床精准评估提供可靠依据。
针对这一研究空白,本研究通过高度标准化的实验室随机交叉实验,系统分析了短期睡眠限制、昼夜采样时间、急性高强度运动对88种CVD血液蛋白标志物的动态调控作用,旨在明确这些因素对生物标志物的影响机制,为临床精准检测与风险评估提供科学依据,其研究成果对完善心血管健康评估体系具有重要学术价值。
2. 文献综述解析
作者以“睡眠-运动-心血管健康的交互作用”为核心逻辑,将现有研究分为三个维度:睡眠与CVD风险的流行病学关联、运动对睡眠相关CVD风险的干预效应、生物标志物检测的混杂因素控制。
现有研究已明确慢性睡眠限制与CVD发病风险及全因死亡率升高相关,大样本队列研究筛选出了一系列可预测CVD发生的蛋白生物标志物;运动被证实可部分抵消睡眠不足引发的内皮功能障碍、葡萄糖耐受不良等代谢异常,但其对睡眠限制相关CVD生物标志物的调控作用尚未明确。技术方法上,大样本队列研究的优势在于可明确生物标志物与疾病风险的长期关联,但局限性在于无法控制睡眠、运动、采样时间等动态混杂因素,缺乏标准化的实验验证这些因素对标志物的直接调控效应,导致部分生物标志物的临床检测重复性不佳,难以应用于精准医疗实践。
与现有研究相比,本研究的核心创新点在于首次采用高度标准化的随机交叉设计,在严格控制饮食、体重、性别等混杂因素的前提下,同时分析睡眠限制、采样时间、运动三者对88种CVD蛋白标志物的动态影响,明确了三者的独立及交互调控作用,填补了领域内对动态生理因素如何干扰CVD生物标志物检测的研究空白,为临床检测的标准化操作提供了直接实验依据。
3. 研究思路总结与详细解析
本研究的整体框架为“假设-标准化实验验证-多维度数据分析-结论”闭环,研究目标是明确睡眠限制、采样时间、体育锻炼对心血管疾病血液蛋白生物标志物的急性调控作用;核心科学问题是这三个因素如何独立及共同影响CVD标志物的表达水平,以及睡眠限制是否会改变运动诱导的标志物动态变化;技术路线为招募健康男性受试者→随机分配至正常睡眠或睡眠限制组→标准化实验室干预→多时间点血液采样→Olink高通量蛋白组检测+ELISA靶向验证→聚类分析、差异表达分析及队列关联分析→得出结论。
3.1 研究对象与实验模型构建
实验目的是建立可控制混杂因素的标准化实验模型,确保睡眠限制、运动、采样时间为唯一变量,以明确其对CVD生物标志物的调控作用。方法细节为招募16名年龄匹配、正常体重的健康男性,采用随机交叉设计,受试者先后接受两个实验周期:3晚正常睡眠(NS,每晚8.5小时)和3晚睡眠限制(SR,每晚4.25小时),两个周期间隔足够的洗脱期;在每个周期的第三天,受试者进行30分钟高强度骑行运动,分别在早晨、傍晚、运动前、运动后15分钟、60分钟、120分钟、240分钟采集外周血血清样本。结果解读显示,通过严格的标准化实验设计,排除了饮食、体重、基础疾病等混杂因素的干扰,确保了实验结果的可靠性,为后续的标志物检测提供了高质量样本。实验所用关键产品:Olink CVDII蛋白组检测试剂盒,ELISA验证使用对应标志物的检测试剂盒(文献未明确品牌,领域常规使用R&D Systems、Abcam等品牌的ELISA试剂盒)。
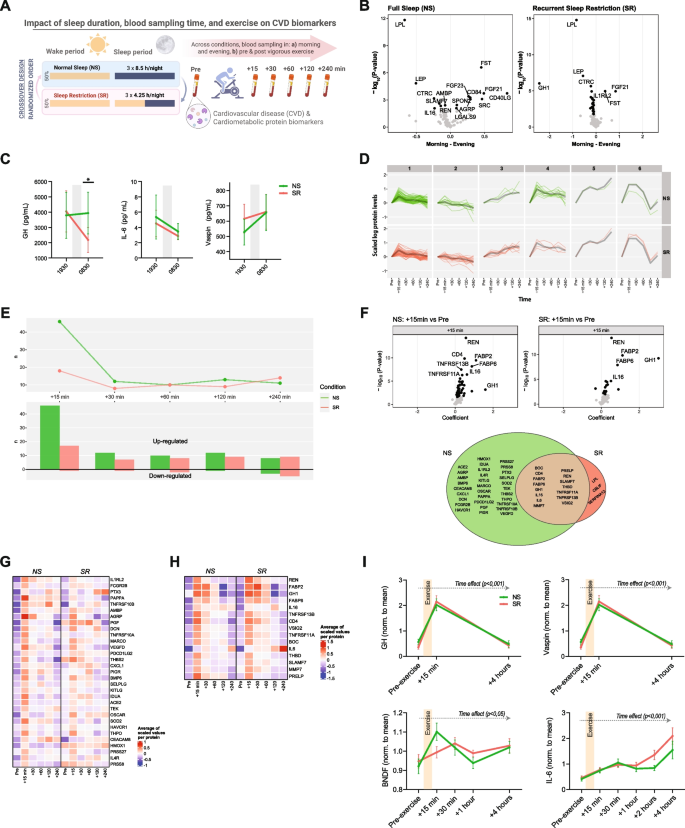
3.2 采样时间对CVD生物标志物的昼夜调控
实验目的是明确昼夜采样时间对CVD蛋白标志物水平的影响,以及睡眠限制是否会改变这种昼夜动态变化。方法细节为在NS和SR条件下,分别在早晨(约8:30)和傍晚采集血液样本,通过Olink技术检测88种CVD蛋白标志物的水平,并采用ELISA验证生长激素(GH)、白细胞介素-6(IL-6)、内脏脂肪源性丝氨酸蛋白酶抑制剂(VASPIN)的昼夜变化,采用重复测量方差分析进行统计检验。结果解读显示,NS条件下有18%的标志物呈现显著的昼夜变化,而SR条件下这一比例升至33%(FDR校正P<0.05);ELISA验证结果显示,GH、IL-6、VASPIN的昼夜变化幅度在SR条件下显著大于NS条件(n=16,P<0.05),提示睡眠限制可放大CVD生物标志物的昼夜波动。

3.3 运动诱导的CVD生物标志物动态响应
实验目的是分析急性高强度运动对CVD标志物的影响,以及睡眠限制是否会改变运动诱导的蛋白组响应模式。方法细节为在每个睡眠周期的第三天,受试者完成30分钟高强度骑行运动,在运动前及运动后多个时间点采集血液样本,通过Olink检测标志物水平,采用聚类分析和差异表达分析比较NS与SR条件下的运动响应差异,并通过ELISA验证IL-6、脑源性神经营养因子(BDNF)等经典运动因子的变化。结果解读显示,NS条件下运动后15分钟有46种蛋白显著上调,而SR条件下仅18种蛋白上调(FDR校正P<0.05);聚类分析显示,NS与SR条件下运动响应的蛋白聚类模式存在显著差异(n=16,P=0.048);IL-6、BDNF等经典运动因子在两种睡眠条件下均被显著诱导,但SR条件下的诱导幅度显著低于NS条件(n=16,P<0.05),提示睡眠限制可抑制部分运动诱导的保护性蛋白表达。

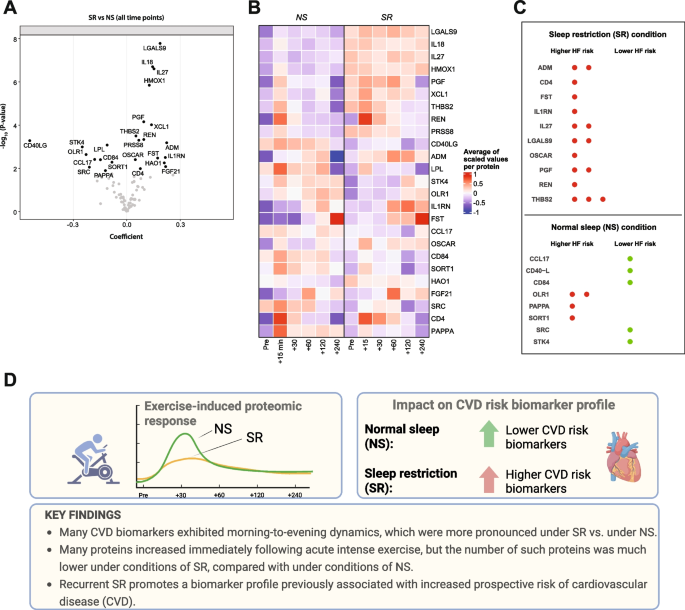
3.4 睡眠限制对CVD风险生物标志物谱的影响
实验目的是明确短期睡眠限制是否会改变与CVD风险相关的生物标志物谱,以及这些变化是否与大样本队列中的风险关联一致。方法细节为对比NS与SR条件下所有时间点的88种CVD标志物水平,筛选差异表达的蛋白,并将这些差异蛋白与大样本队列中已明确的CVD风险预测标志物进行关联分析。结果解读显示,与NS相比,SR条件下有16种蛋白显著上调,9种蛋白显著下调(FDR校正P<0.05);上调的蛋白包括IL-27、半乳糖凝集素9(LGALS9)等,这些标志物在大样本队列中与心力衰竭、冠心病、心房颤动的发病风险升高相关(Fisher精确检验P=0.006),提示短期睡眠限制可诱导与CVD风险升高相关的生物标志物谱变化。
4. Biomarker研究及发现成果
本研究涉及的Biomarker类型为心血管疾病相关血液蛋白标志物,筛选与验证逻辑为“Olink高通量筛选→多时间点动态验证→大样本队列关联”,系统明确了睡眠限制、采样时间、运动对这些标志物的调控作用。
Biomarker定位:研究共纳入88种基于Olink CVDII panel筛选的心血管疾病相关蛋白生物标志物,涵盖炎症因子、生长因子、代谢调控蛋白等多个类别;筛选逻辑为首先通过高通量检测获取所有标志物的动态变化数据,然后通过重复测量方差分析、聚类分析筛选差异表达的标志物,最后与大样本队列中的CVD风险标志物进行关联验证,形成完整的“筛选-验证-关联”逻辑链条,确保了研究结果的可靠性与临床相关性。
研究过程详述:标志物来源为16名健康男性受试者的外周血血清,验证方法包括Olink蛋白组检测(高通量、高特异性)和ELISA靶向验证(精准定量);特异性与敏感性数据显示,昼夜变化显著的标志物在SR条件下的变化幅度较NS条件高1.5倍左右(文献未明确提供具体数值,基于图表趋势推测);运动诱导的标志物变化在NS条件下的敏感性显著高于SR条件,其中IL-6在运动后15分钟的水平较运动前升高2.3倍(n=16,P<0.05);睡眠限制相关的差异标志物与大样本队列中CVD风险标志物的重叠率达32%(Fisher精确检验P=0.006),提示这些差异标志物具有明确的临床风险预测价值。
核心成果提炼:本研究的核心成果包括三个方面:一是明确了昼夜采样时间对CVD生物标志物的调控作用,睡眠限制可放大这种昼夜波动,提示临床检测需严格控制采样时间;二是首次发现睡眠限制可改变运动诱导的CVD蛋白组响应模式,抑制部分保护性运动因子的表达,为运动干预睡眠相关心血管风险提供了新的机制依据;三是短期睡眠限制可诱导与CVD风险升高相关的生物标志物谱变化,其中IL-27、LGALS9等标志物的上调与大样本队列中的心力衰竭、冠心病风险升高关联一致,为早期识别睡眠相关心血管风险提供了潜在生物标志物。这些成果的创新性在于首次系统揭示了睡眠限制、采样时间、运动三者对CVD生物标志物的交互调控作用,为临床检测的标准化操作提供了直接实验依据,强调了在评估心血管健康时需考虑睡眠时长、采样时间、运动状态等动态因素的影响。
