1. 领域背景与文献引入
文献英文标题:Novel insights into the m⁶A-RNA methyltransferase METTL3 in cancer;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤表观遗传学(RNA甲基化调控与肿瘤发生发展)
领域共识:表观遗传学通过DNA、RNA及蛋白的化学修饰在不改变基因组序列的前提下调控基因表达,是肿瘤发生发展的核心调控机制之一。RNA甲基化作为表观遗传学的重要分支,其中N6-甲基腺苷(m⁶A)是真核生物中最常见且功能最明确的RNA内部修饰,其动态调控由“写入器”“擦除器”和“读取器”三类蛋白协同完成。2011年,脂肪量和肥胖相关蛋白(FTO)被鉴定为首个m⁶A去甲基化酶,标志着m⁶A修饰的可逆性被证实;2015年,研究明确甲基转移酶样蛋白3(METTL3)作为m⁶A甲基转移酶复合物(MTC)的核心催化亚基,主导m⁶A的沉积过程,推动领域进入m⁶A调控因子功能研究的爆发期。当前研究热点聚焦于m⁶A调控因子在肿瘤增殖、侵袭、耐药中的功能及靶向治疗潜力,但核心未解决问题包括:METTL3在不同肿瘤中呈现的促癌/抑癌双向作用机制尚不明确,且缺乏针对METTL3的特异性临床转化抑制剂。在此背景下,本研究系统整合现有文献,梳理METTL3在各肿瘤中的功能与调控网络,为其作为肿瘤Biomarker及治疗靶点提供全面参考,具有重要的学术整合价值。
2. 文献综述解析
作者以肿瘤类型为核心分类维度,系统综述了METTL3在胃肠道肿瘤、呼吸道肿瘤、泌尿生殖系统肿瘤、神经系统肿瘤等多类肿瘤中的功能、调控机制及临床意义,同时探讨了靶向METTL3的治疗潜力。
现有研究已证实,METTL3在多数肿瘤中通过调控信使RNA(mRNA)的剪接、翻译、稳定性及非编码RNA(microRNA、长链非编码RNA)的成熟,促进肿瘤细胞增殖、侵袭、代谢重编程及耐药;部分研究也发现METTL3在特定肿瘤或亚型中发挥抑癌作用,如三阴性乳腺癌、子宫内膜癌等。现有研究的优势在于覆盖了多肿瘤类型,且从分子层面揭示了METTL3与RNA的相互作用机制,为理解肿瘤表观遗传调控提供了新视角;但局限性在于不同肿瘤中METTL3作用的异质性机制未被系统阐明,且多数研究停留在细胞及动物实验层面,缺乏大规模临床样本验证及靶向治疗的临床数据。
本研究的创新价值在于首次系统整合了METTL3在各肿瘤中的双向作用及调控网络,明确了其作为预后Biomarker的潜力,并针对性讨论了靶向METTL3的治疗策略,填补了领域内对METTL3异质性作用的整合分析空白,为后续研究提供了清晰的方向。
3. 研究思路总结与详细解析
本研究为系统综述,研究目标是全面梳理METTL3在人类癌症中的功能、调控机制及临床应用潜力,核心科学问题是阐明METTL3在不同肿瘤中双向作用的分子基础及转化价值,技术路线遵循“领域背景铺垫→METTL3与RNA相互作用机制解析→分肿瘤类型功能总结→靶向治疗潜力探讨”的逻辑闭环。
3.1 METTL3与RNA相互作用机制梳理
实验目的:明确METTL3对不同类型RNA的调控方式及反向调控机制。
方法细节:通过整合已发表的分子机制研究,从细胞核及细胞质两个亚细胞定位层面,分析METTL3对mRNA成熟、转运、翻译及非编码RNA成熟的调控作用,同时总结非编码RNA对METTL3表达及功能的反向调控。
结果解读:细胞核内METTL3通过在pre-mRNA的剪接区域沉积m⁶A,促进pre-mRNA的成熟与剪接,并增强成熟mRNA向细胞质的转运;细胞质中METTL3通过m⁶A依赖的方式稳定mRNA并促进其翻译,同时可通过与翻译起始因子eIF3h相互作用直接增强翻译效率。此外,非编码RNA可通过靶向METTL3的3"UTR抑制其表达,或通过招募METTL3调控靶基因的m⁶A修饰。
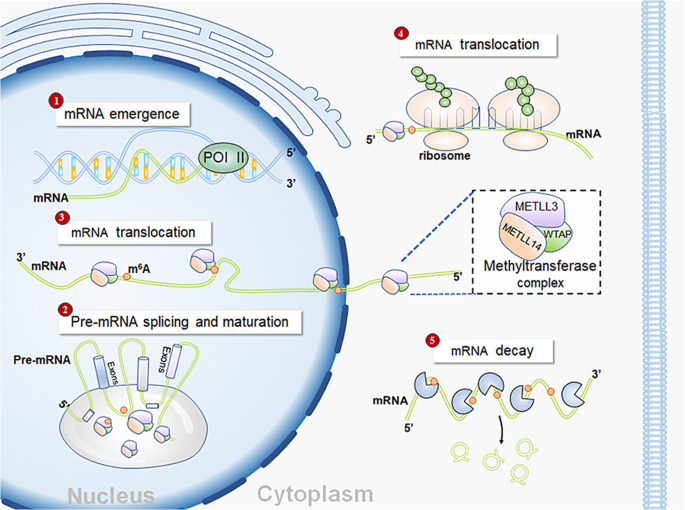
文献未提及具体实验产品,领域常规使用RNA甲基化测序试剂盒、甲基转移酶活性检测试剂、免疫共沉淀实验试剂等。
3.2 分肿瘤类型的功能与机制总结
实验目的:系统总结METTL3在不同肿瘤中的促癌/抑癌作用及具体调控靶点。
方法细节:按照胃肠道肿瘤、呼吸道肿瘤、泌尿生殖系统肿瘤、神经系统肿瘤、血液系统肿瘤等分类,整合已发表的临床及基础研究数据,分析METTL3在各肿瘤中的表达模式、预后价值及下游调控通路。
结果解读:在胃癌、肝细胞癌、结直肠癌等多数胃肠道肿瘤中,METTL3高表达与肿瘤进展及不良预后相关,通过调控MYC、SEC62等癌基因的mRNA稳定性,或激活糖酵解通路促进肿瘤生长;但在部分胃癌亚型中,METTL3通过调控BATF2发挥抑癌作用。在肺癌、鼻咽癌等呼吸道肿瘤中,METTL3主要通过调控YAP、EZH2等促进肿瘤干细胞生成及上皮间质转化。在膀胱癌、前列腺癌等泌尿生殖系统肿瘤中,METTL3通过调控miR-221/222、AFF4等通路促进肿瘤增殖与转移;但在子宫内膜癌中,METTL3低表达通过激活AKT通路促癌。在胶质母细胞瘤中,METTL3呈现双向作用,既维持肿瘤干细胞活性,又可抑制细胞增殖。
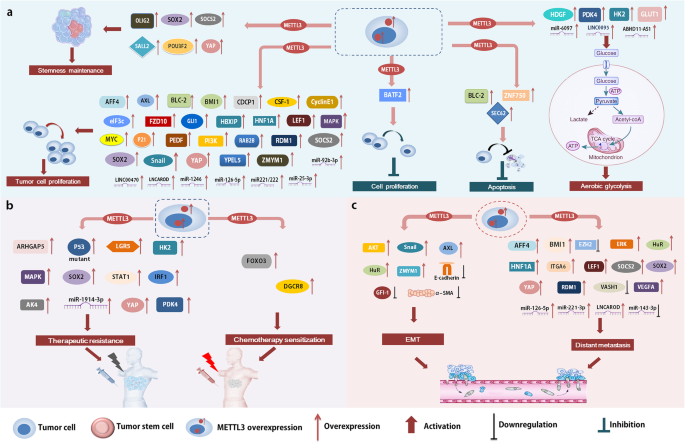
文献未提及具体实验产品,领域常规使用肿瘤细胞系、异种移植动物模型、免疫组化检测试剂盒等。
3.3 METTL3靶向治疗潜力分析
实验目的:探讨以METTL3为靶点的肿瘤治疗策略的可行性及前景。
方法细节:整合已发表的METTL3抑制剂研究及耐药逆转研究数据,分析靶向METTL3的作用机制及潜在临床价值。
结果解读:基于METTL3的促癌作用,靶向其催化结构域或竞争结合辅因子S-腺苷甲硫氨酸(SAM)的小分子抑制剂可有效降低其甲基转移酶活性,在体外实验中可逆转肿瘤细胞的耐药性;此外,抑制METTL3可增强抗PD-1免疫治疗的效果。
推测:METTL3抑制剂联合化疗或免疫治疗有望成为难治性肿瘤的新治疗方案,但需进一步的体内实验及临床研究验证。
文献未提及具体实验产品,领域常规使用小分子化合物筛选平台、药物敏感性检测试剂盒等。
4. Biomarker研究及发现成果解析
本研究将METTL3定位为具有双向预后价值的肿瘤表观遗传Biomarker,其筛选与验证逻辑为基于公共数据库(如TCGA)的生物信息学分析结合临床样本的表达验证,明确了METTL3在不同肿瘤中的表达模式与预后的相关性。
METTL3的来源为肿瘤组织样本,验证方法主要包括免疫组化(IHC)检测蛋白表达、实时荧光定量聚合酶链式反应(qRT-PCR)检测mRNA表达;在肝细胞癌中,高METTL3表达患者的总生存期显著缩短(文献未明确提供具体HR值及样本量,基于图表趋势推测);在三阴性乳腺癌中,低METTL3表达与不良预后相关(文献未明确提供具体统计学数据,基于研究结论推测)。
核心成果提炼:METTL3可作为多种肿瘤的独立预后Biomarker,其表达水平与肿瘤的增殖、侵袭、耐药密切相关;创新性在于系统阐明了METTL3在不同肿瘤中的双向预后价值,为肿瘤的个体化预后评估提供了新的表观遗传指标。目前缺乏大规模多中心临床样本验证其作为Biomarker的特异性与敏感性,需进一步研究完善。
