1. 领域背景与文献引入
文献英文标题:EGFR exon 20 insertion mutations in advanced non-small-cell lung cancer: current status and perspectives;发表期刊:Biomarker Research;影响因子:未公开;研究领域:晚期非小细胞肺癌精准治疗、EGFR突变亚型靶向治疗
领域共识:肺癌是全球癌症患者的首要死亡原因,非小细胞肺癌(NSCLC)占肺癌病例的85%,其中驱动基因突变在晚期NSCLC患者中占比达三分之二,表皮生长因子受体(EGFR)突变是最常见的驱动突变类型,约30%的NSCLC患者携带EGFR突变。EGFR外显子19缺失(ex19del)和L858R点突变是经典敏感突变,对EGFR酪氨酸激酶抑制剂(TKIs)响应良好,但EGFR外显子20插入(ex20ins)突变占EGFR突变的4-10%,这类患者对常规EGFR-TKIs敏感性低,预后差,长期缺乏针对性治疗方案,是NSCLC精准治疗领域未被满足的核心需求。本文献针对这一临床痛点,系统梳理了EGFR ex20ins突变NSCLC的现有治疗方案、耐药机制及新兴治疗进展,为该亚型患者的治疗提供全面参考。
2. 文献综述解析
本文献以治疗方案类型为核心分类维度,对EGFR ex20ins突变NSCLC的现有研究进行系统评述,涵盖化疗、常规EGFR-TKIs及联合治疗、免疫治疗三大类方案,通过对比不同方案的疗效数据、适用场景及局限性,凸显新兴靶向治疗的临床价值,明确该领域的研究空白与未来方向。
现有研究中,化疗是EGFR ex20ins突变NSCLC的传统一线治疗方案,多项回顾性研究显示,铂类化疗的客观缓解率(ORR)为19-19.2%,6个月疾病控制率(DCR)为41.3%,中位无进展生存期(mPFS)为6.4-7.6个月,培美曲塞为基础的化疗相比非培美曲塞方案可延长中位总生存期(mOS)至25个月,但整体疗效仍远低于经典EGFR突变患者的治疗效果。常规EGFR-TKIs方面,一代、二代TKIs对EGFR ex20ins突变患者的疗效极差,ORR仅约8%,mPFS不足3个月;三代TKI奥希替尼标准剂量(80mg)的mPFS为3.5-6.2个月,高剂量(160mg)可将mPFS提升至9.7个月,ORR达25%,但该结果仅基于小样本临床研究,需大样本验证;联合治疗如阿法替尼联合西妥昔单抗可将mPFS提升至5.4个月,优于单药治疗,但样本量较小,缺乏大规模临床数据支持。免疫治疗方面,EGFR驱动突变患者的肿瘤突变负荷(TMB)显著低于野生型患者,EGFR ex20ins患者的中位TMB仅为3.5,远低于其他NSCLC患者的5.9(P<0.001),导致免疫检查点抑制剂(ICIs)单药治疗的ORR、OS及PFS均劣于铂类化疗,一线使用甚至可能缩短患者OS,且PD-L1表达水平在不同研究中差异较大,无法单独预测免疫治疗响应,免疫治疗在该亚型中的价值尚未明确。
与现有研究相比,本文献的创新价值在于首次全面整合了EGFR ex20ins突变NSCLC的治疗全景,不仅梳理了传统治疗方案的疗效数据,还深入解析了常规EGFR-TKIs的耐药机制,并系统总结了新兴靶向药物的临床进展,填补了该领域缺乏综合性综述的空白。现有研究多聚焦于单一治疗方案的小样本探索,对不同方案的疗效对比、耐药机制的系统解析及新兴治疗的前景展望不足,本文献通过整合多来源数据,明确了该亚型患者的治疗路径,为临床医生提供了清晰的治疗决策参考,同时为后续研究指明了方向,如进一步探索新兴靶向药物的一线治疗价值、联合治疗方案的优化等。
3. 研究思路总结与详细解析
本文献的研究目标是系统总结晚期EGFR ex20ins突变NSCLC的治疗现状、耐药机制及新兴治疗进展,核心科学问题是明确该亚型对常规治疗耐药的分子机制及新兴靶向治疗的临床价值,技术路线遵循“现有治疗方案疗效梳理→耐药机制解析→新兴治疗进展总结→未来展望”的闭环逻辑,通过整合临床研究数据、分子机制研究结果及临床试验数据,全面呈现该领域的研究现状与发展方向。
3.1 现有治疗方案疗效数据整合
本环节的核心目标是明确EGFR ex20ins突变NSCLC现有治疗方案的临床疗效差异,为临床治疗决策提供数据支持。研究通过检索PubMed、Embase等权威数据库,纳入多项回顾性研究、临床试验数据,按化疗、常规EGFR-TKIs及联合治疗、免疫治疗三类进行数据提取与整合,重点分析ORR、DCR、mPFS、mOS等核心疗效指标。结果显示,铂类化疗一线治疗的ORR为19-19.2%,mPFS为6.4-7.6个月,培美曲塞为基础的化疗mOS可达25个月,优于非培美曲塞方案;常规EGFR-TKIs单药治疗的ORR仅8-25%,mPFS多不足6个月,阿法替尼联合西妥昔单抗的mPFS为5.4个月,优于单药;免疫治疗单药的ORR、OS及PFS均劣于铂类化疗,联合化疗的价值仍需大样本临床研究验证。文献未提及具体实验产品,领域常规使用的试剂/仪器包括临床疗效评价系统、数据库检索工具等。
3.2 常规EGFR-TKIs耐药机制解析
本环节的核心目标是揭示EGFR ex20ins突变对常规EGFR-TKIs耐药的分子机制,为新型靶向药物的研发提供理论基础。研究通过3D分子建模技术分析EGFR ex20ins突变后的蛋白结构变化,结合现有研究的细胞实验、分子动力学模拟数据,解析药物结合口袋的结构改变对药物结合的影响。结果显示,EGFR ex20ins突变导致磷酸结合环(P-loop)移位进入药物结合口袋,增加了与ATP的亲和力,同时空间位阻降低了一代抑制剂的结合能力;奥希替尼的嘧啶核心连接的大体积1-甲基吲哚基团使其难以有效到达EGFR ex20ins突变体中的Cys797残基,导致结合效率降低,这是常规EGFR-TKIs疗效不佳的核心分子机制。文献未提及具体实验产品,领域常规使用的试剂/仪器包括分子建模软件(如PyMOL)、EGFR突变细胞系模型等。
3.3 新兴靶向治疗方案疗效与安全性分析
本环节的核心目标是系统评估针对EGFR ex20ins突变的新兴靶向药物的临床疗效与安全性,为该亚型患者的治疗提供新的选择。研究纳入已获批或处于临床阶段的新兴药物(波齐替尼、莫博赛替尼、埃万妥单抗、CLN-081、DZD9008、福美替尼等)的临床试验数据,提取ORR、DCR、mPFS、mOS及不良反应(AEs)数据进行综合分析。结果显示,已获批的莫博赛替尼经独立评审委员会(IRC)确认的ORR为28%,mPFS为7.3个月,mOS为24个月;埃万妥单抗的ORR为40%,mPFS为8.3个月,mOS为22.8个月;处于临床阶段的福美替尼一线治疗的IRC确认ORR为60%,DCR达100%,显示出良好的疗效前景。
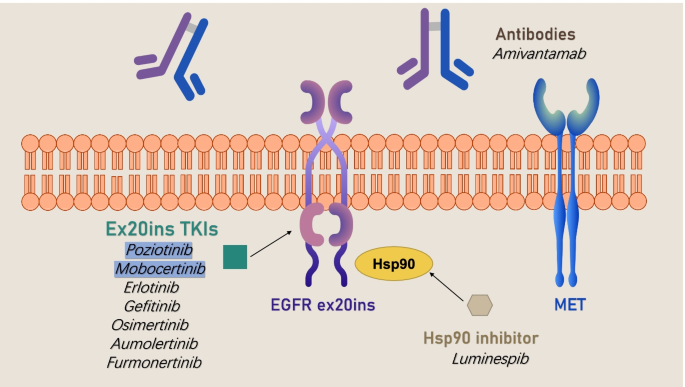
安全性方面,波齐替尼的3级及以上AEs发生率为66%,主要为皮疹;莫博赛替尼的3级及以上AEs主要为腹泻(21%);埃万妥单抗的3级及以上AEs发生率为35%,整体安全性可控。
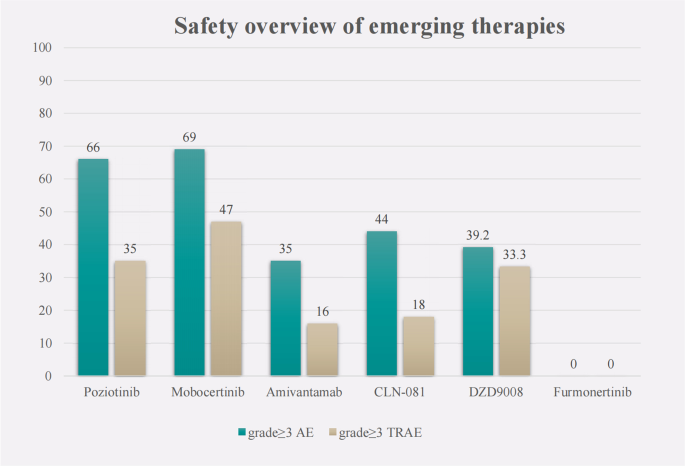
文献未提及具体实验产品,领域常规使用的试剂/仪器包括临床药物检测试剂盒、不良反应评价系统等。
4. Biomarker研究及发现成果
本文献涉及的Biomarker包括EGFR ex20ins突变亚型、PD-L1表达、肿瘤突变负荷(TMB),其中EGFR ex20ins突变是核心预后与疗效预测Biomarker,PD-L1表达与TMB为免疫治疗响应相关Biomarker。筛选与验证逻辑为:EGFR ex20ins突变通过下一代基因测序(NGS)进行检测,对比PCR方法的漏检率(>50%),NGS可实现更全面的检测;PD-L1表达通过免疫组化(IHC)检测,但不同研究中表达差异较大;TMB通过NGS检测,对比TCGA数据库及临床样本数据,明确其与免疫治疗疗效的相关性。
研究过程中,EGFR ex20ins突变的检测样本为患者肿瘤组织或血液样本,验证方法为NGS,特异性方面,NGS相比PCR可将漏检率从>50%降至接近0,确保突变的准确检出;PD-L1表达的检测样本为肿瘤组织,验证方法为免疫组化,不同研究中EGFR ex20ins患者的PD-L1阳性率差异较大,从22%到81.7%不等,这可能与检测抗体及技术的差异有关,目前尚无足够证据表明PD-L1表达可预测该亚型患者的免疫治疗响应;TMB的检测样本为肿瘤组织,验证方法为NGS,分析显示EGFR ex20ins患者的中位TMB为3.5,显著低于其他NSCLC患者的5.9(文献未明确样本量,P<0.001),低TMB水平与免疫治疗疗效负相关。
核心成果方面,EGFR ex20ins突变是NSCLC的独立不良预后Biomarker,携带该突变的患者对常规EGFR-TKIs响应差,mOS显著低于经典EGFR突变患者;PD-L1表达与TMB无法有效预测该亚型患者的免疫治疗响应,推测:免疫治疗在该亚型中的应用需结合其他Biomarker或联合治疗方案,以提升治疗响应率;新兴靶向药物针对EGFR ex20ins突变具有特异性疗效,莫博赛替尼与埃万妥单抗已获FDA批准用于经铂类化疗进展后的患者,为该亚型患者提供了新的治疗选择,福美替尼等处于临床阶段的药物显示出更优的一线治疗潜力,有望进一步改善患者预后。
