1. 领域背景与文献引入
文献英文标题:Development of a novel BRCAness score that predicts response to PARP inhibitors;发表期刊:Biomarker Research;影响因子:未公开;研究领域:乳腺癌精准诊疗与生物标志物研究
领域共识:BRCAness是指模拟BRCA1/2胚系突变表型的同源重组缺陷(HRD)状态,由同源重组修复(HRR)基因体细胞突变、表观遗传调控异常等多种因素导致,可使肿瘤细胞对DNA损伤类化疗药物及聚腺苷二磷酸核糖聚合酶(PARP)抑制剂产生合成致死敏感性。2017年OlympiAD研究证实PARP抑制剂奥拉帕利可显著改善BRCA胚系突变转移性乳腺癌患者的预后,此后PARP抑制剂逐渐成为BRCA突变乳腺癌的标准治疗方案,但目前临床仅将BRCA胚系突变作为PARP抑制剂的适应症,而约50%的高BRCAness患者为BRCA野生型,现有量化BRCAness的方法如基因组HRD评分仅针对特定基因变异,未考虑肿瘤微环境的贡献,缺乏基于转录组的泛化性评分体系。因此,建立一种可覆盖BRCA野生型患者、基于转录组的BRCAness评分体系,对扩大PARP抑制剂的临床受益人群具有重要学术价值与临床意义。
2. 文献综述解析
作者围绕BRCAness的定义、形成机制、现有量化方法及临床应用局限展开综述,按“基础机制-量化技术-临床转化”的逻辑分类梳理领域研究。
现有研究支持BRCAness由HRR基因功能缺失、表观调控异常等多因素共同驱动,可有效预测乳腺癌患者对化疗及PARP抑制剂的响应;现有技术方法中,基因组HRD评分可通过检测染色体不稳定性反映同源重组缺陷,但其优势仅局限于BRCA突变或特定HRR基因变异的患者,局限性在于未考虑肿瘤微环境中非肿瘤细胞对BRCAness的贡献,且临床应用严格依赖BRCA胚系突变检测,无法覆盖BRCA野生型的高BRCAness患者。通过对比现有研究的不足,本文的创新价值在于首次基于BRCA1突变相关的34个基因表达谱,采用基因集变异分析(GSVA)算法构建跨大样本队列验证的BRCAness评分体系,纳入肿瘤微环境细胞的贡献,可独立于BRCA突变状态预测PARP抑制剂的响应,为BRCA野生型高BRCAness患者的精准治疗提供依据。
3. 研究思路总结与详细解析
本研究以“构建基于转录组的BRCAness评分体系→验证其生物学特征→明确其与免疫微环境的关联→验证药物响应预测价值”为闭环技术路线,核心科学问题是BRCAness评分能否独立于BRCA突变状态预测PARP抑制剂的临床响应,研究目标是建立可用于临床转化的BRCAness量化工具,扩大PARP抑制剂的受益人群。
3.1 研究队列数据获取与预处理
本环节的核心目标是获取具有代表性的大样本乳腺癌转录组及临床数据,为评分体系的构建与多维度验证提供基础。研究人员从Molecular Taxonomy of Breast Cancer International Consortium(METABRIC)、GSE96058(SCAN-B队列)、The Cancer Genome Atlas(TCGA)三个公共数据库分别获取1903例、3273例、1069例乳腺癌患者的基因表达数据(RSEM格式转换为转录本每百万读数(TPM))及对应的临床信息,同时纳入Cancer Cell Line Encyclopedia(CCLE)的乳腺癌细胞系数据及GSE75688的单细胞转录组数据用于补充验证。结果显示,三个队列覆盖了不同种族、分子亚型的乳腺癌样本,为评分体系的泛化性验证提供了充足的样本量支持。文献未提及具体实验产品,领域常规使用R语言、生物信息学数据库分析工具等。
3.2 BRCAness评分体系构建与性能验证
本环节旨在筛选与BRCA1突变高度相关的基因,构建可靠的BRCAness评分体系并验证其性能。研究人员通过受试者工作特征曲线下面积(ROC-AUC)分析,在TCGA和METABRIC队列中筛选出34个与BRCA1突变显著关联的基因(AUC>0.65),采用基因集变异分析(GSVA)算法基于这些基因的表达水平构建BRCAness评分。随后通过Spearman秩相关分析验证评分与DNA修复评分、同源重组缺陷(HRD)评分的相关性,结果显示BRCAness评分与DNA修复评分在TCGA队列的相关系数为0.593(n=1069,P<0.001),在GSE96058队列为0.559(n=3273,P<0.001),与HRD评分在TCGA队列的相关系数为0.633(n=1069,P<0.001);ROC-AUC分析显示,该评分对BRCA1突变的区分能力在TCGA队列AUC为0.709,在METABRIC队列为0.735,显著优于DNA修复评分、BRCA1/2基因表达等其他BRCAness相关因子。
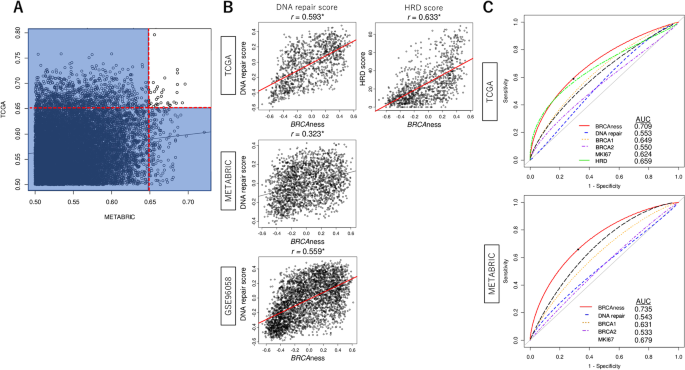
文献未提及具体实验产品,领域常规使用GSVA算法、ROC分析工具等。
3.3 BRCAness评分与乳腺癌生物学特征的关联分析
本环节旨在明确BRCAness评分与乳腺癌核心生物学特征的关联,验证其对BRCAness表型的反映能力。研究人员对比高低BRCAness组(以三分位数为cutoff)的突变负荷、DNA修复活性及细胞增殖相关指标,结果显示高BRCAness组的突变计数在三个队列均显著更高(n=6245,P<0.001),同时与高HRD评分、肿瘤内异质性显著相关;DNA修复评分和MKi67基因表达在高BRCAness组显著升高,且该关联独立于BRCA1突变状态。基因集富集分析(GSEA)结果显示,高BRCAness组不仅显著富集DNA修复相关基因集,还一致富集所有5个细胞增殖相关的Hallmark基因集(包括有丝分裂纺锤体、MYC靶点等),提示高BRCAness与乳腺癌的侵袭性表型密切相关。此外,三阴性乳腺癌(TNBC)的BRCAness评分在三个队列中均为最高,且与高Nottingham病理分级显著相关(n=6245,P<0.001)。
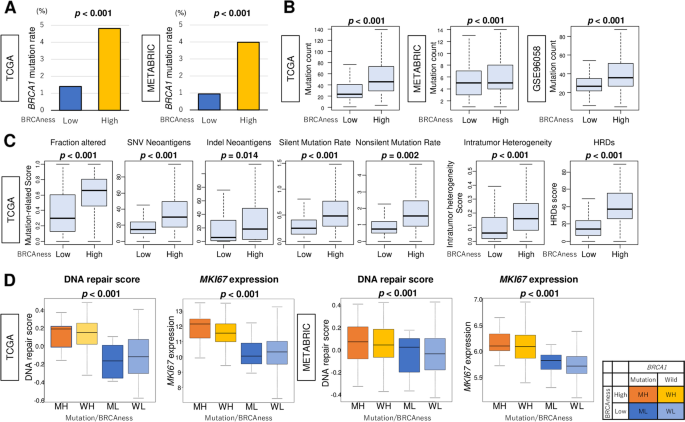
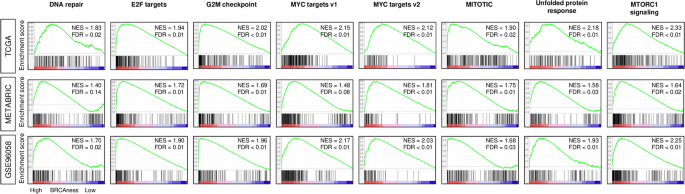
文献未提及具体实验产品,领域常规使用GSEA、统计分析软件等。
3.4 BRCAness评分与肿瘤免疫微环境的关联分析
本环节旨在探索BRCAness评分对肿瘤免疫微环境的调控作用,明确非肿瘤细胞对BRCAness评分的贡献。研究人员通过xCell算法估算肿瘤浸润免疫细胞的比例,结果显示高BRCAness组的M1巨噬细胞、辅助性T细胞1(Th1)、CD4+记忆T细胞等抗肿瘤免疫细胞浸润水平显著升高(TCGA队列,P<0.001),而M2巨噬细胞等促肿瘤免疫细胞的浸润无显著差异;同时高BRCAness组的细胞溶解活性评分、免疫检查点指数(ICI)均显著升高(三个队列,P<0.001)。通过单细胞转录组数据分析发现,除肿瘤细胞外,肿瘤微环境中的基质细胞、T细胞、B细胞及髓系细胞也会贡献BRCAness评分,提示BRCAness是肿瘤细胞与微环境细胞共同作用的结果。
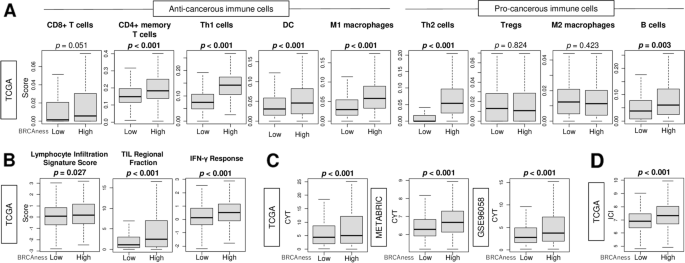
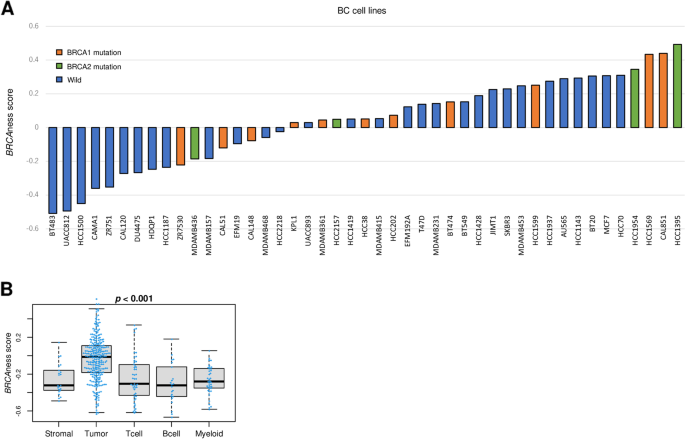
文献未提及具体实验产品,领域常规使用xCell算法、免疫相关评分计算工具等。
3.5 BRCAness评分与药物响应的验证
本环节的核心目标是验证BRCAness评分对化疗及PARP抑制剂响应的预测价值,明确其临床转化潜力。研究人员在接受蒽环类联合紫杉类新辅助化疗的GSE25066队列中分析发现,BRCAness评分对TNBC和雌激素受体阳性/人表皮生长因子受体2阴性(ER+/HER2-)乳腺癌的病理完全缓解(pCR)预测AUC分别为0.624(n=508,P<0.05)和0.714(n=508,P<0.05);在接受度伐利尤单抗联合奥拉帕利治疗的GSE173839队列中,评分对pCR的预测AUC分别提升至0.815(P<0.001)和0.715(P<0.001)。此外,CCLE细胞系数据显示,BRCAness评分与奥拉帕利的敏感性呈正相关,TNBC细胞系的相关系数为0.489,ER+/HER2-细胞系为0.771,提示该评分可有效预测不同亚型乳腺癌对PARP抑制剂的响应。
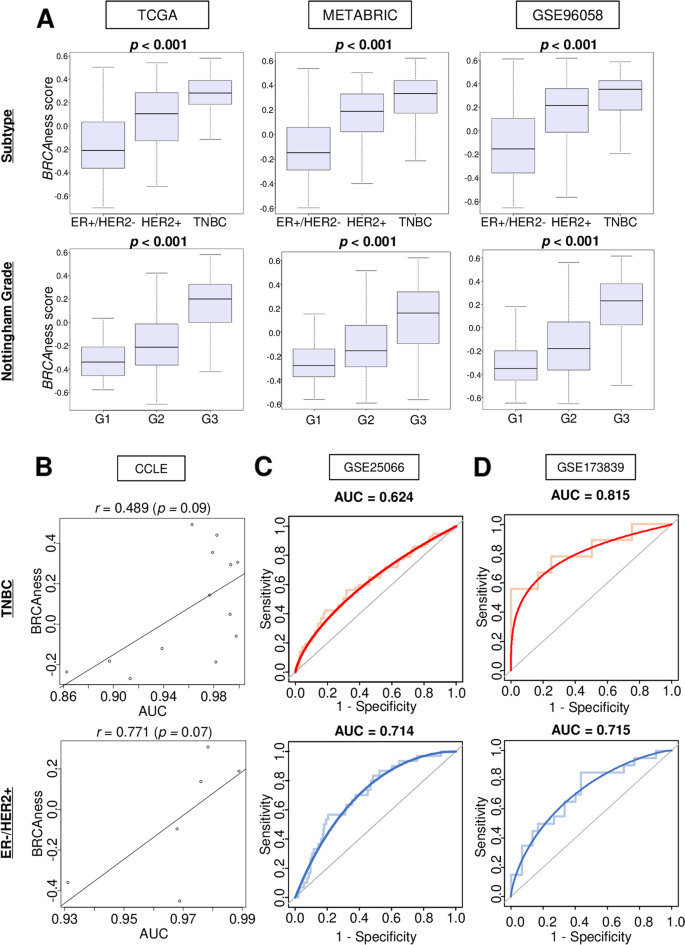
文献未提及具体实验产品,领域常规使用药物敏感性数据库、ROC分析工具等。
4. Biomarker研究及发现成果
本研究的核心生物标志物为基于34个BRCA1突变相关基因构建的新型BRCAness评分,属于转录组水平的复合生物标志物,其筛选与验证逻辑覆盖了“队列筛选→算法构建→多维度验证→临床转化”的完整链条,为乳腺癌PARP抑制剂的精准应用提供了可靠工具。
Biomarker定位方面,该BRCAness评分是首个纳入肿瘤微环境细胞贡献的转录组复合生物标志物,筛选逻辑为通过TCGA和METABRIC队列中BRCA1突变与野生型的基因表达差异,筛选出34个AUC>0.65的关联基因,经GSVA算法构建评分后,通过三个独立大样本队列验证其与DNA修复、突变负荷、免疫微环境的关联,同时利用单细胞转录组数据明确非肿瘤细胞的贡献。研究过程详述:该生物标志物的来源为乳腺癌患者的bulk转录组数据及单细胞转录组数据,验证方法包括多队列相关性分析、GSEA富集分析、ROC-AUC验证及药物敏感性关联分析;特异性与敏感性方面,对BRCA1突变的区分AUC在TCGA队列达0.709,METABRIC队列达0.735,预测奥拉帕利联合免疫治疗pCR的AUC在TNBC亚型达0.815,具有良好的特异性与敏感性。核心成果提炼:该BRCAness评分可独立于BRCA突变状态,全面反映乳腺癌的DNA修复活性、细胞增殖能力及免疫微环境状态,作为PARP抑制剂响应的预测生物标志物,不仅可用于BRCA突变患者,还能识别BRCA野生型的高BRCAness患者,为扩大PARP抑制剂的临床受益人群提供了关键依据;统计学结果显示,所有关联分析均具有P<0.001或P<0.05的显著性,样本量覆盖三个队列共6245例患者,验证了该生物标志物的可靠性与泛化性。
