1. 领域背景与文献引入
文献英文标题:Advances and challenges in CAR-T cell therapy for head and neck squamous cell carcinoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:头颈部肿瘤免疫治疗
领域共识:头颈部鳞状细胞癌(HNSCC)是全球第六大常见恶性肿瘤,每年新增约88万例患者,死亡44万例,其发病与烟草、酒精暴露、人乳头瘤病毒(HPV)感染等因素密切相关。传统治疗手段包括手术、放疗、化疗及免疫检查点抑制剂,但患者五年生存率仅为50%~66%,仅约20%的患者能从免疫检查点抑制剂治疗中获益,主要瓶颈在于肿瘤异质性强、免疫逃逸机制复杂、治疗耐药性高。CAR-T细胞治疗在血液系统恶性肿瘤中取得突破性成功,通过基因工程改造T细胞使其特异性识别肿瘤抗原,实现精准杀伤,但在HNSCC等实体瘤应用中仍面临肿瘤微环境(TME)免疫抑制、抗原异质性、浸润不足等诸多挑战。本文作为系统性综述,旨在全面梳理CAR-T细胞治疗HNSCC的研究现状、潜在靶点、核心挑战及新兴优化策略,为该领域的后续研究及临床转化提供参考依据。
2. 文献综述解析
本文以“CAR-T细胞治疗HNSCC的进展与挑战”为核心主题,采用“疾病基础铺垫-CAR-T技术原理-靶点研究现状-挑战问题梳理-优化策略探讨”的逻辑框架,系统整合了近年来HNSCC病理生理、CAR-T技术发展及实体瘤应用的相关研究成果,重点围绕CAR-T在HNSCC中的治疗瓶颈及解决方案展开评述。
现有研究已证实CAR-T细胞治疗在血液肿瘤中的显著疗效,其主要组织相容性复合体(MHC)非依赖的抗原识别机制可有效克服肿瘤免疫逃逸,但在HNSCC等实体瘤中,由于TME存在大量免疫抑制细胞(如调节性T细胞、髓源性抑制细胞、M2型肿瘤相关巨噬细胞)、酸性缺氧环境及致密基质结构,导致CAR-T细胞浸润不足、存活时间短、杀伤活性受抑;同时,HNSCC抗原异质性高,单一靶点CAR-T易出现肿瘤逃逸,且部分靶点在正常组织低表达,存在脱靶毒性风险。目前针对HNSCC的CAR-T研究主要聚焦于筛选特异性肿瘤相关抗原(TAAs),如ErbB家族、CD70、MUC1等,并通过CAR结构优化、联合治疗等方式提升疗效,但多数研究仍处于预临床阶段,临床转化数据有限。
与现有单一靶点或单一策略的研究不同,本文全面覆盖了HNSCC中CAR-T治疗的多类潜在靶点,详细解析了各靶点的表达特征、预临床疗效及局限性;同时系统总结了克服CAR-T治疗瓶颈的新兴策略,包括多靶点CAR设计、CRISPR基因编辑、溶瘤病毒联合、瘤内递送优化等,尤其重点介绍了T4免疫疗法等已进入临床研究的创新方案,为HNSCC的CAR-T治疗提供了全景式的参考框架,填补了该领域系统性综述的空白。
3. 研究思路总结与详细解析
本文为综述性研究,整体研究目标是全面阐述CAR-T细胞治疗HNSCC的当前格局、核心挑战及未来发展方向;核心科学问题是如何突破CAR-T细胞在HNSCC等实体瘤中的治疗瓶颈,提升其临床疗效与安全性;技术路线遵循“疾病背景铺垫-技术原理介绍-应用现状分析-挑战问题梳理-优化策略探讨-未来方向展望”的逻辑闭环,通过整合大量基础研究与临床数据,为该领域的研究提供系统性指导。
3.1 HNSCC病理生理与肿瘤微环境特征解析
实验目的:明确HNSCC的发病机制、分子特征及肿瘤微环境(TME)对免疫治疗的影响,为CAR-T治疗的靶点选择及策略优化提供理论基础。
方法细节:通过综述已发表的HNSCC病理生理、分子生物学及免疫微环境相关研究,系统梳理HNSCC的致病因素、基因突变、信号通路异常及TME组成特征。
结果解读:HNSCC起源于口腔、咽喉部黏膜上皮,致病因素包括烟草酒精暴露、HPV/EB病毒感染等;常见基因突变包括TP53、NOTCH1、PIK3CA、EGFR等,Wnt/β-catenin、NF-κB、PI3K/AKT/mTOR等信号通路异常激活,驱动肿瘤增殖、侵袭及转移;TME富含免疫抑制细胞、酸性缺氧环境及致密基质结构,共同导致免疫逃逸,抑制免疫治疗效果。
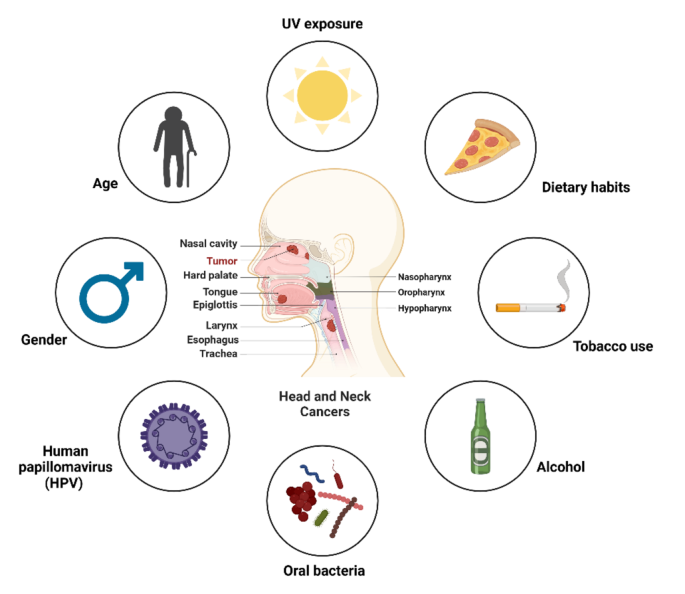
产品关联:文献未提及具体实验产品,领域常规使用免疫组化(IHC)、流式细胞术、qRT-PCR等试剂检测肿瘤组织的分子表达及TME细胞组成。
3.2 CAR-T细胞基础与作用机制解析
实验目的:介绍CAR-T细胞的发展历程、结构组成及杀伤肿瘤细胞的核心机制,为理解其在HNSCC中的应用提供技术基础。
方法细节:综述CAR-T细胞的研发历史,从第一代到第五代CAR的结构演变,以及CAR-T细胞识别、杀伤肿瘤细胞的分子机制。
结果解读:CAR-T细胞由以色列科学家于1989-1993年研发,经历五代发展:第一代仅含CD3ζ信号域,激活能力有限;第二代加入CD28或4-1BB共刺激域,提升T细胞增殖与存活;第三代加入多个共刺激域,理论活性更强但临床未显示优势;第四代(TRUCKs)可分泌细胞因子(如IL-12),调节TME;第五代整合细胞因子受体域,增强免疫信号。CAR-T细胞通过单链可变片段(scFv)特异性识别肿瘤抗原,无需MHC呈递,激活后通过穿孔素-颗粒酶途径、Fas-FasL途径诱导肿瘤细胞凋亡,同时分泌TNF-α、IFN-γ等细胞因子招募免疫细胞,增强抗肿瘤免疫反应。
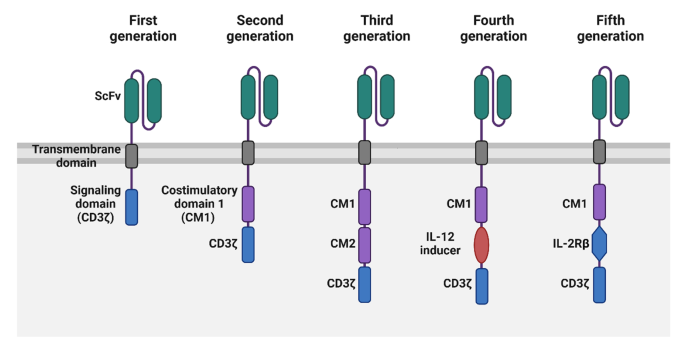
产品关联:文献未提及具体实验产品,领域常规使用慢病毒/逆转录病毒载体、CRISPR-Cas9基因编辑工具、细胞培养试剂等构建与扩增CAR-T细胞。
3.3 HNSCC中CAR-T的潜在靶点研究解析
实验目的:总结HNSCC中已报道的CAR-T潜在靶点,分析各靶点的表达特征、预临床疗效及应用前景。
方法细节:综述针对ErbB家族、CD70、MUC1、CD98hc等靶点的CAR-T细胞治疗HNSCC的预临床及临床研究数据。
结果解读:ErbB家族(EGFR、HER2等)在90%以上HNSCC中过表达,EGFR靶向CAR-T细胞在FaDu下咽癌细胞系中可实现52.66%的肿瘤细胞裂解率,T4免疫疗法(靶向ErbB二聚体)在临床研究中对12例患者实现69%的疾病控制率,且耐受性良好;CD70在19%的HNSCC活检样本中表达,靶向CAR-T细胞可有效清除CD70阳性HNSCC细胞;MUC1在HNSCC中过表达,与不良预后相关,第四代CAR-MUC1-IL22细胞可分泌IL-22,增强T细胞增殖与肿瘤杀伤活性;CD98hc在放射抵抗HNSCC细胞中高表达,CD98hc靶向UniCAR-T细胞在3D肿瘤球模型中显示出良好的肿瘤杀伤效果。
产品关联:文献未提及具体实验产品,领域常规使用重组抗体、CAR构建试剂盒、细胞毒性检测试剂等开展相关研究。
3.4 CAR-T治疗HNSCC的挑战分析
实验目的:系统分析CAR-T细胞治疗HNSCC面临的核心挑战,为后续优化策略提供方向。
方法细节:综述CAR-T细胞在HNSCC中应用的相关研究,从TME抑制、肿瘤浸润、抗原异质性、治疗毒性等方面梳理瓶颈问题。
结果解读:TME免疫抑制是核心挑战之一,酸性缺氧环境、免疫抑制细胞及细胞因子抑制CAR-T细胞的存活与活性;实体瘤致密基质结构导致CAR-T细胞浸润困难,静脉注射后难以有效到达肿瘤部位;HNSCC抗原异质性高,单一靶点CAR-T细胞易出现肿瘤细胞抗原丢失导致的治疗逃逸;治疗毒性包括“on-target, off-tumor”脱靶毒性(靶点在正常组织低表达)及系统性毒性(如细胞因子释放综合征CRS、神经毒性ICANS),CRS主要表现为发热、低血压等,ICANS可导致意识障碍、癫痫等严重不良反应。
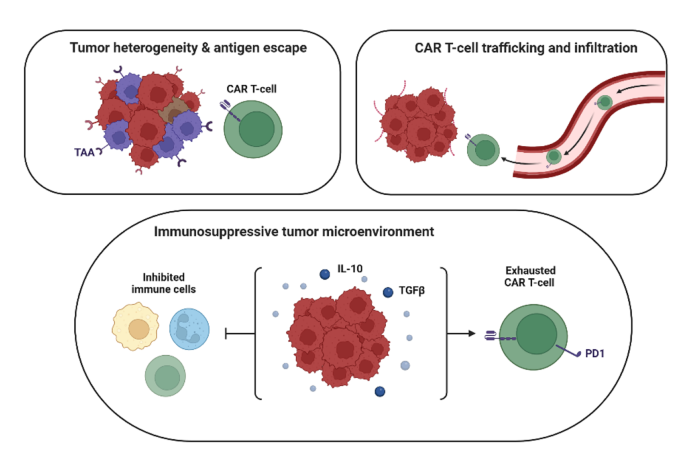
产品关联:文献未提及具体实验产品,领域常规使用细胞因子检测试剂盒、毒性评估量表等开展相关研究。
3.5 增强CAR-T疗效的策略研究解析
实验目的:探讨提升CAR-T细胞治疗HNSCC疗效与安全性的优化策略,推动临床转化应用。
方法细节:综述多靶点CAR设计、CRISPR基因编辑、联合治疗、递送方式优化等新兴策略的研究进展。
结果解读:多靶点CAR(如双靶点、串联CAR)可同时识别多个肿瘤抗原,克服抗原异质性导致的肿瘤逃逸;CRISPR基因编辑可敲除CAR-T细胞中的PD-1、CTLA-4等抑制性基因,增强T细胞活性,或编辑CAR结构提升特异性;联合免疫检查点抑制剂(如纳武利尤单抗)、溶瘤病毒、放疗等可改善TME免疫抑制状态,增强CAR-T细胞浸润与活性;瘤内注射等递送方式优化可提高CAR-T细胞在肿瘤部位的浓度,降低系统性毒性,T4免疫疗法采用瘤内注射实现了良好的临床疗效与安全性。
产品关联:文献未提及具体实验产品,领域常规使用CRISPR-Cas9系统、免疫检查点抑制剂、溶瘤病毒载体等开展相关研究。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker主要为HNSCC中CAR-T细胞治疗的潜在靶点抗原,包括ErbB家族(EGFR、HER2)、CD70、MUC1、CD98hc,这些Biomarker的筛选基于HNSCC中的特异性高表达特征及与肿瘤进展的相关性,经过预临床验证部分已进入临床研究阶段,为HNSCC的精准CAR-T治疗提供了关键靶点。
Biomarker定位:本文中Biomarker属于肿瘤相关抗原(TAAs)类型,筛选逻辑为:首先基于HNSCC的转录组、蛋白质组数据筛选出在肿瘤组织中特异性高表达的分子,然后通过细胞系、动物模型验证其作为CAR-T靶点的有效性,部分靶点进一步进入临床研究验证安全性与疗效。具体包括:ErbB家族(尤其是EGFR)在90%以上HNSCC中过表达,与肿瘤增殖、侵袭相关;CD70在19% HNSCC中表达,参与免疫逃逸;MUC1在HNSCC中过表达,与不良预后相关;CD98hc在放射抵抗HNSCC中高表达,参与肿瘤细胞存活与耐药。
研究过程详述:这些Biomarker的来源主要为HNSCC肿瘤组织样本及细胞系,验证方法包括:免疫组化(IHC)检测肿瘤组织中抗原表达水平,流式细胞术分析细胞表面抗原表达,CAR-T细胞体外杀伤实验验证靶点有效性,动物异种移植模型评估体内抗肿瘤活性,临床研究验证安全性与疗效。具体数据:EGFR在90%以上HNSCC中过表达(文献未明确样本量);CD70在19%的HNSCC活检样本中表达(n=未明确);MUC1在HNSCC肿瘤组织中的表达显著高于相邻正常组织(n=未明确);CD98hc在放射抵抗HNSCC细胞中的表达水平显著高于敏感细胞(n=未明确)。T4免疫疗法(靶向ErbB二聚体)在临床研究中对12例HNSCC患者实现69%的疾病控制率,无剂量限制性毒性(n=12,P值未提及)。
核心成果提炼:这些Biomarker作为CAR-T靶点,在预临床研究中均显示出一定的抗肿瘤活性,其中T4免疫疗法已进入临床研究并取得初步疗效,为HNSCC的CAR-T治疗提供了可行的临床方案;创新性在于首次系统总结了HNSCC中CAR-T治疗的多类潜在靶点,明确了各靶点的特征与应用前景,同时结合新兴策略为Biomarker的临床应用提供了优化方向;统计学结果方面,EGFR靶向CAR-T细胞在FaDu细胞系中的肿瘤裂解率为52.66%(n=未明确,P值未提及);T4免疫疗法临床研究的疾病控制率为69%(n=12,P值未提及),其余靶点的统计学数据文献未明确提供。
