1. 领域背景与文献引入
文献英文标题:The role of pyroptosis in modulating the tumor immune microenvironment;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫微环境与细胞焦亡调控
领域共识:肿瘤免疫微环境(TIME)是肿瘤发生发展、免疫逃逸及治疗耐药的核心调控枢纽,其由肿瘤细胞、免疫细胞、基质细胞及细胞因子等多组分构成,通过复杂的细胞间相互作用形成免疫抑制网络。当前肿瘤免疫治疗(如免疫检查点抑制剂)在多数实体瘤中的响应率不足30%,尤其是以胰腺癌为代表的“冷肿瘤”,因TIME中效应T细胞浸润不足、免疫抑制细胞(肿瘤相关巨噬细胞TAM、髓源性抑制细胞MDSC、胰腺星状细胞PSC)富集,免疫治疗效果极差。细胞焦亡是近年发现的由gasdermin(GSDM)家族介导的程序性坏死,可释放促炎细胞因子重塑局部炎症微环境,但其在TIME中的调控作用呈现双向性,具体机制及临床转化潜力尚未形成系统性认知。针对这一研究空白,本综述系统梳理了细胞焦亡调控TIME的分子机制,总结了靶向焦亡的肿瘤治疗进展,为领域内后续研究及临床转化提供了核心参考框架。
2. 文献综述解析
本综述的核心评述逻辑以“TIME免疫抑制机制→细胞焦亡分子通路→焦亡调控TIME的多层面机制→靶向焦亡的治疗转化”为递进式框架,按分子组分(GSDM家族、炎症小体、促炎细胞因子)和研究阶段(基础机制→临床转化)对现有研究进行分类整合。
现有研究的关键结论包括:TIME的免疫抑制主要依赖TAM、MDSC、PSC等细胞通过分泌精氨酸酶1(Arg-1)、转化生长因子β(TGF-β)、白细胞介素10(IL-10)等分子抑制效应T细胞功能;细胞焦亡分为经典通路(NLRP3等炎症小体激活caspase-1切割GSDMD)、非经典通路(caspase-4/5/11切割GSDMD)及药物诱导的caspase-3切割GSDME通路三类;GSDM家族、炎症小体、IL-1β/IL-18在TIME中均呈现双向调控作用,既可以激活抗肿瘤免疫,也可以诱导免疫抑制。现有研究的技术方法优势在于通过生信分析泛癌数据库初步构建了焦亡基因与TIME的关联网络,结合细胞共培养、动物异种移植模型验证了核心调控机制;局限性则体现在多数研究集中于细胞及动物模型,临床样本验证数据匮乏,焦亡双向作用的具体调控节点尚未明确,靶向焦亡的临床治疗效果未达预期。
本综述的创新价值在于首次系统整合了细胞焦亡调控TIME的多层面分子机制,弥补了领域内缺乏系统性综述的空白;同时梳理了从基础研究到临床转化的全链条进展,明确了当前研究的核心瓶颈与未来方向,为靶向焦亡的肿瘤免疫治疗提供了系统性理论支撑。
3. 研究思路总结与详细解析
本综述的整体研究框架为:先明确TIME在肿瘤发生发展及治疗耐药中的核心作用,再系统阐述细胞焦亡的分子调控通路,随后分模块解析焦亡各组分对TIME的调控机制,最后总结靶向焦亡的肿瘤治疗策略及未来展望,形成“问题提出→机制解析→应用展望”的完整逻辑闭环。
3.1 肿瘤免疫微环境(TIME)免疫抑制机制解析
实验目的:以胰腺癌为典型“冷肿瘤”模型,明确TIME的组成及核心免疫抑制机制。方法细节:通过整合已发表的临床样本分析、细胞共培养及动物实验研究,系统梳理TIME中各类细胞及细胞因子的相互作用网络。结果解读:胰腺癌TIME中肿瘤细胞占比仅10%,TAM、MDSC、PSC等免疫抑制细胞富集,TAM可通过分泌Arg-1、TGF-β抑制CD8+T细胞功能,MDSC可通过活性氧(ROS)、一氧化氮(NO)通路抑制T细胞增殖,PSC可通过分泌细胞外基质形成物理屏障并招募免疫抑制细胞,共同构成免疫抑制的“冷肿瘤”微环境。
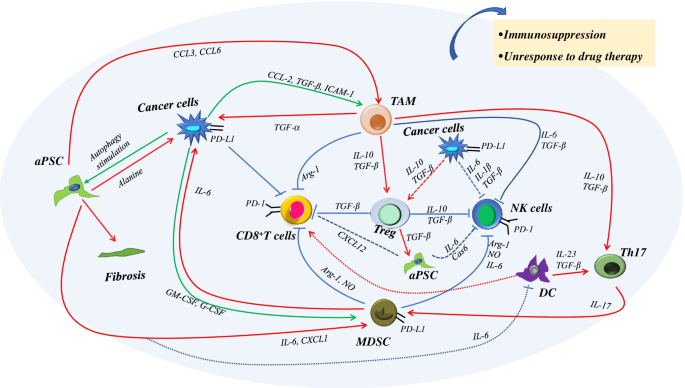
产品关联:文献未提及具体实验产品,领域常规使用免疫组化(IHC)、流式细胞术、实时荧光定量PCR(qRT-PCR)等试剂/仪器。
3.2 细胞焦亡分子通路解析
实验目的:系统总结细胞焦亡的三类核心调控通路。方法细节:整合已发表的分子机制研究,梳理不同通路的激活信号、关键蛋白酶及效应分子。结果解读:经典焦亡通路由NLRP3、AIM2等炎症小体识别病原体或损伤信号,激活caspase-1切割GSDMD,其N端结构域在细胞膜形成孔道引发细胞坏死并释放IL-1β、IL-18;非经典通路由胞内脂多糖(LPS)直接激活caspase-4/5(人)或caspase-11(小鼠)切割GSDMD;药物诱导通路由阿霉素、顺铂等化疗药物激活caspase-3切割GSDME,引发细胞焦亡。
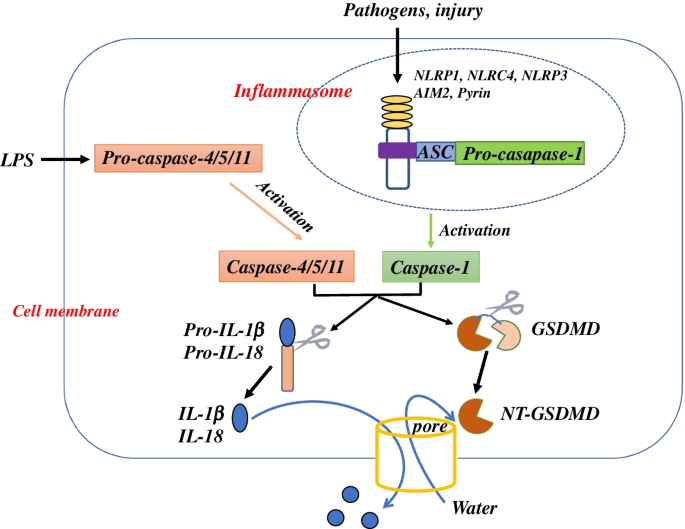
产品关联:文献未提及具体实验产品,领域常规使用蛋白质免疫印迹(WB)、免疫荧光、caspase活性检测试剂盒等。
3.3 焦亡组分对TIME的调控机制解析
实验目的:明确焦亡核心组分(GSDM家族、炎症小体、IL-1β/IL-18)对TIME的双向调控作用。方法细节:整合生信分析、细胞实验及动物实验研究结果,分模块解析各组分的调控网络。结果解读:GSDMC可通过诱导肿瘤细胞焦亡促进树突状细胞(DC)成熟及CD8+T细胞浸润,GSDMD的亚细胞定位与结直肠癌中免疫细胞浸润相关,GSDME的作用呈现组织特异性;NLRP3炎症小体可通过招募MDSC、TAM抑制免疫,而NLRC4可促进效应T细胞活化;IL-1β和IL-18既可以激活Th1细胞及NK细胞的抗肿瘤功能,也可以诱导MDSC、TAM富集形成免疫抑制微环境。
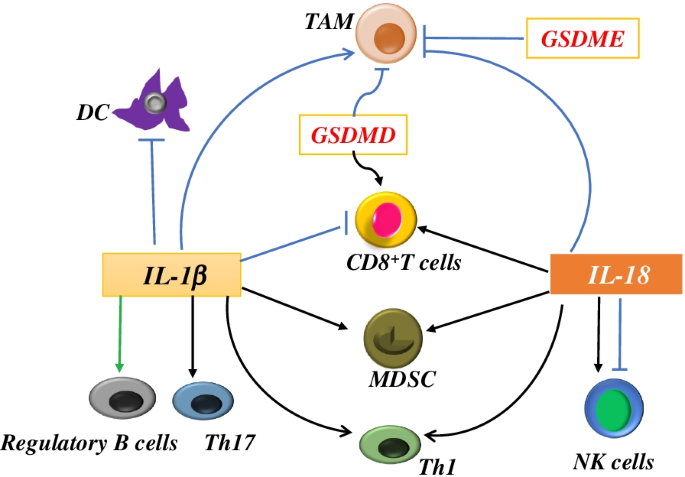
产品关联:文献未提及具体实验产品,领域常规使用CRISPR-Cas9基因编辑工具、细胞共培养体系、动物异种移植模型等。
3.4 靶向焦亡的肿瘤治疗策略解析
实验目的:总结靶向焦亡的肿瘤治疗进展及临床转化潜力。方法细节:整合临床前研究及临床试验数据,梳理不同治疗策略的作用机制及效果。结果解读:激活GSDMD/GSDME介导的焦亡可增强肿瘤免疫原性,与免疫检查点抑制剂联用可显著提升治疗效果;抑制NLRP3炎症小体可改善TIME,但部分研究显示其与PD-L1抑制剂联用存在拮抗效应;靶向IL-1β的单抗(如canakinumab)已进入临床试验,靶向IL-18的工程化改造策略(如DR-18、IL-18分泌型CAR-T)展现出良好的临床前效果。
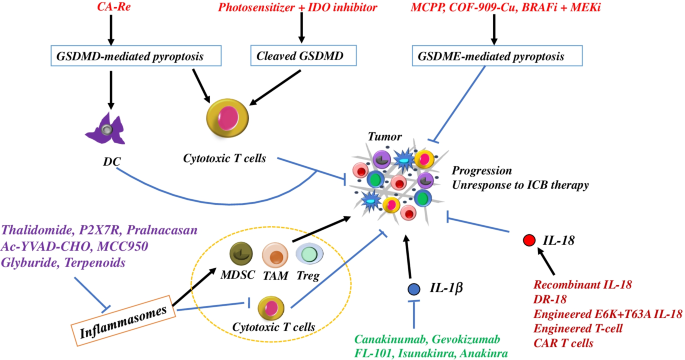
产品关联:实验所用关键产品:canakinumab(抗IL-1β单抗)、spartalizumab(抗PD-1单抗)、MCC950(NLRP3抑制剂)。
4. Biomarker研究及发现成果解析
Biomarker定位
文献中涉及的Biomarker主要为焦亡相关基因(GSDM家族基因、炎症小体基因、IL-1β/IL-18编码基因),筛选与验证逻辑为:首先通过泛癌生信分析(TCGA数据库)筛选与肿瘤浸润免疫细胞显著相关的焦亡基因,随后通过细胞系实验、动物实验验证其对TIME的调控作用,部分基因通过临床样本分析验证与患者生存及免疫治疗疗效的相关性。
研究过程详述
Biomarker来源包括TCGA等公共数据库的肿瘤转录组数据、临床肿瘤组织样本及细胞系;验证方法涵盖生信分析(生存分析、相关性分析、免疫浸润分析)、qRT-PCR、WB、免疫组化、动物异种移植模型等;特异性与敏感性数据方面,NLRP3炎症小体评分与肿瘤浸润淋巴细胞和巨噬细胞显著相关,是比肿瘤突变负荷(TMB)更强的免疫特征预测因子(文献未明确具体AUC值);结直肠癌中胞质GSDMD表达与肿瘤中心及浸润前沿的CD3+淋巴细胞富集相关(文献未明确具体统计学数据)。
核心成果提炼
焦亡相关基因可作为TIME的调控Biomarker,其表达水平与肿瘤免疫浸润状态、患者生存预后显著相关;首次系统揭示了焦亡组分在TIME中的双向调控机制,为靶向焦亡的免疫治疗提供了理论依据;部分焦亡相关Biomarker(如NLRP3)可作为免疫治疗疗效的潜在预测因子,但需大样本临床研究进一步验证(文献未明确HR值、样本量等具体统计学数据)。此外,研究明确了靶向焦亡的治疗策略需充分考虑其双向作用,为后续临床转化研究提供了关键参考。
