1. 领域背景与文献引入
文献英文标题:Identification of urinary bacterial genes as biomarkers for non-invasive diagnosis of renal lupus;发表期刊:Biomarker Research;影响因子:未公开;研究领域:自身免疫病(系统性红斑狼疮)、微生物组学、临床诊断生物标志物。
系统性红斑狼疮是一种复杂的自身免疫性疾病,以免疫过度激活和自身抗体异常产生为特征,全球年发病率约为每10万人5例,育龄女性患病率显著更高。肾脏受累(狼疮性肾炎)是SLE最严重的并发症之一,也是患者死亡的主要原因之一。当前狼疮性肾炎的诊断依赖肾活检,该方法为侵入性操作,存在出血、感染等风险,且无法实现早期、动态监测。领域共识:近年来,微生物组与自身免疫病的关联成为研究热点,肠道、口腔微生物组失调已被证实与SLE的发病及疾病进展相关,但其具体调控机制尚未完全明确。然而,泌尿微生物组(urobiome)与SLE的关联研究极为有限,仅有的1项研究样本量较小,结论局限性大,缺乏针对狼疮性肾炎的特异性泌尿微生物组生物标志物,这一空白限制了无创诊断工具的开发。
针对这一领域空白,本研究旨在通过大样本队列分析SLE患者的泌尿微生物组特征,鉴定可区分肾性与非肾性SLE的细菌基因生物标志物,为开发狼疮性肾炎的无创诊断工具提供理论基础,弥补现有诊断方法的不足。
2. 文献综述解析
作者对领域内现有研究的分类维度为微生物组的身体部位(肠道、口腔、泌尿),并结合研究结论与技术方法进行评述。现有研究的关键结论包括:肠道微生物组失调可破坏肠道屏障完整性,促进自身抗原暴露,进而诱发SLE的自身免疫反应;口腔微生物组的组成变化与SLE患者的免疫指标异常相关。技术方法方面,16S rRNA基因测序、宏基因组学等高通量技术为微生物组分析提供了有力工具,可实现微生物群落的分类与功能预测,但现有研究存在样本量较小、缺乏多中心验证、未聚焦于SLE肾脏受累亚群等局限性,尤其是泌尿微生物组的研究严重不足,仅有的研究未深入分析其与狼疮性肾炎的关联。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次基于大样本多中心队列分析SLE患者的泌尿微生物组特征,重点关注肾性与非肾性SLE的差异,鉴定了具有诊断价值的细菌基因生物标志物,并在独立队列中验证了其性能,填补了泌尿微生物组在狼疮性肾炎诊断领域的研究空白,为该领域提供了新的研究方向与潜在诊断靶点。
3. 研究思路总结与详细解析
整体框架概括:本研究的核心目标是鉴定SLE患者泌尿微生物组中可区分肾性与非肾性SLE的细菌基因生物标志物,核心科学问题是泌尿微生物组失调与SLE肾脏受累的关联机制及潜在诊断标志物的筛选,技术路线遵循“队列构建→多组学分析→差异筛选→模型构建→独立验证”的闭环逻辑,确保研究结果的可靠性与临床转化潜力。
3.1 研究队列构建与样本采集
实验目的是建立包含健康对照、非肾性SLE、肾性SLE的大样本多中心队列,为后续微生物组与代谢组学分析提供标准化的研究对象。方法细节:从欧洲PRECISESADS项目中招募585名女性受试者,其中健康对照339名、SLE患者336名(非肾性236名、肾性100名),将样本分为发现队列(309健康、206非肾性、70肾性)与独立验证队列(各30名)。采集受试者中段尿样本,排除处于经期、存在活动性感染或近期使用抗生素的个体,同时收集所有受试者的临床、血清学及人口统计学数据,所有参与者均签署知情同意书,研究方案经各中心伦理委员会批准。结果解读:统计分析显示,各研究组人群年龄匹配,疾病病程、免疫抑制剂使用、心脏受累情况在组间存在显著差异(p<0.05),但PERMANOVA分析表明这些临床因素对微生物组组成变异的解释率远低于分组因素,不会对后续微生物组分析产生显著干扰。产品关联:文献未提及具体实验产品,领域常规使用无菌尿液采集管、-80℃低温冰箱等样本存储设备。
3.2 泌尿微生物组测序与功能特征分析
实验目的是解析SLE患者泌尿微生物组的分类组成与功能通路变化,筛选与肾脏受累相关的差异特征。方法细节:提取尿液细菌沉淀中的DNA,采用融合通用引物扩增16S rRNA基因的V1-V3区,使用Illumina MiSeq平台进行双端测序;利用Mothur软件进行质量控制与嵌合体去除,基于SILVA数据库进行分类学注释,通过PICRUSt工具进行功能预测,将基因家族映射至KEGG通路。结果解读:测序共获得11059442条有效reads,平均每个样本的测序深度为18900 reads,样本覆盖率均超过99%,满足后续分析要求。Alpha多样性分析显示,非肾性与肾性SLE患者的观测操作分类单元数(p<0.0001,n=585)和Chao1指数(p<0.0001,n=585)均显著低于健康对照,提示SLE患者泌尿微生物组多样性降低;门水平分析显示,SLE患者厚壁菌门/拟杆菌门比值显著降低(p<0.05,n=585),微生物组组成失调;PERMANOVA分析表明三组人群的微生物组组成存在显著差异(p=0.0035,n=585)。
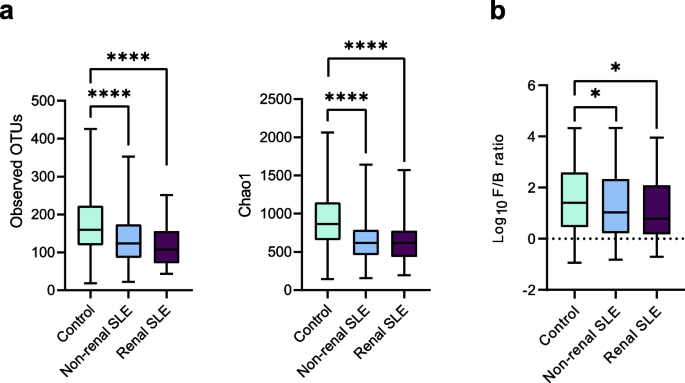
产品关联:实验所用关键产品:Illumina MiSeq测序平台、NanoDrop 2000 UV-Vis分光光度计(Thermo Fisher Scientific)、SILVA v132数据库、PICRUSt功能预测工具。
3.3 差异微生物分类群与功能基因筛选
实验目的是筛选出可区分不同研究组的微生物分类群与功能基因,为后续诊断模型构建提供候选标志物。方法细节:采用线性判别分析效应大小(LEfSe)方法筛选差异操作分类单元(OTUs),设置p<0.05、线性判别分析(LDA)值>2.0为显著阈值;通过MaAsLin2分析筛选差异KEGG通路,利用BLAST分析鉴定差异OTUs对应的具体细菌物种。结果解读:LEfSe分析显示,非肾性SLE与健康对照相比有34个差异OTUs,肾性SLE与对照相比有20个差异OTUs,非肾性与肾性SLE之间有6个差异OTUs;功能通路分析显示,非肾性SLE患者的氨基酸代谢通路(如缬氨酸、亮氨酸和异亮氨酸生物合成)显著富集,而肾性SLE患者这些通路无显著变化,提示泌尿微生物组的功能变化与SLE肾脏受累密切相关。
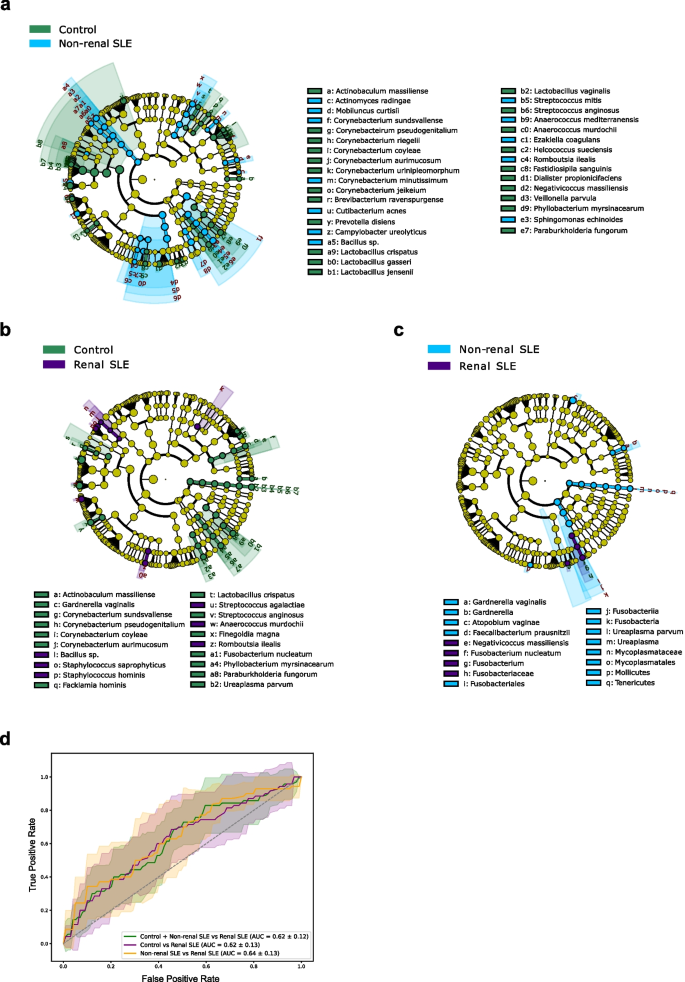
产品关联:文献未提及具体实验产品,领域常规使用Python LEfSe工具、R MaAsLin2分析包、NCBI BLAST数据库。
3.4 诊断模型构建与独立队列验证
实验目的是构建并验证基于微生物特征的诊断模型,评估其区分肾性与非肾性SLE的性能。方法细节:基于筛选出的差异OTUs与细菌基因,采用随机森林(RF)算法构建分类模型,通过十折交叉验证优化模型;在独立验证队列中,采用定量PCR(qPCR)检测候选细菌基因的丰度,验证模型的可靠性。结果解读:基于OTUs的模型区分肾性SLE与其他组的AUC为0.62,基于9个细菌基因(sco1、lldG、cysK等)的模型AUC为0.7,其中ilvA和ilvH区分肾性与非肾性SLE的AUC分别为0.7±0.07和0.67±0.07(发现队列n=276 SLE患者);独立验证队列中qPCR结果显示,这些基因在肾性与非肾性SLE患者中的丰度差异显著(p<0.05,n=30每组),证实了模型的稳定诊断性能。
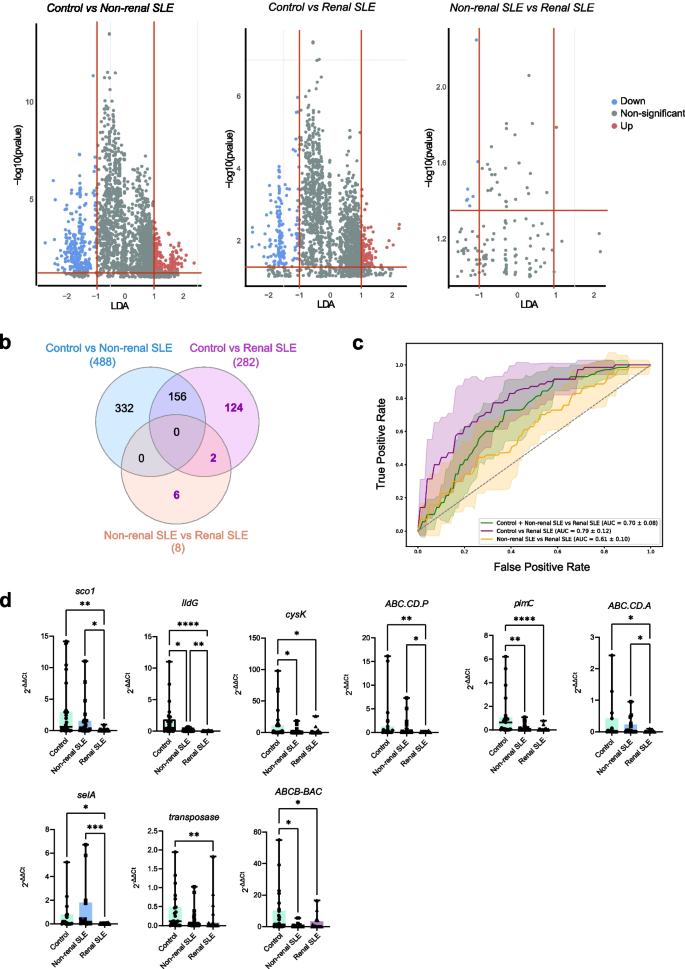
产品关联:实验所用关键产品:Illumina Nextera XT Index Kit、SYBR Green qPCR mix(Thermo Fisher Scientific)、scikit-learn RF模型分析工具。
3.5 尿液代谢组学验证分析
实验目的是验证微生物功能通路变化对应的尿液代谢物水平差异,揭示微生物组与宿主代谢的关联。方法细节:采用核磁共振(NMR)技术检测400名受试者的尿液代谢物,使用Chenomx Profiler软件进行代谢物的鉴定与定量,将代谢物浓度归一化后进行组间差异分析。结果解读:非肾性SLE患者尿液中缬氨酸(p<0.0001,n=400)、亮氨酸(p<0.001,n=400)水平显著低于健康对照,丙酮酸水平显著升高(p<0.0001,n=400),而肾性SLE患者无此变化;结合微生物功能通路分析结果,提示非肾性SLE患者泌尿微生物对支链氨基酸的降解增强,导致宿主尿液中氨基酸水平降低、丙酮酸水平升高,这一代谢变化可能与免疫调节异常相关。
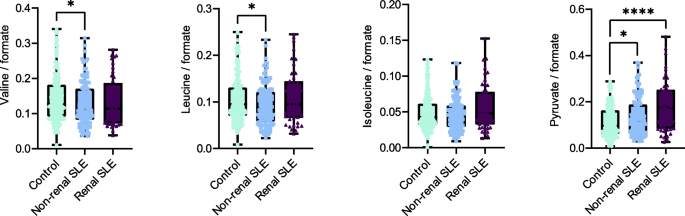
产品关联:实验所用关键产品:Bruker Avance 600 MHz NMR光谱仪(配备Prodigy TCI低温探头)、Chenomx Profiler v10.0软件。
4. Biomarker研究及发现成果解析
Biomarker定位:本研究鉴定的生物标志物为泌尿微生物组中的细菌基因,包括ilvA、ilvH、trpE、trpG等,其中ilvA和ilvH为核心标志物。筛选与验证逻辑为:首先通过发现队列的16S rRNA测序与PICRUSt功能预测筛选差异细菌基因,然后利用随机森林模型评估其诊断性能,最后在独立验证队列中通过qPCR定量检测基因丰度,验证其区分肾性与非肾性SLE的可靠性,形成“筛选→评估→验证”的完整逻辑链条。
研究过程详述:生物标志物的来源为SLE患者的中段尿液样本,验证方法采用定量PCR技术,以16S rRNA为内参,通过2^(-ΔΔCt)法计算基因相对丰度。特异性与敏感性数据显示,ilvA区分肾性与非肾性SLE的受试者工作特征曲线下面积(AUC)为0.7±0.07,ilvH的AUC为0.67±0.07(发现队列n=276 SLE患者,验证队列n=60 SLE患者),验证队列中qPCR检测显示,ilvA在肾性SLE患者中的丰度显著低于非肾性SLE患者(p<0.05,n=30每组),具有良好的特异性。
核心成果提炼:本研究鉴定的细菌基因生物标志物可有效区分肾性与非肾性SLE患者,其中ilvA的诊断性能最优,AUC达0.7,其创新性在于首次揭示了泌尿微生物组中支链氨基酸代谢通路基因与SLE肾脏受累的关联,为狼疮性肾炎的无创诊断提供了新的候选标志物。统计学结果显示,这些基因在发现队列与验证队列中的丰度差异均具有统计学意义(p<0.05),提示其性能稳定。此外,研究还发现这些基因的丰度与SLE患者的自身抗体水平(如抗dsDNA、抗U1-RNP)呈负相关,推测:该类细菌基因可能通过调控支链氨基酸代谢影响宿主的免疫反应,进而参与SLE肾脏受累的发生发展,需进一步的机制研究验证。
