1. 领域背景与文献引入
文献英文标题:Enhanced expression of a 35 kDa fragment of inter-alpha-trypsin inhibitor H4 in sera of healthy pregnant women and patients with hydatidiform mole;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤生物标志物、妊娠内分泌与临床蛋白质组学。
肿瘤生物标志物是实现恶性肿瘤早期诊断、预后分层的核心工具,其中雌激素相关肿瘤(如子宫内膜癌、卵巢癌、乳腺癌)因发病机制与雌激素信号通路的密切关联,其特异性标志物的研发一直是领域研究热点。领域共识:α-胰蛋白酶抑制物重链4(ITIH4)是肝来源的血清蛋白家族成员,其C端包含激肽释放酶敏感的缓激肽样结构域,可被微量血浆激肽释放酶切割为35 kDa的O-糖基化片段;前期研究发现该片段在子宫内膜癌、卵巢癌等雌激素相关肿瘤患者血清中显著上调,被认为是潜在的肿瘤特异性标志物。不过,现有研究仅聚焦于肿瘤患者群体,未涉及妊娠、葡萄胎等非癌的高雌激素状态,无法明确该片段表达的特异性是否仅局限于肿瘤,也未直接验证其与血清雌激素水平的因果关联,这一局限性导致该片段作为肿瘤生物标志物的临床价值存在争议。因此,本研究旨在通过检测健康孕妇与葡萄胎患者血清中该片段的表达,明确其与雌激素水平的相关性,评估其作为肿瘤生物标志物的局限性。
2. 文献综述解析
作者对领域内现有研究从三个核心维度进行分类评述:一是ITIH4的分子结构与功能基础研究,二是35 kDa ITIH4片段在肿瘤中的表达谱研究,三是雌激素与激肽释放酶对ITIH4的调控机制研究。
现有研究表明,ITIH4是α-胰蛋白酶抑制物家族的独特成员,其C端的缓激肽样结构域使其对血浆激肽释放酶高度敏感,可被切割为35 kDa的C端片段与85 kDa的N端片段,其中35 kDa片段具有O-糖基化修饰,可通过特异性凝集素识别。在肿瘤研究领域,前期凝胶蛋白质组学与凝集素检测结果显示,该35 kDa片段在子宫内膜癌、卵巢癌、乳腺癌等雌激素相关肿瘤患者血清中显著上调,但在鼻咽癌、骨肉瘤、宫颈癌等非雌激素相关肿瘤中表达水平与健康对照无显著差异,提示其表达可能与雌激素水平相关。不过,现有研究仅聚焦于肿瘤患者群体,未涉及妊娠、葡萄胎等非癌的高雌激素状态,无法明确该片段表达的特异性是否仅局限于肿瘤,也未直接验证其与血清雌激素水平的因果关联,这一局限性导致该片段作为肿瘤生物标志物的临床价值存在争议。本研究的创新价值在于首次将研究群体扩展至非癌的高雌激素状态人群,通过直接对比健康孕妇、葡萄胎患者与健康非孕女性的血清样本,明确该35 kDa片段的表达与雌激素水平的直接相关性,而非肿瘤特异性,填补了现有研究在标志物特异性验证方面的空白。
3. 研究思路总结与详细解析
本研究的核心目标是验证35 kDa ITIH4片段作为肿瘤生物标志物的特异性,明确其在非癌高雌激素状态中的表达特征;核心科学问题为该片段的上调表达是否仅依赖于肿瘤发生,还是与高雌激素水平直接相关;技术路线遵循“临床样本分组→内分泌指标验证→蛋白质组学检测→分子鉴定→定量分析→结论推导”的闭环逻辑,通过多技术手段的组合应用实现研究目标。
3.1 血清样本收集与临床分组
实验目的是建立标准化的血清样本库,确保三组样本的临床特征匹配,为后续实验提供可靠的研究材料。方法细节为在马来西亚马来亚医学中心伦理委员会批准的前提下,收集20名健康非孕女性(对照组)、20名健康早期妊娠女性(妊娠组)、20名早期葡萄胎患者(葡萄胎组)的血清样本,所有样本均来自21-45岁的年龄匹配人群,妊娠组与葡萄胎组样本均采集于妊娠早期;血液样本采用BD真空采血管收集,经3000g离心10分钟分离血清,分装为100μl aliquots后于-80℃保存。结果解读显示,三组样本的年龄分布、样本处理流程均保持一致,排除了临床特征差异对实验结果的干扰,为后续的内分泌与蛋白质组学分析提供了标准化基础。实验所用关键产品:BD vacutainers采血管(Becton, Dickinson & Co)、Eppendorf 5403离心机。
3.2 血清雌二醇水平定量检测
实验目的是验证妊娠组与葡萄胎组的血清雌激素水平显著高于对照组,明确两组研究对象的高雌激素状态。方法细节采用ADVIA Centaur系统,按照厂商提供的操作说明书对三组样本的血清雌二醇水平进行定量检测,检测结果以均值±标准误(SEM)表示。结果解读显示,妊娠组的血清雌二醇水平为4816±610 pmol/L(n=20),葡萄胎组为3468±1955 pmol/L(n=20),对照组为393±91 pmol/L(n=20),两组妊娠相关样本的雌二醇水平均显著高于对照组,证实了研究对象的高雌激素状态,为后续蛋白质表达分析提供了内分泌学依据。
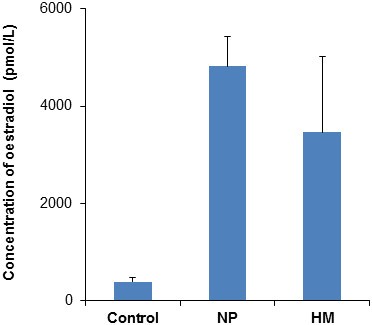
实验所用关键产品:ADVIA Centaur雌二醇检测系统(Siemens Medical Solutions Diagnostics)。
3.3 血清O-糖基化蛋白质双向电泳与凝集素印迹
实验目的是分离并特异性检测血清中O-糖基化的35 kDa ITIH4片段,对比三组样本的表达差异。方法细节为取约800μg血清蛋白,先与含9M尿素、60mM DTT的IPG样本缓冲液孵育,再经pH4-7的IPG干胶条进行等电聚焦,随后经8-18%梯度SDS-PAGE进行第二向电泳分离;分离后的蛋白质转移至硝酸纤维素膜,采用经辣根过氧化物酶标记的CGB凝集素(特异性结合O-糖链)进行印迹检测,通过显色反应显示目标蛋白。结果解读显示,双向电泳结果表明35 kDa ITIH4片段因O-糖基化异质性形成5个亚型斑点簇,妊娠组与葡萄胎组的该斑点簇信号强度显著高于对照组,直观显示其表达上调趋势。
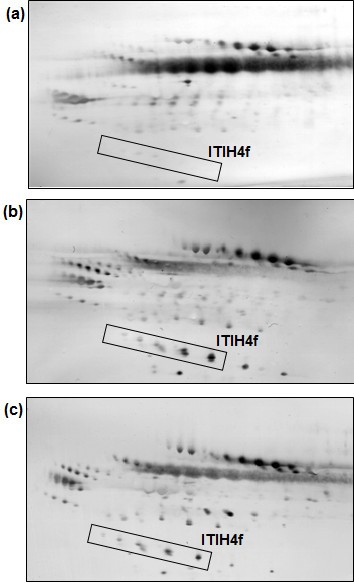
实验所用关键产品:GE Healthcare IPG Immobiline Drystrips、SE 600 Ruby电泳系统、Whatman硝酸纤维素膜、CGB凝集素。
3.4 蛋白质质谱鉴定与数据库检索
实验目的是确认双向电泳中差异表达的斑点簇为35 kDa ITIH4片段,明确其分子身份。方法细节为从硝酸纤维素膜上切取目标斑点,经膜上胰酶消化后,采用4800 Plus MALDI ToF/ToF质谱仪进行串联质谱分析;所得质谱数据通过MASCOT检索引擎比对Swiss-Prot数据库中的人类蛋白质序列,检索参数设置为胰酶消化、1个漏切位点、半胱氨酸氨基甲酰化与甲硫氨酸氧化为可变修饰。结果解读显示,质谱鉴定结果与数据库中ITIH4的序列匹配度符合蛋白质鉴定标准,结合双向电泳的分子量与等电点数据,确认该差异斑点簇为ITIH4的35 kDa截断片段。
实验所用关键产品:Applied Biosystems 4800 Plus MALDI ToF/ToF质谱仪、MASCOT检索引擎。
3.5 蛋白表达水平的图像定量分析
实验目的是定量比较三组样本中35 kDa ITIH4片段的表达差异,明确其上调幅度的统计学显著性。方法细节为采用Bio-Rad GS690成像密度仪扫描凝集素印迹膜,使用Image Master 2D Platinum软件分析目标斑点簇的体积占总糖蛋白斑点体积的百分比,该指标可消除上样量与染色差异对结果的影响;采用Student’s t-test进行统计学分析,P<0.01被认为具有显著性差异。结果解读显示,妊娠组的35 kDa ITIH4片段表达水平较对照组上调8.7倍(n=20,P=0.0002),葡萄胎组较对照组上调5.6倍(n=20,P<0.0001),上调幅度与前期在雌激素相关肿瘤患者中观察到的结果相当;同时,该片段在三组样本中的表达趋势与雌二醇水平的变化趋势一致,进一步支持其与雌激素水平的相关性。
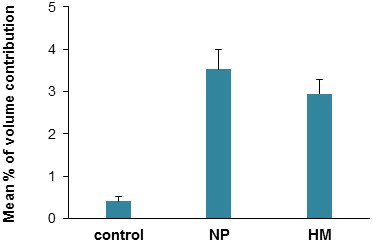
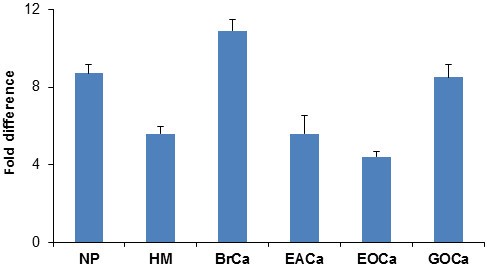
实验所用关键产品:Bio-Rad GS690成像密度仪、GE Healthcare Image Master 2D Platinum软件。
4. Biomarker研究及发现成果
本研究聚焦的Biomarker为O-糖基化修饰的35 kDa ITIH4片段,其筛选与验证逻辑为“基于前期肿瘤研究基础→扩展至高雌激素非癌人群→内分泌指标验证→蛋白质组学检测→质谱鉴定→定量分析→相关性推导”,通过多维度验证明确该标志物的表达特征与临床局限性。
该Biomarker的来源为人类血清样本,验证方法包括双向电泳-凝集素印迹技术(特异性检测O-糖基化蛋白)、MALDI ToF/ToF质谱鉴定(明确分子身份)、成像密度定量分析(比较表达差异)。特异性与敏感性方面,该片段在健康孕妇与葡萄胎患者中的表达上调幅度与雌激素相关肿瘤患者相当,说明其对肿瘤的特异性不足,无法区分癌性与非癌性的高雌激素状态;研究未提供该标志物的ROC曲线等诊断效能数据,无法评估其敏感性与特异性的量化指标。核心成果方面,该35 kDa ITIH4片段的表达与血清雌激素水平直接相关,不仅在子宫内膜癌、卵巢癌、乳腺癌等雌激素相关肿瘤中上调,也在健康妊娠与葡萄胎等非癌高雌激素状态中显著上调,其作为肿瘤生物标志物的局限性在于缺乏肿瘤特异性;统计学结果显示,妊娠组该片段表达上调8.7倍(n=20,P=0.0002),葡萄胎组上调5.6倍(n=20,P<0.0001),两组样本的血清雌二醇水平均显著高于健康对照(n=20,P值未明确提供,但图表显示差异显著)。此外,本研究首次明确该片段的表达仅依赖于高雌激素水平,而非肿瘤发生,为后续雌激素相关的蛋白质修饰研究提供了新的方向,但该标志物无法单独用于肿瘤的诊断,需与其他肿瘤特异性标志物联合使用。
