1. 领域背景与文献引入
文献英文标题:Maged1, a new regulator of skeletal myogenic differentiation and muscle regeneration;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:骨骼肌干细胞生物学与肌肉再生
领域共识:正常成年骨骼肌细胞更新缓慢,损伤或病理状态下,肌肉干细胞(卫星细胞)被激活,增殖后不可逆退出细胞周期并融合形成功能性肌纤维,该过程受肌源性调控因子(MRFs)如MyoD、肌生成素等的精密调控,同时依赖细胞周期的有序退出。当前研究热点聚焦于肌肉再生的分子调控网络,尤其是MAGE家族蛋白的功能,其中Necdin已被证实可促进肌成细胞存活与分化、改善肌肉再生,但同家族的Maged1在骨骼肌中的功能尚未明确。现有研究存在的核心空白是缺乏Maged1在骨骼肌分化与再生中的系统功能研究,而杜氏肌营养不良(DMD)患者肌肉中Maged1表达上调的现象提示其可能参与肌肉修复过程,因此本研究旨在明确Maged1在骨骼肌成肌分化与再生中的作用及分子机制,为肌肉疾病的治疗提供新的靶点参考。
2. 文献综述解析
作者从MAGE家族蛋白的功能分类、骨骼肌分化的调控机制、细胞周期退出与肌分化的关联三个维度对现有研究进行评述。在MAGE家族蛋白研究方面,Necdin作为该家族成员,已被证实通过调控肌源性因子表达、抑制TNF信号通路促进肌肉再生并保护肌纤维免受消耗;Maged1此前仅被报道在TNF受体介导的凋亡信号通路中发挥作用,其在骨骼肌中的功能完全未知。在骨骼肌分化调控领域,MRFs家族蛋白通过结合靶基因启动子的E-box序列激活肌特异性基因表达,同时诱导细胞周期抑制剂如p21表达,驱动细胞周期退出与终末分化,但现有研究尚未揭示Maged1是否参与这一调控网络。现有研究的局限性在于缺乏对Maged1在骨骼肌生理病理过程中功能的探究,无法解释DMD患者中Maged1表达上调的生物学意义。本研究的创新价值在于首次系统阐明了Maged1是骨骼肌成肌分化与再生的关键调控因子,通过调控p21表达与细胞周期退出实现对肌分化的调控,填补了MAGE家族蛋白在骨骼肌功能研究中的空白,为肌肉损伤修复的分子机制提供了新的视角。
3. 研究思路总结与详细解析
本研究的整体框架为“表达模式分析→转录调控机制→功能验证→机制探究”的闭环逻辑,研究目标是明确Maged1在骨骼肌成肌分化与再生中的功能及分子机制,核心科学问题是Maged1如何调控成肌细胞的细胞周期退出与终末分化,技术路线为首先通过细胞和动物模型检测Maged1在肌分化与再生中的表达动态,随后通过启动子分析明确其转录调控因子,再利用基因敲除细胞和动物模型验证Maged1的功能,最后通过分子实验探究其调控细胞周期的具体机制。
3.1 Maged1在成肌分化与肌肉再生中的表达模式分析
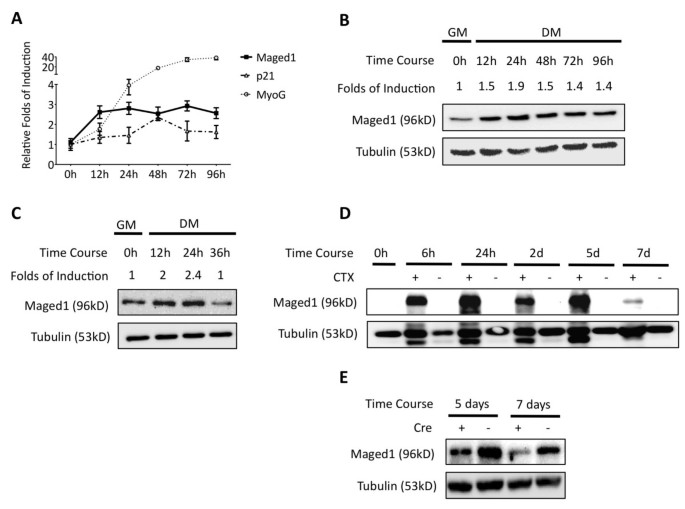
实验目的:明确Maged1在成肌细胞分化及损伤后肌肉再生过程中的表达动态。方法细节:采用C2C12成肌细胞系和原代小鼠成肌细胞,通过血清饥饿诱导分化,在0、24、48、72、96小时采用实时荧光定量PCR(qRT-PCR)和免疫印迹(Western blot)检测Maged1的RNA和蛋白水平;同时建立小鼠胫骨前肌(TA)肉毒毒素(CTX)损伤模型,在损伤后不同时间点采用免疫印迹检测Maged1蛋白表达,并通过肌细胞特异性敲除Maged1的小鼠明确其细胞来源。结果解读:在C2C12细胞中,Maged1在增殖期低表达,血清饥饿诱导分化后24小时RNA和蛋白水平分别上调3倍和2倍,并维持至分化结束;原代成肌细胞分化后Maged1蛋白水平上调2倍;野生型小鼠TA肌肉损伤后6小时Maged1蛋白显著诱导表达,而肌细胞特异性敲除Maged1的小鼠中Maged1诱导水平显著降低,表明Maged1的诱导表达主要来源于分化的肌细胞(图1)。产品关联:实验所用关键产品:BD Sciences的Maged1抗体(货号612500)、Qiagen的RNeasy mini试剂盒、Applied Biosystems的Power SYBR Green PCR Master Mix等。
3.2 Maged1转录调控机制研究
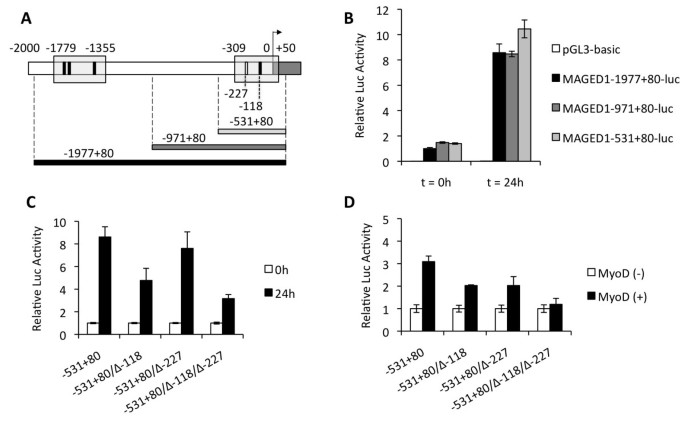
实验目的:探究Maged1在成肌分化中表达上调的转录调控机制。方法细节:通过生物信息学分析人、小鼠、猪、犬的Maged1启动子区域,寻找保守的E-box序列;构建包含不同长度Maged1启动子片段的荧光素酶报告基因载体,转染C2C12细胞,检测分化前后的荧光素酶活性;通过定点突变E-box序列验证其功能,并在NIH-3T3细胞中过表达MyoD,检测其对Maged1启动子的激活作用。结果解读:生物信息学分析显示Maged1启动子区域存在4个保守的E-box序列,其中近端的-227和-118位E-box在哺乳动物中高度保守;包含-531至+80片段的启动子载体在C2C12分化后荧光素酶活性上调约10倍,与全长启动子活性相当;突变-118位E-box后,分化诱导的荧光素酶活性显著降低;在NIH-3T3细胞中过表达MyoD可使Maged1启动子活性上调3倍,表明MyoD通过结合E-box序列激活Maged1的转录(图2)。产品关联:实验所用关键产品:Promega的Dual Luciferase Reporter Assay试剂盒、Fermentas的ExGen500转染试剂等。
3.3 Maged1缺失对成肌分化与肌肉再生的影响
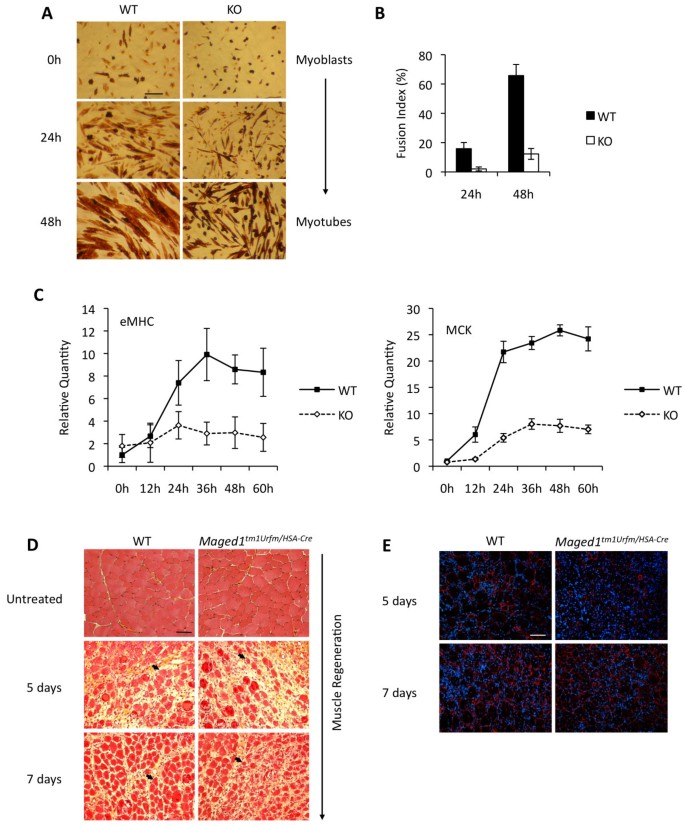
实验目的:验证Maged1在成肌分化与体内肌肉再生中的功能。方法细节:分离野生型和Maged1全身敲除小鼠的原代成肌细胞,血清饥饿诱导分化,通过免疫组化(IHC)检测肌球蛋白重链(MHC)表达,计算融合指数(多核肌管中核的比例),采用qRT-PCR检测晚期分化标志物胚胎肌球蛋白重链(eMHC)和肌酸激酶(MCK)的表达;同时构建肌细胞特异性Maged1敲除小鼠,通过CTX诱导TA肌肉损伤,在损伤后5天和7天采用苏木精-伊红(H&E)染色和层粘连蛋白免疫组化分析肌肉再生情况,测量新生肌纤维的横截面积。结果解读:Maged1缺失的原代成肌细胞在分化48小时后仅形成少量细肌管,融合指数在24小时和48小时均显著低于野生型细胞(n=3,P<0.01);eMHC和MCK的RNA水平显著降低(n=3,P<0.05);体内实验中,肌细胞特异性敲除Maged1的小鼠在损伤后5天新生肌纤维数量少且横截面积比野生型小47%(44±7 μm² vs 82±9 μm²,n=3,P<0.01),7天时差异仍存在但有所缩小(图3)。产品关联:实验所用关键产品:Santa Cruz的MHC抗体(货号Sc-20641)、Sigma-Aldrich的层粘连蛋白抗体(货号L9393)等。
3.4 Maged1调控成肌分化的分子机制探究
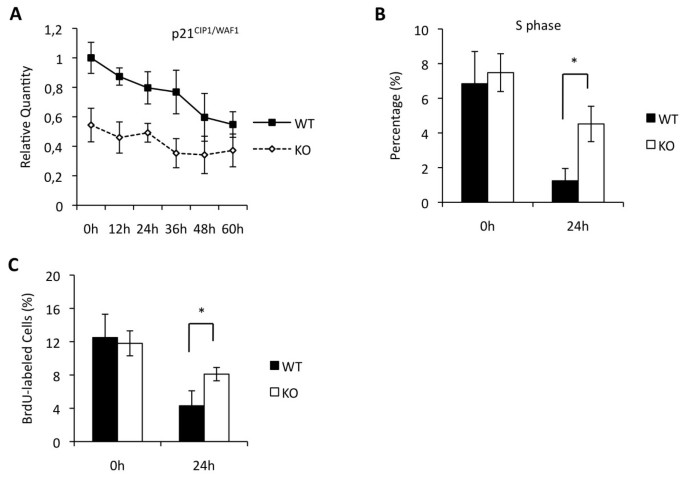
实验目的:明确Maged1调控成肌分化的下游分子机制,重点探究细胞周期退出的调控。方法细节:采用qRT-PCR检测野生型和Maged1敲除成肌细胞中肌源性调控因子MyoD、肌生成素(MyoG)、Mef2C及细胞周期抑制剂p21的RNA水平;通过流式细胞术分析细胞周期分布,采用BrdU掺入实验检测细胞增殖活性。结果解读:Maged1敲除成肌细胞中MyoD、MyoG、Mef2C的RNA水平与野生型无显著差异,但p21的RNA水平在增殖期和分化期均显著降低(n=3,P<0.05);流式细胞术显示,分化24小时后,Maged1敲除细胞中S期细胞比例是野生型的3倍(n=3,P<0.01);BrdU掺入实验显示,Maged1敲除细胞的BrdU阳性比例是野生型的2倍(n=3,P<0.01),表明Maged1缺失导致成肌细胞无法有效退出细胞周期,进而影响终末分化(图4)。产品关联:实验所用关键产品:BD Sciences的BrdU抗体(货号555627)、Invitrogen的TOPRO-3染色剂等。
4. Biomarker研究及发现成果
本研究中鉴定的核心生物标志物为Maged1,属于调控性生物标志物,其筛选与验证逻辑为“临床样本线索→细胞模型验证表达模式→基因敲除模型验证功能→分子机制解析”的完整链条。
Biomarker定位:Maged1是骨骼肌成肌分化与再生的关键调控性生物标志物,其表达模式具有阶段特异性,在正常成年肌肉中低表达,在成肌细胞分化早期及损伤后肌肉再生过程中显著上调。研究过程详述:Maged1的来源为骨骼肌卫星细胞激活后形成的成肌细胞及分化中的肌管,验证方法包括qRT-PCR、免疫印迹、免疫组化及体内损伤模型,特异性表现为仅在肌分化启动后及肌肉损伤早期诱导表达,敏感性方面,损伤后6小时即可检测到显著的蛋白表达上调;功能验证显示,Maged1缺失导致成肌细胞融合指数降低(n=3,P<0.01),体内新生肌纤维横截面积减少47%(n=3,P<0.01),p21表达水平降低(n=3,P<0.05),S期细胞比例增加3倍(n=3,P<0.01)。核心成果提炼:Maged1首次被证实为骨骼肌成肌分化与再生的必需因子,通过调控p21表达促进成肌细胞的细胞周期退出,进而保障肌管成熟与肌肉再生;其创新性在于填补了MAGE家族蛋白在骨骼肌功能研究中的空白,揭示了Maged1作为细胞周期调控因子在肌分化中的关键作用,为肌肉损伤修复及肌营养不良等疾病的治疗提供了潜在的靶点;所有关键实验数据均具有显著的统计学差异(P<0.05或P<0.01),样本量均为3次独立重复实验。
