1. 领域背景与文献引入
文献英文标题:lncRNA H19 promotes matrix mineralization through up-regulating IGF1 by sponging miR-185-5p in osteoblasts;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:骨代谢与成骨细胞生物学。
骨代谢是骨形成(成骨细胞主导)与骨吸收(破骨细胞主导)的动态平衡过程,成骨细胞的增殖、分化及基质矿化是骨形成的核心环节,其功能异常与骨质疏松、骨发育不良等疾病直接相关。近年来,长链非编码RNA(lncRNA)作为竞争性内源性RNA(ceRNA)调控microRNA(miRNA)及靶基因的机制,成为骨代谢研究的前沿方向。已有研究证实,lncRNA MALAT1、MEG3等通过ceRNA网络调控成骨细胞分化,但lncRNA H19在成骨细胞基质矿化中的具体功能及分子机制尚未完全阐明。此外,miR-185-5p虽被报道抑制成釉和成骨,但与H19的相互作用及对成骨细胞基质矿化的影响仍不清楚;胰岛素样生长因子1(IGF1)作为促进骨基质矿化的关键因子,其上游lncRNA-miRNA调控通路也有待挖掘。因此,探讨H19在成骨细胞基质矿化中的作用及分子机制,对揭示骨代谢调控网络、寻找骨疾病治疗靶点具有重要意义。
2. 文献综述解析
文献综述围绕“lncRNA在骨代谢中的作用”“ceRNA机制在成骨细胞功能调控中的研究现状”“H19、miR-185-5p及IGF1的已有研究”三个维度展开评述。现有研究表明,lncRNA可通过多种机制调控成骨细胞功能:如lncRNA MALAT1通过海绵miR-204促进人主动脉瓣间质细胞成骨分化;lncRNA H19通过激活Wnt/β-catenin通路促进成骨细胞分化。ceRNA机制(lncRNA-miRNA-mRNA网络)在成骨调控中的研究也逐步深入,例如lncRNA MEG3通过miR-27a-3p/IGF1轴促进矿化相关蛋白表达;但H19在成骨细胞基质矿化中的ceRNA调控网络尚未报道。对于关键分子,H19作为首个发现的lncRNA,虽被证实参与骨再生,但在成骨细胞基质矿化中的作用未知;miR-185-5p被报道抑制成釉和成骨,但具体靶点及通路未明;IGF1虽明确促进成骨细胞基质矿化,但其上游lncRNA-miRNA调控关系仍待阐明。
现有研究的局限性在于,缺乏H19对成骨细胞基质矿化的直接功能研究,以及H19-miR-185-5p-IGF1轴的调控机制尚未揭示。本研究的创新点在于,首次证实H19通过ceRNA机制海绵吸附miR-185-5p,上调IGF1表达,从而促进成骨细胞基质矿化,明确了H19在成骨细胞基质矿化中的作用及分子通路。
3. 研究思路总结与详细解析
本研究以“揭示lncRNA H19在成骨细胞基质矿化中的功能及分子机制”为目标,围绕“H19是否调控成骨细胞基质矿化”“H19通过何种机制调控矿化”两个核心科学问题,采用“矿化模型构建→表达差异分析→功能验证→机制解析→rescue实验”的闭环技术路线,最终明确了H19-miR-185-5p-IGF1轴的调控关系及对成骨细胞基质矿化的作用。
3.1 成骨细胞矿化模型构建与验证
实验目的:构建成骨细胞矿化模型并验证矿化表型及关键分子的表达差异。
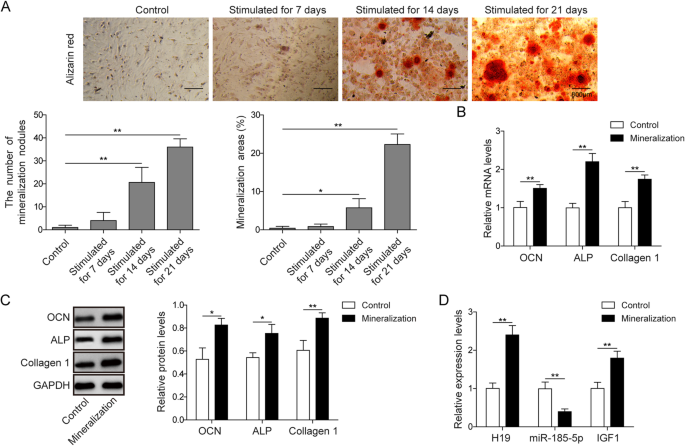
方法细节:采用小鼠前成骨细胞MC3T3-E1,分为对照组(α-MEM培养基)和矿化组(含10⁻⁸M地塞米松、50mg/L抗坏血酸、10mM β-甘油磷酸的α-MEM培养基),每3天换液,分别在培养7、14、21天后检测矿化指标。通过茜素红染色观察矿化结节,qPCR和Western blot检测矿化标志物(骨钙素OCN、碱性磷酸酶ALP、Ⅰ型胶原蛋白Col1a2)的mRNA和蛋白水平,qPCR检测H19、miR-185-5p和IGF1的表达。
结果解读:矿化组在7、14、21天的茜素红染色矿化结节及相对面积显著增加(图1a);矿化组OCN、ALP、Col1a2的mRNA和蛋白水平较对照组显著上调(图1b-c,n=3,P<0.05或P<0.01);H19和IGF1的mRNA水平显著上调,miR-185-5p水平显著下调(图1d,n=3,P<0.05或P<0.01)。
产品关联:实验所用关键试剂包括α-MEM培养基(Invitrogen)、胎牛血清(Invitrogen)、地塞米松(Sigma,推测)、抗坏血酸(Sigma,推测)、β-甘油磷酸(Sigma,推测)、qPCR试剂盒(Takara)、Western blot抗体(OCN、ALP、Col1a2购自abcam;GAPDH购自CST)。
3.2 H19敲低对成骨细胞矿化的功能影响
实验目的:验证H19对成骨细胞基质矿化的调控作用。
方法细节:用小干扰RNA(si-H19)或阴性对照(si-NC)转染MC3T3-E1细胞,qPCR检测H19敲低效率;qPCR和Western blot检测矿化标志物的mRNA和蛋白水平;ELISA检测细胞上清中Col1a2和骨特异性ALP(BALP)的水平;ALP染色检测ALP活性;茜素红染色检测矿化结节。
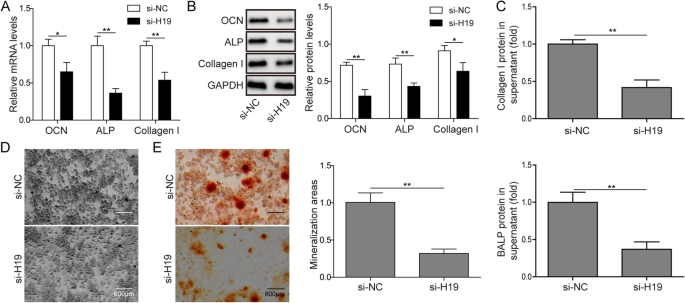
结果解读:si-H19处理后,H19水平较si-NC组下降约50%(图3a,n=3,P<0.01);OCN、ALP、Col1a2的mRNA和蛋白水平显著下调(图2a-b,n=3,P<0.05或P<0.01);细胞上清中Col1a2和BALP水平显著降低(图2c,n=3,P<0.01);ALP染色阳性率和茜素红染色矿化面积均显著减少(图2d-e,n=3,P<0.01)。
产品关联:实验所用关键产品包括si-H19和si-NC(Genepharma)、Lipofectamine 3000(Invitrogen)、ELISA试剂盒(BALP和Col1a2购自FineTest)、ALP染色试剂盒(GeFan biotechnology)。
3.3 H19与miR-185-5p的相互作用验证
实验目的:验证H19是否通过ceRNA机制海绵吸附miR-185-5p。
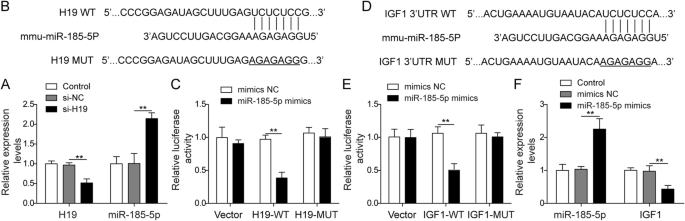
方法细节:用starBase预测H19与miR-185-5p的结合位点;构建H19野生型(H19-WT)和突变型(H19-MUT)荧光素酶报告质粒,与miR-185-5p mimics或阴性对照(miR-NC)共转染MC3T3-E1细胞,检测荧光素酶活性;qPCR检测H19敲低或miR-185-5p过表达后对方的表达水平。
结果解读:starBase预测H19与miR-185-5p存在互补结合位点(图3b);miR-185-5p mimics显著抑制H19-WT的荧光素酶活性,但对H19-MUT无影响(图3c,n=3,P<0.01);H19敲低后miR-185-5p水平显著上调(图3a,n=3,P<0.01)。
产品关联:实验所用关键产品包括starBase数据库(在线工具)、pGL3-control载体(Promega)、miR-185-5p mimics和miR-NC(RiboBio)、荧光素酶报告基因试剂盒(Promega)。
3.4 miR-185-5p对IGF1及矿化的功能影响
实验目的:验证miR-185-5p对IGF1表达及成骨细胞矿化的调控作用。
方法细节:用miR-185-5p mimics或miR-NC转染MC3T3-E1细胞,Western blot检测IGF1蛋白水平;qPCR和Western blot检测矿化标志物的mRNA和蛋白水平;ELISA检测细胞上清中Col1a2和BALP的水平;ALP染色和茜素红染色检测矿化表型。
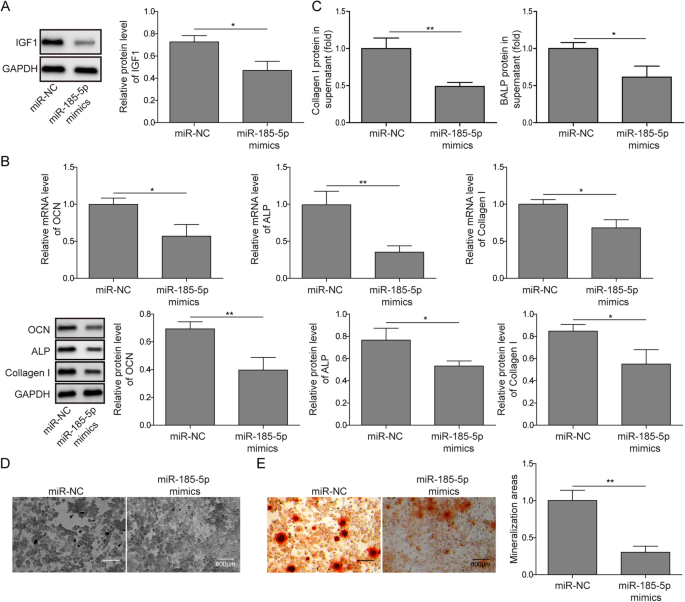
结果解读:miR-185-5p mimics处理后,IGF1蛋白水平显著下调(图4a,n=3,P<0.01);OCN、ALP、Col1a2的mRNA和蛋白水平显著降低(图4b,n=3,P<0.05或P<0.01);细胞上清中Col1a2和BALP水平显著下降(图4c,n=3,P<0.01);ALP染色阳性率和茜素红染色矿化面积均显著减少(图4d-e,n=3,P<0.01)。
产品关联:实验所用关键产品包括miR-185-5p mimics和miR-NC(RiboBio)、Western blot抗体(IGF1,推测购自abcam)。
3.5 H19-miR-185-5p-IGF1轴的rescue验证
实验目的:确认H19通过miR-185-5p-IGF1轴调控成骨细胞矿化。
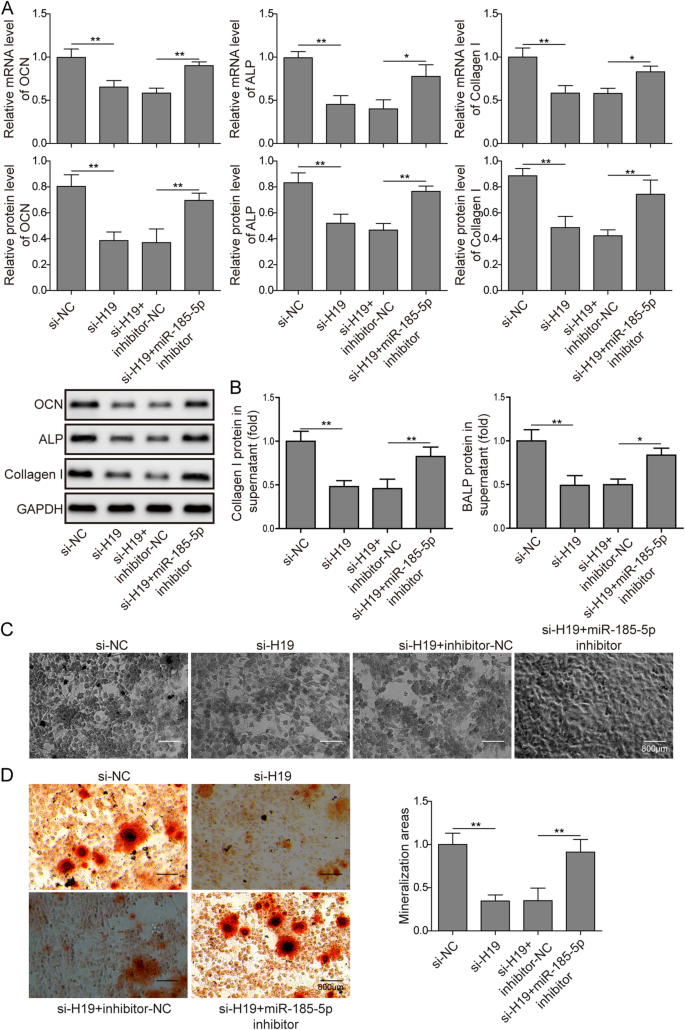
方法细节:用si-H19联合miR-185-5p inhibitor或抑制剂阴性对照(inhibitor-NC)转染MC3T3-E1细胞,qPCR和Western blot检测矿化标志物的mRNA和蛋白水平;ELISA检测细胞上清中Col1a2和BALP的水平;ALP染色和茜素红染色检测矿化表型。
结果解读:si-H19处理后,OCN、ALP、Col1a2的mRNA和蛋白水平显著下调,而联合miR-185-5p inhibitor后,这些指标均显著回升(图5a,n=3,P<0.01);细胞上清中Col1a2和BALP水平的抑制效应被逆转(图5b,n=3,P<0.01);ALP染色阳性率和茜素红染色矿化面积的减少也被修复(图5c-d,n=3,P<0.01)。
产品关联:实验所用关键产品包括miR-185-5p inhibitor和inhibitor-NC(RiboBio)。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究涉及的Biomarker为lncRNA H19、miR-185-5p和IGF1,均为成骨细胞基质矿化的调控分子。筛选逻辑基于“矿化诱导模型中的表达差异”:矿化组H19和IGF1上调、miR-185-5p下调(图1d);验证逻辑为“功能验证(敲低/过表达对矿化的影响)→机制验证(靶向结合)→rescue实验确认调控轴”,形成完整的“筛选-验证”链条。
研究过程与数据支撑
Biomarker来源为MC3T3-E1细胞的矿化诱导模型及转染模型;验证方法包括qPCR(RNA表达)、Western blot(蛋白表达)、ELISA(分泌蛋白水平)、ALP染色(酶活性)、茜素红染色(矿化结节)、荧光素酶报告基因(靶向结合)。具体数据:H19敲低后,OCN的mRNA水平较对照组下降约40%(图2a,n=3,P<0.01);miR-185-5p过表达后,IGF1蛋白水平下降约50%(图4a,n=3,P<0.01);rescue实验中,miR-185-5p inhibitor使si-H19组的OCN mRNA水平回升约60%(图5a,n=3,P<0.01)。
核心成果与创新性
本研究的核心成果为:(1)明确H19作为促矿化Biomarker,其表达水平与成骨细胞矿化正相关,敲低H19显著抑制矿化;(2)miR-185-5p作为抑矿化Biomarker,过表达显著抑制矿化;(3)IGF1作为下游效应Biomarker,介导H19和miR-185-5p的调控作用。创新性在于首次揭示H19-miR-185-5p-IGF1轴作为成骨细胞基质矿化的调控网络,为骨代谢疾病的治疗提供了新的靶点组合;同时明确了H19通过ceRNA机制发挥作用,为lncRNA在骨代谢中的功能研究提供了新的机制范例。
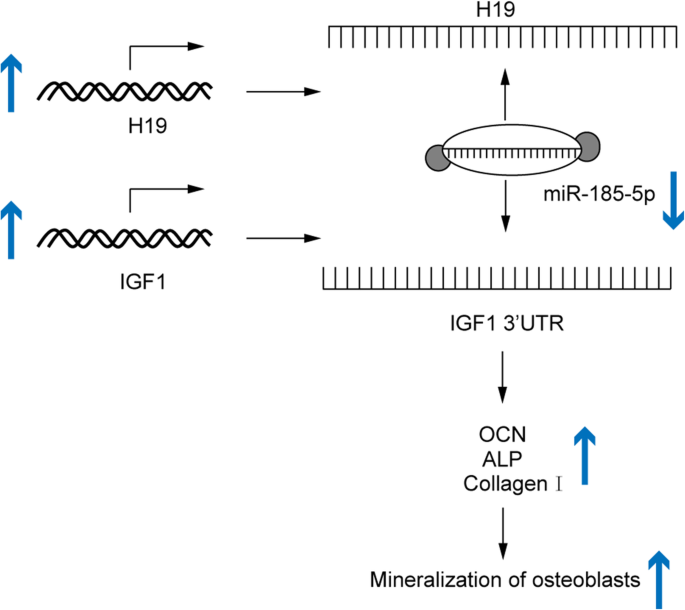
(图6:H19-miR-185-5p-IGF1轴调控成骨细胞基质矿化的机制示意图)
