1. 领域背景与文献引入
文献英文标题:Keratin 18 attenuates estrogen receptor α-mediated signaling by sequestering LRP16 in cytoplasm;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:乳腺癌雌激素受体α(ERα)信号调控。
乳腺癌是女性最常见的恶性肿瘤之一,雌激素受体α(ERα)的过度激活是ER阳性乳腺癌发生发展的核心驱动因素。ERα作为核受体转录因子,结合雌激素后会招募共激活因子(如LRP16)形成转录复合物,促进靶基因(如pS2、cyclin D1)表达,推动细胞增殖。LRP16是ERα的关键共激活因子,既是ERα的靶基因,又能通过正反馈环路增强ERα活性,其过表达与乳腺癌细胞的雌激素依赖增殖密切相关。另一方面,角蛋白18(K18)是上皮细胞中间丝蛋白,在正常乳腺腔上皮细胞中高表达,但在25%-80%的乳腺癌中表达下调,且与肿瘤高增殖率、不良预后显著相关。然而,K18调控乳腺癌细胞增殖的分子机制尚未明确,尤其是其与ERα信号通路的关系未被研究。本研究针对“K18如何调控ERα信号”这一核心问题,首次探索K18与LRP16的相互作用及对ERα信号的影响,旨在揭示K18下调促进乳腺癌增殖的机制。
2. 文献综述解析
作者围绕“ERα信号的共激活因子调控”和“K18的功能机制”两大维度综述现有研究。关键结论包括:①LRP16是ERα的共激活因子,通过与ERα直接结合增强其转录活性,促进MCF-7乳腺癌细胞的雌激素依赖增殖;②K18在乳腺癌中表达下调,与肿瘤大小、分化程度、有丝分裂指数等增殖相关参数显著负相关,但分子机制未知。现有研究的技术优势在于采用MCF-7细胞模型(ERα阳性、雌激素依赖)模拟临床ER阳性乳腺癌的生物学特性,但局限性是未探索K18与ERα共激活因子的相互作用。
本研究的创新价值在于:首次发现K18与LRP16的物理相互作用,证明K18通过将LRP16隔离在细胞质中,减少其核内丰度,从而减弱ERα介导的转录和细胞周期进展。这一发现填补了K18调控ERα信号机制的研究空白,解释了“K18下调→LRP16核定位增加→ERα信号增强→乳腺癌增殖加快”的分子链路,为ER阳性乳腺癌的靶向治疗提供了新的理论依据。
3. 研究思路总结与详细解析
3.1 整体框架
研究目标:阐明K18对LRP16亚细胞定位及ERα信号的调控机制;核心科学问题:K18是否与LRP16相互作用,如何影响其核定位及ERα介导的转录和细胞周期;技术路线:酵母双杂交筛选相互作用蛋白→体外(GST pulldown)和体内(CoIP)验证相互作用→亚细胞定位分析→功能实验(报告基因、qPCR、ChIP)检测ERα信号→细胞周期分析。
3.2 酵母双杂交筛选LRP16相互作用蛋白
实验目的:筛选与LRP16相互作用的蛋白。方法细节:以LRP16为诱饵构建pGBKT7-LRP16质粒,转化酵母AH109细胞,与MCF-7细胞cDNA文库(pGADT7载体)进行杂交,通过β-半乳糖苷酶活性检测相互作用。结果解读:筛选到K18作为候选相互作用蛋白,β-半乳糖苷酶活性显著高于空载体对照,阳性对照(p53与SV40大T抗原)验证实验系统有效性。
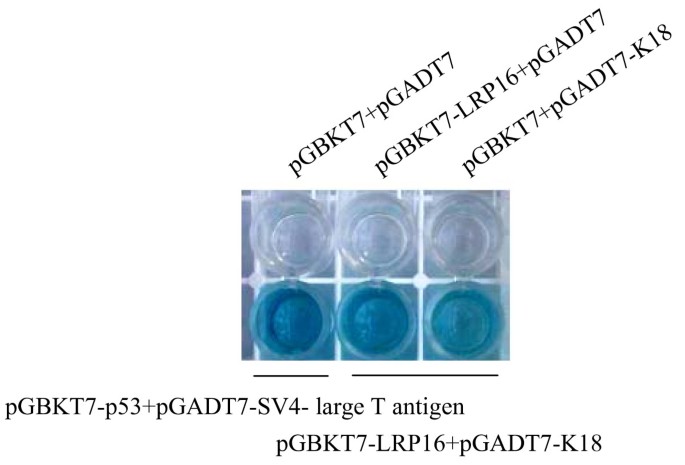
产品关联:文献未提及具体实验产品,领域常规使用Clontech MATCHMARKER酵母双杂交系统。
3.3 GST pulldown验证相互作用区域
实验目的:确定K18与LRP16的相互作用区域。方法细节:①构建GST-LRP16融合蛋白,与体外翻译的^{35}S标记的K18全长及缺失突变体(N端1-150 aa、中段80-375 aa、C端301-430 aa/390-430 aa)孵育,SDS-PAGE分离后放射自显影;②构建GST-LRP16缺失突变体(N端1-160 aa、C端161-324 aa),与K18孵育验证LRP16的结合区域。结果解读:K18的C末端(301-430 aa)是与LRP16结合的关键区域,而LRP16的C末端(161-324 aa,含macro结构域)是结合K18的核心区域。
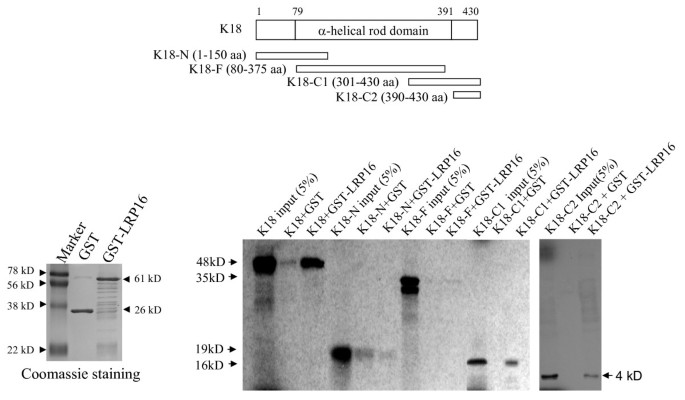
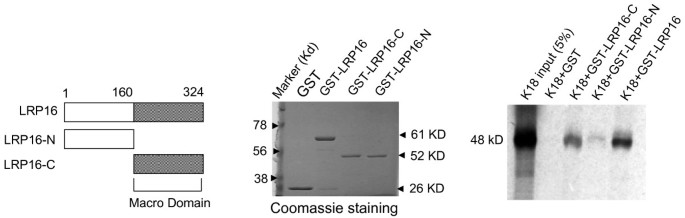
产品关联:文献未提及具体实验产品,领域常规使用pGEX载体(Amersham)构建GST融合蛋白,Promega TNT系统进行体外翻译。
3.4 CoIP验证体内相互作用
实验目的:验证K18与LRP16在哺乳动物细胞内的相互作用。方法细节:①MCF-7细胞转染LRP16表达载体或空载体,用抗K18抗体免疫沉淀,抗LRP16抗体检测结合情况;②转染Flag-K18-C1(301-430 aa)载体,用抗Flag抗体免疫沉淀,抗LRP16抗体检测内源性LRP16的结合。结果解读:LRP16与K18在体内特异性相互作用,Flag-K18-C1可与内源性LRP16共沉淀,证明C末端是体内相互作用的关键区域。
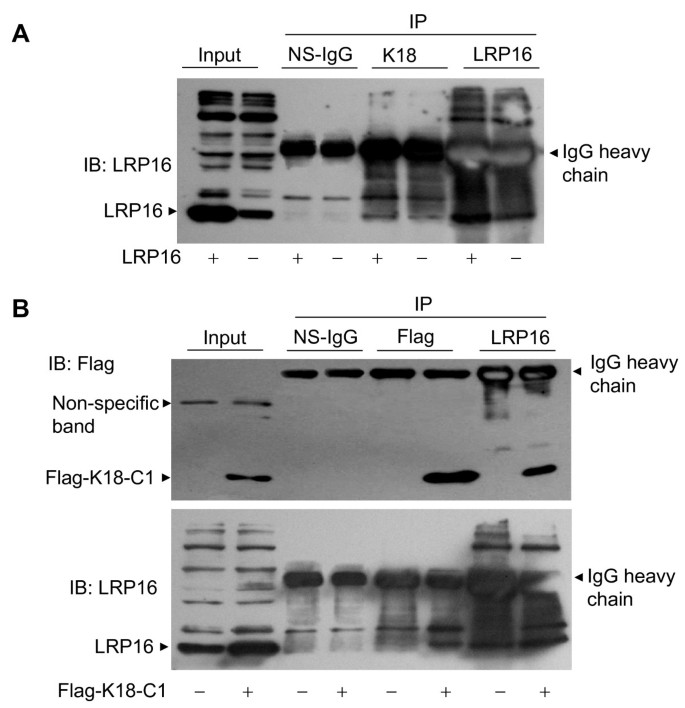
产品关联:使用兔抗LRP16抗体、鼠抗K18抗体(Abgent)、兔抗Flag抗体(Sigma)进行免疫沉淀和印迹。
3.5 荧光分析LRP16亚细胞定位
实验目的:研究K18对LRP16亚细胞定位的影响。方法细节:MCF-7细胞共转染LRP16-GFP融合蛋白与K18表达载体或空载体,DAPI染色细胞核,荧光显微镜观察GFP信号分布,统计核定位细胞比例。结果解读:空载体转染时,78%的细胞中LRP16-GFP定位于细胞核;K18转染后,仅32%的细胞中LRP16-GFP定位于细胞核,68%定位于细胞质,证明K18可将LRP16隔离在细胞质中。
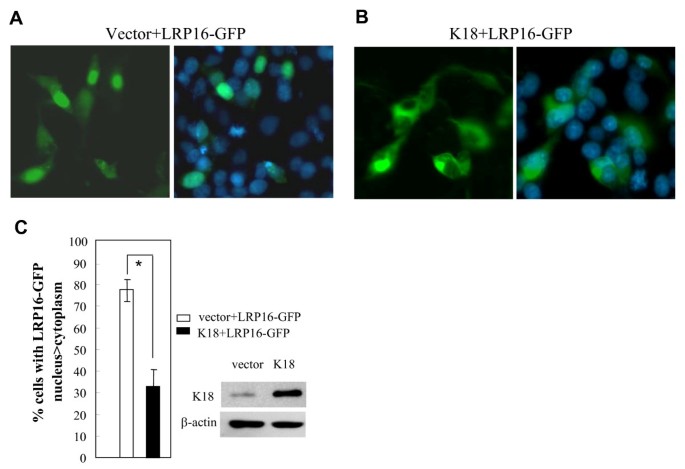
产品关联:使用pEGFP-N1载体构建融合蛋白,Olympus IX-71荧光显微镜观察。
3.6 细胞质/细胞核组分免疫印迹
实验目的:量化K18对LRP16亚细胞分布的影响。方法细节:MCF-7细胞转染K18表达载体或K18 siRNA,用ReadyPrep试剂盒分离细胞质和细胞核组分,免疫印迹检测LRP16水平,β-actin(细胞质)和Sp1(细胞核)作为内参。结果解读:K18过表达显著增加细胞质LRP16水平,降低细胞核水平;K18敲低则相反,且不影响总LRP16水平,证明K18仅调控LRP16的亚细胞分布,不影响其总表达。
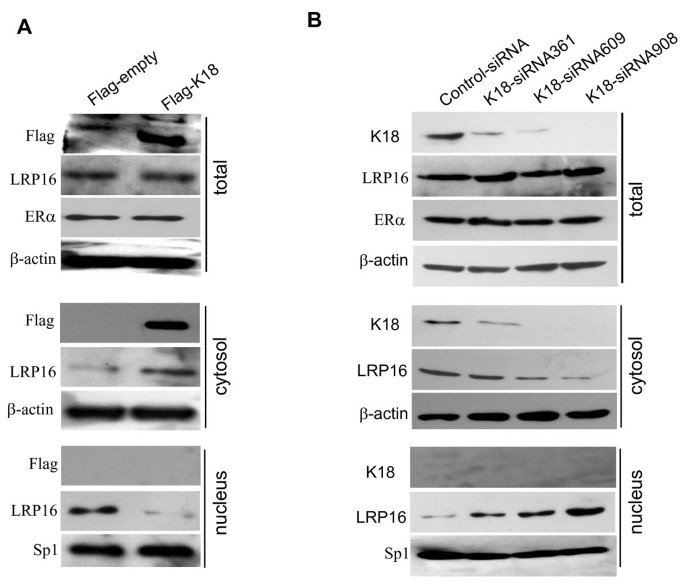
产品关联:使用Bio-Rad ReadyPrep蛋白提取试剂盒分离细胞质和细胞核组分。
3.7 报告基因实验检测ERα转录活性
实验目的:研究K18对ERα介导的转录活性的影响。方法细节:MCF-7细胞转染3×ERE-TATA-Luc报告基因(含3个雌激素反应元件)、ERα表达载体及K18/LRP16表达载体或siRNA,E2(100 nM)处理后检测luciferase活性,pRL-SV40作为转染对照。结果解读:①K18过表达使E2诱导的luciferase活性从2.3倍降至1.5倍;②LRP16过表达增强活性(3.5倍),但被K18抑制(2.0倍);③K18 siRNA增强E2诱导的活性(3.0倍),证明K18通过抑制LRP16功能减弱ERα转录活性。
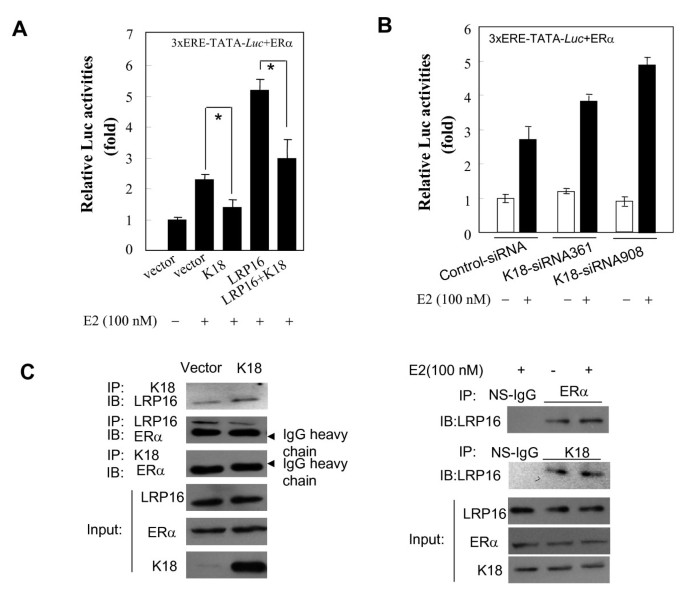
产品关联:使用Qiagen Superfect转染试剂、Promega Luciferase Assay系统检测活性。
3.8 qPCR检测ERα靶基因表达
实验目的:验证K18对ERα靶基因mRNA水平的影响。方法细节:MCF-7细胞转染K18/LRP16表达载体或siRNA,E2处理后提取总RNA,反转录为cDNA,qPCR检测pS2、cyclin D1、c-Myc的表达,HPRT作为内参。结果解读:K18过表达使E2诱导的pS2、cyclin D1、c-Myc mRNA水平分别降低40%、35%、30%;LRP16过表达缓解这种抑制(仅降低15%、10%、10%);K18 siRNA使靶基因水平增加50%-60%,证明K18通过抑制LRP16减少ERα靶基因表达。
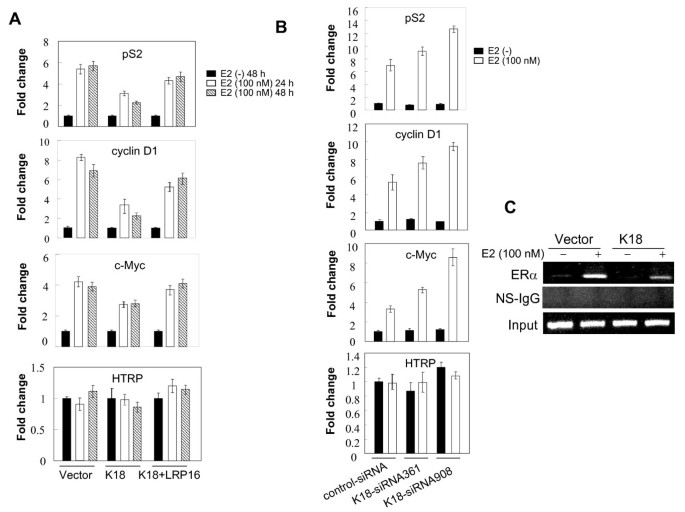
产品关联:使用Invitrogen TRIzol试剂提取RNA,Superscript II反转录酶合成cDNA。
3.9 ChIP检测ERα结合靶基因启动子
实验目的:研究K18对ERα结合靶基因启动子的影响。方法细节:MCF-7细胞转染K18表达载体,E2处理后,用抗ERα抗体免疫沉淀染色质,PCR检测pS2启动子的结合情况。结果解读:K18过表达使E2诱导的ERα与pS2启动子的结合减少50%,证明K18通过降低核内LRP16水平,抑制ERα与靶基因启动子的结合。
产品关联:使用Qiagen QIAquick Spin Kit纯化免疫沉淀的DNA。
3.10 BrdU掺入实验检测细胞周期
实验目的:研究K18对E2诱导的细胞周期S期进入的影响。方法细节:MCF-7细胞转染K18/LRP16表达载体或siRNA,E2处理后,BrdU标记12小时,荧光显微镜观察GFP阳性细胞的BrdU掺入率(S期比例)。结果解读:①E2处理使S期比例从10%增加至23%;②K18过表达使S期比例仅增加至14%;③LRP16过表达使S期比例增加至30%,但被K18抑制(18%);④K18 siRNA使S期比例增加至35%,证明K18通过抑制LRP16减弱E2诱导的细胞周期进展。
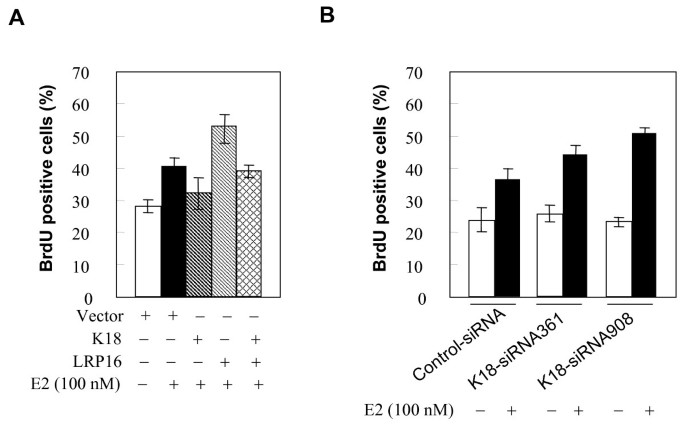
产品关联:使用Becton Dickinson抗BrdU抗体检测DNA合成。
4. Biomarker研究及发现成果解析
4.1 Biomarker定位与筛选逻辑
本研究涉及的Biomarker包括K18表达水平和LRP16亚细胞定位,筛选逻辑基于“K18-LRP16相互作用→LRP16核定位→ERα信号→细胞增殖”的功能链路。验证逻辑为:①通过细胞系实验(过表达/敲低)验证K18对LRP16定位的调控;②通过功能实验(报告基因、qPCR、ChIP、BrdU)验证其对ERα信号和细胞周期的影响。
4.2 研究过程与核心成果
Biomarker来源:乳腺癌细胞系(MCF-7)的内源性蛋白;验证方法包括免疫印迹(K18表达水平)、荧光显微镜和细胞质/细胞核组分分析(LRP16亚细胞定位)、功能实验验证其调控ERα信号的能力。
核心成果:①K18表达水平与LRP16核定位负相关:K18过表达使LRP16核定位率从78%降至32%(n=3,P<0.05),K18敲低则使核定位率增加至85%(n=3,P<0.05);②K18表达水平与ERα信号负相关:K18过表达使E2诱导的luciferase活性降低40%(n=3,P<0.05),靶基因mRNA水平降低30%-40%(n=3,P<0.05);③K18表达水平与细胞增殖负相关:K18过表达使E2诱导的S期比例减少60%(n=3,P<0.05),K18敲低使S期比例增加50%(n=3,P<0.05)。
4.3 创新性与临床意义
本研究首次将K18表达水平与LRP16亚细胞定位关联,证明K18是LRP16的功能抑制因子,其下调会导致LRP16核定位增加、ERα信号增强、细胞增殖加快。这一发现为ER阳性乳腺癌的预后评估提供了新的Biomarker组合(K18低表达+LRP16核定位高),同时为靶向治疗提供了新靶点(如恢复K18表达或抑制LRP16核定位)。
总结:本研究通过多层面实验揭示了K18调控ERα信号的分子机制,解释了K18下调促进乳腺癌增殖的原因,为ER阳性乳腺癌的基础研究和临床治疗提供了重要理论支持。