1. 领域背景与文献引入
文献英文标题:Metastasis suppression: a role of the Dice(r);发表期刊:Genome Biology;影响因子:未公开;研究领域:肿瘤转移与微小RNA(miRNA)调控
人类癌症死亡的绝大多数归因于远处转移,而非原发肿瘤本身,转移的发生依赖于一系列复杂的细胞生物学事件构成的“侵袭-转移级联反应”,涉及肿瘤细胞的远处播散及在异质微环境中的适应,目前对转移发病机制的理解仍不完整。微小RNA作为一类进化保守的调控RNA,通过靶向mRNA的3"非翻译区抑制基因表达,在侵袭-转移级联反应中发挥关键作用,过去3年的研究已鉴定出多个促进或抑制转移特定步骤的单个微小RNA,但针对微小RNA生成关键酶的整体调控在转移中的作用尚未明确。此前研究发现肿瘤组织中整体微小RNA水平常降低,抑制微小RNA生成关键酶Dicer可促进原发肿瘤发生,但Dicer在肿瘤转移中的具体功能仍属研究空白,本文综述的两项研究首次解析了Dicer作为乳腺癌转移抑制因子的作用及上游调控通路,填补了该领域的关键空白。
2. 文献综述解析
本综述以Dicer的上游调控通路为分类维度,整合了两项独立研究的成果,分别从转录后调控(miR-103/107介导)和转录调控(TaP63介导)两个层面,系统阐述了Dicer在乳腺癌转移中的抑制作用及分子机制。
此前领域内研究已证实微小RNA整体水平在人类肿瘤标本中普遍降低,实验性抑制Dicer或其他微小RNA生成通路组分可加速原发肿瘤的发展,但这些研究均未聚焦Dicer在肿瘤转移进程中的功能。Piccolo团队的研究发现,miR-103/107家族微小RNA可直接靶向Dicer的mRNA,在多种癌细胞系及乳腺癌患者组织标本中,miR-103/107与Dicer的表达呈负相关,且miR-103/107的表达与乳腺癌患者的转移复发倾向正相关;功能实验显示,过表达miR-103/107可增强乳腺癌细胞的体外运动能力,而强制表达Dicer可逆转该效应,shRNA介导的内源性Dicer敲低也能增强细胞体外运动能力,裸鼠异种移植模型进一步证实miR-107过表达可赋予弱转移性乳腺癌细胞更强的转移能力,且该效应可被Dicer过表达完全消除。Flores团队的研究则发现,p53相关转录因子TaP63的基因缺陷小鼠发生转移性肿瘤的频率显著升高,TaP63可通过染色质免疫沉淀(ChIP)直接结合Dicer的启动子区域,调控Dicer的转录表达,TaP63缺陷细胞系中Dicer的mRNA水平显著降低,且在患者来源的转移性肿瘤标本中,TaP63低表达与Dicer低表达呈正相关;功能实验显示,强制表达Dicer可逆转TaP63缺陷导致的细胞体外侵袭性增强。
此前领域内尚未明确Dicer在肿瘤转移中的功能,这两项研究首次证实了Dicer作为乳腺癌转移抑制因子的核心作用,同时解析了两条独立的上游调控通路,不仅完善了微小RNA调控网络在转移中的作用机制,也为乳腺癌转移的诊断和治疗提供了新的潜在靶点,具有重要的学术价值。
3. 研究思路总结与详细解析
本综述整合的两项研究均围绕“Dicer调控乳腺癌转移的分子机制”这一核心科学问题,采用“临床样本关联分析→细胞功能验证→动物模型验证(部分)”的研究逻辑,分别从转录后和转录水平解析Dicer的调控机制及功能效应,形成了完整的实验验证闭环。
3.1 miR-103/107对Dicer的转录后调控及转移功能验证
实验目的:明确miR-103/107对Dicer的靶向调控关系,及该调控在乳腺癌转移中的功能效应。
方法细节:首先通过生物信息学预测结合实验验证,确定miR-103/107与Dicer mRNA的靶向结合关系,随后在多种乳腺癌细胞系及临床组织标本中,采用实时荧光定量PCR(qRT-PCR)检测miR-103/107与Dicer的表达水平,通过过表达/抑制miR-103/107、shRNA敲低内源性Dicer、强制表达Dicer等基因操作,结合细胞划痕实验、Transwell实验检测细胞运动及侵袭能力,构建裸鼠异种移植模型检测体内转移能力。
结果解读:实验结果显示,miR-103/107与Dicer的表达在细胞系及临床标本中均呈显著负相关(文献未明确样本量及P值),过表达miR-103/107可使乳腺癌细胞体外运动能力显著增强,该效应可被Dicer过表达完全逆转,裸鼠异种移植模型中,miR-107过表达组的肺部转移结节数量显著多于对照组(文献未明确样本量及P值),同时miR-103/107过表达或Dicer敲低可诱导正常乳腺上皮细胞发生上皮-间质转化(EMT)。
产品关联:文献未提及具体实验产品,领域常规使用实时荧光定量PCR试剂盒、免疫印迹(WB)试剂盒、Transwell小室、裸鼠异种移植模型相关试剂等。
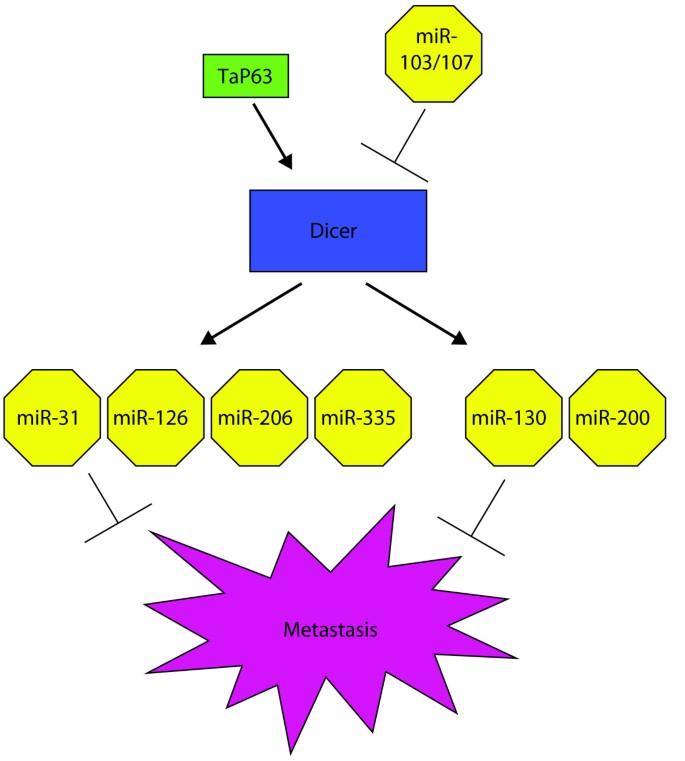
图注:图1展示了已知的涉及Dicer的转移调控信号通路组分,其中miR-31、miR-126、miR-206和miR-335的转移抑制作用已在体内实验中直接证实,miR-130和miR-200的转移作用则由体外实验暗示,尚未在体内直接分析。
3.2 TaP63对Dicer的转录调控及转移功能验证
实验目的:明确TaP63对Dicer的转录调控关系,及该调控在肿瘤转移中的功能效应。
方法细节:首先构建TaP63基因缺陷小鼠模型,统计不同基因型小鼠的转移性肿瘤发生率,随后在TaP63缺陷细胞系及患者来源的转移性肿瘤标本中,采用实时荧光定量PCR检测Dicer的表达水平,通过染色质免疫沉淀(ChIP)实验验证TaP63与Dicer启动子的直接结合,结合Transwell实验检测细胞侵袭能力,强制表达Dicer验证功能逆转效应。
结果解读:实验结果显示,TaP63+/-和TaP63-/-小鼠发生转移性癌的比例相当,且TaP63+/-小鼠发生转移性肉瘤的风险高于TaP63-/-小鼠(文献未明确样本量及P值),TaP63缺陷细胞系中Dicer的mRNA水平显著降低(文献未明确样本量及P值),染色质免疫沉淀实验证实TaP63可直接结合Dicer的启动子区域,强制表达Dicer可完全逆转TaP63缺陷导致的细胞体外侵袭性增强。
产品关联:文献未提及具体实验产品,领域常规使用基因编辑小鼠模型、染色质免疫沉淀(ChIP)试剂盒、实时荧光定量PCR试剂盒、Transwell小室等。
4. Biomarker研究及发现成果解析
本综述涉及的Biomarker包括miR-103/107、Dicer及TaP63,筛选及验证逻辑为“临床样本关联分析→细胞功能验证→动物模型验证(部分)”,覆盖了从临床相关性到功能效应的完整验证链条。
Biomarker的来源及验证方法如下:miR-103/107的来源为乳腺癌患者组织标本及癌细胞系,采用实时荧光定量PCR检测其表达水平,验证方法包括细胞功能实验(运动、侵袭)及裸鼠异种移植模型;Dicer的来源为癌细胞系、基因缺陷小鼠组织及患者转移性肿瘤标本,采用实时荧光定量PCR检测mRNA水平,推测采用免疫印迹检测蛋白水平;TaP63的来源为基因缺陷小鼠组织及患者转移性肿瘤标本,采用基因型分析及实时荧光定量PCR检测表达水平。文献未明确提供上述Biomarker的特异性与敏感性量化数据(如ROC曲线AUC值、敏感性、特异性等)。
核心成果提炼:miR-103/107可作为乳腺癌转移复发的潜在预后Biomarker,其表达与乳腺癌患者转移复发倾向正相关;Dicer作为转移抑制因子,其表达水平与乳腺癌转移风险负相关,且受miR-103/107的转录后调控及TaP63的转录调控;TaP63作为Dicer的上游调控因子,其缺陷与转移性肿瘤的发生风险正相关。本研究首次在乳腺癌中发现miR-103/107-Dicer及TaP63-Dicer这两条调控通路与转移的关联,为乳腺癌转移的机制研究及靶向治疗提供了新的方向,文献未明确提供上述关联的具体统计学结果(如HR值、P值、样本量等)。
