1. 领域背景与文献引入
文献英文标题:Sphingosine kinase 2 supports the development of BCR/ABL-independent acute lymphoblastic leukemia in mice;发表期刊:Biomarker Research;影响因子:未公开;研究领域:急性淋巴细胞白血病的分子机制与靶向治疗
鞘氨醇激酶(SphK)是调控鞘脂代谢稳态的关键酶,分为SphK1和SphK2两个亚型,其介导生成的鞘氨醇-1-磷酸(S1P)在细胞存活、增殖、迁移等过程中发挥核心调控作用。领域共识:SphK1在恶性肿瘤中的促癌作用已得到广泛证实,其过表达与多种实体瘤患者的不良预后、治疗耐药密切相关,且其抑制剂在急性髓系白血病(AML)中展现出明确的临床前活性,为血液系统肿瘤的靶向治疗提供了潜在方向。相比之下,SphK2的功能研究起步较晚,早期存在争议,但近年来的研究逐渐明确其在恶性疾病中的促癌功能,包括促进肿瘤细胞存活、增强化疗耐药性等,其特异性抑制剂已完成I期临床研究并进入II期,涵盖B细胞恶性肿瘤等多种癌症类型。
急性淋巴细胞白血病(ALL)是儿童及成人常见的血液系统恶性肿瘤,BCR/ABL1融合基因是部分ALL的驱动因素,但仍有超过半数的ALL属于BCR/ABL非依赖性亚型,这类ALL的发病机制尚未完全阐明,缺乏针对性的靶向治疗策略。此前研究仅在BCR/ABL1驱动的ALL模型中证实了SphK2的促癌作用,而BCR/ABL非依赖性ALL中SphK2的功能尚未被探索,这一研究空白为本文的开展提供了核心必要性,旨在明确SphK2在非BCR/ABL驱动的ALL发生中的作用,拓展SphK2抑制剂的临床适用范围。
2. 文献综述解析
作者以SphK亚型为核心分类维度,系统综述了SphK1和SphK2在恶性肿瘤中的研究进展,明确现有研究的成果与局限性,进而精准定位本文的研究切入点。
现有研究中,SphK1的促癌机制已较为清晰,在肺癌、乳腺癌、胃癌等多种实体瘤中,SphK1过表达与患者不良生存结局直接相关,且其介导的信号通路可增强肿瘤细胞的化疗耐药性;针对SphK1的抑制剂在AML中展现出显著的临床前活性,为血液系统肿瘤的靶向治疗提供了新方向。而SphK2的研究起步较晚,早期因部分研究结果矛盾存在争议,但近年来的大量研究证实其在多种肿瘤中发挥促癌作用,包括调控肿瘤细胞存活、参与肿瘤微环境重塑等,其特异性抑制剂ABC294640已进入II期临床研究,涵盖肝细胞癌、多发性骨髓瘤等多种癌症。不过,现有关于SphK2在ALL中的研究仅局限于BCR/ABL1驱动的亚型,对于占比更高的BCR/ABL非依赖性ALL,SphK2的功能尚未被阐明,这一空白限制了SphK2抑制剂在ALL中的全面应用。
本文的创新价值在于首次聚焦BCR/ABL非依赖性ALL模型,通过基因敲除策略明确SphK2的促癌作用,填补了这一领域的研究空白,为SphK2抑制剂在更多ALL亚型中的临床应用提供了实验依据,拓展了鞘脂代谢通路靶向治疗的适用范围。
3. 研究思路总结与详细解析
本文的研究目标是明确SphK2在BCR/ABL非依赖性ALL发生中的调控作用,核心科学问题是SphK2是否参与ARF缺失诱导的ALL发生过程,技术路线遵循“基因工程模型构建→疾病诱导与监测→表型分析与机制推测”的闭环逻辑,通过对比SphK2缺失与野生型小鼠的疾病发生情况,验证SphK2的功能。
3.1 基因工程小鼠模型构建与验证
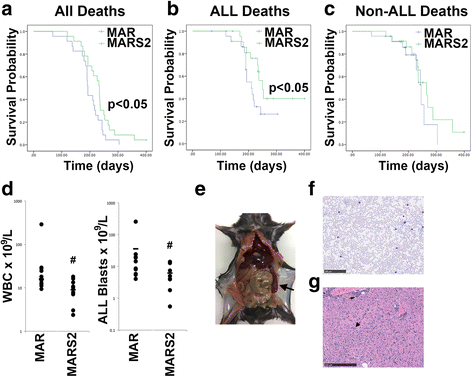
实验目的是构建BCR/ABL非依赖性的ALL小鼠模型,并探究SphK2缺失对该模型中ALL发生的影响。方法细节:将携带floxed ARF基因的小鼠与Rag1敲除小鼠杂交,获得Mx1.Cre.ARFfl/fl.Rag1-/-(MAR)小鼠,再将其与SphK2全身敲除小鼠杂交,得到Mx1.Cre.ARFfl/fl.Rag1-/- .SphK2-/-(MARS2)小鼠;在小鼠6周龄时,通过腹腔注射PolyI:polyC(15mg/kg,每2天1次,共3次)诱导ARF基因的条件性缺失,通过PCR技术验证基因缺失效率;对所有实验小鼠进行长达400天的生存监测,定义ALL的诊断标准为死亡时骨髓和脾脏中B220+CD19+Gr1-细胞占主要比例,采用Kaplan-Meier法进行生存分析。结果解读:MAR小鼠的中位生存时间为193天,61%的小鼠最终发生B系ALL;而MARS2小鼠的中位生存时间延长至234天(文献未明确提供样本量,p<0.05),ALL发生率降至43%(文献未明确提供样本量,p=0.044),说明SphK2缺失可显著降低BCR/ABL非依赖性ALL的发生风险。实验所用关键产品:DirectPCR Lysis Reagent(Viagen Biotech)、proteinase K(Promega)、MyTaq DNA polymerase(Bioline)、流式抗体(BD Biosciences、Australian Biosearch、Thermofisher Scientific)、NanoZoomer Slide Scanner(SDR Scientific)等。

3.2 疾病表型分析与验证
实验目的是验证SphK2缺失对ALL疾病特征的影响,明确其作用环节是疾病起始还是进展。方法细节:对发病小鼠进行血常规检测,分析外周血白细胞计数(WBC)和循环 blast细胞比例;采用流式细胞术分析骨髓、脾脏细胞的表面标志物,包括B220、CD19、Gr1、CD43、IgM等,明确细胞亚型;对肝脏、脾脏等组织进行组织学检查,观察肿瘤细胞浸润情况。结果解读:MARS2小鼠发生ALL时的WBC和循环 blast细胞数显著低于MAR小鼠(文献未明确提供样本量,p<0.05),但疾病的核心表型与MAR小鼠一致,均为B系ALL,细胞表达B220、CD19、CD43等B细胞早期标志物,脾脏和肝脏出现肿大,肿瘤细胞浸润模式无明显差异,说明SphK2缺失主要影响ALL的发生起始环节,而非疾病进展过程。
4. Biomarker研究及发现成果
本文中涉及的Biomarker为鞘氨醇激酶2(SphK2),属于分子型Biomarker,其筛选与验证逻辑为通过基因工程小鼠模型,在ARF缺失诱导的BCR/ABL非依赖性ALL模型中,验证SphK2对疾病发生的调控作用,形成“通路关联→模型验证→功能确认”的完整逻辑链条。
该Biomarker来源于鞘脂代谢调控通路,验证方法包括基因工程小鼠构建、生存分析、流式细胞术表型分析、组织学检查等多维度实验。特异性与敏感性数据方面,SphK2缺失可使ALL发生率从61%降至43%(文献未明确提供样本量,p=0.044),中位生存时间从193天延长至234天(文献未明确提供样本量,p<0.05),具有显著的统计学差异,表明SphK2对BCR/ABL非依赖性ALL的发生具有特异性调控作用。
核心成果提炼:SphK2作为BCR/ABL非依赖性ALL的促癌分子,其缺失可显著降低疾病的发生风险,首次明确了SphK2在非BCR/ABL驱动的ALL中的功能,为SphK2抑制剂在这类ALL中的临床应用提供了实验依据,拓展了SphK2靶向治疗的适用范围。该Biomarker的功能关联为调控ALL的发生起始环节,而非疾病进展,创新性在于填补了BCR/ABL非依赖性ALL中SphK2功能研究的空白,为ALL的精准靶向治疗提供了新的方向,具有重要的临床转化潜力。
