1. 领域背景与文献引入
文献英文标题:Epigenetic dysregulation of steroidogenesis and neuroactive steroid deficiency in premature ovarian insufficiency: implications for neurodegenerative risk;发表期刊:Biomarker Research;影响因子:未公开;研究领域:生殖内分泌与神经退行性疾病交叉领域
早发性卵巢功能不全(POI)是指女性在40岁前出现卵巢功能丧失的生殖内分泌疾病,临床特征包括闭经、促性腺激素水平升高及卵巢储备标志物降低,不仅直接影响生育功能,还会对骨健康、心血管系统及神经认知功能产生长期不良影响。领域共识:近年来的流行病学研究显示,POI患者发生痴呆等神经退行性疾病的风险显著高于同龄女性,神经影像学证据也证实POI患者存在脑结构的异常改变,但目前连接POI与神经退行性风险的具体分子机制尚未明确。现有研究多聚焦于POI的内分泌替代治疗或单一系统的病理改变,缺乏对表观遗传调控、胆固醇代谢与类固醇生成通路的整合分析,因此本研究旨在通过外周血白细胞甲基化组分析与循环类固醇激素定量,揭示POI患者中可能介导神经退行性风险升高的分子机制,为POI的神经并发症预防提供潜在靶点。
2. 文献综述解析
作者对POI领域现有研究的评述逻辑主要分为三个维度,一是POI的多系统临床影响,二是POI与神经退行性疾病的流行病学及影像学关联,三是现有机制研究的局限性。
现有研究已明确POI会对女性的生殖、骨、心血管及神经健康造成损害,其中神经认知方面的影响表现为痴呆风险升高及脑结构改变,部分研究通过神经影像学技术观察到POI患者存在脑灰质体积减少、白质完整性下降等异常,但这些研究仅停留在临床现象的关联层面,未深入解析背后的分子调控机制。同时,现有关于POI内分泌改变的研究多集中于性激素水平的检测,缺乏对胆固醇代谢、类固醇生成通路及神经保护类固醇的系统分析,也未涉及表观遗传调控在其中的作用。本研究的创新价值在于首次将表观遗传组学与循环类固醇代谢组学结合,针对POI与神经退行性风险的机制空白,通过筛选差异甲基化基因与验证类固醇激素水平,构建了“表观遗传失调→胆固醇代谢异常→类固醇生成抑制→神经保护类固醇缺乏→神经退行性风险升高”的完整机制链条,填补了领域内的研究空白。
3. 研究思路总结与详细解析
本研究的整体研究目标是揭示早发性卵巢功能不全(POI)与神经退行性风险升高的分子机制,核心科学问题为POI中表观遗传失调如何调控胆固醇代谢与类固醇生成通路,进而影响神经保护类固醇的水平,技术路线遵循“队列构建→组学分析→差异筛选→功能验证→机制推论”的闭环逻辑。
3.1 研究队列构建与基线特征验证
实验目的是建立年龄匹配的POI患者与健康对照队列,验证POI的临床内分泌特征,确保队列的可比性。方法细节为研究共纳入50例POI患者与50例年龄匹配的健康对照,进一步分为两个独立队列,队列1包含20例POI患者与20例对照,用于DNA甲基化组分析;队列2包含30例POI患者与30例对照,用于循环类固醇激素定量检测,所有POI患者均符合统一的临床诊断标准。结果解读显示,POI患者的血浆促卵泡激素(FSH)、黄体生成素(LH)水平显著升高,而卵巢储备标志物雌二醇(E₂)、抗缪勒管激素(AMH)水平显著降低(n=50,P<0.05,文献未明确具体P值),符合POI的典型内分泌特征,验证了队列的可靠性。产品关联:文献未提及具体实验产品,领域常规使用化学发光免疫分析试剂盒检测血浆内分泌激素。
3.2 外周血白细胞甲基化组分析
实验目的是筛选POI患者与对照之间的差异甲基化基因与功能通路,寻找可能介导POI病理改变的表观遗传标志物。方法细节为对队列1的样本进行全基因组DNA甲基化芯片检测,在分析前先校正芯片批次效应,同时保留年龄作为协变量以排除年龄相关甲基化改变的干扰,随后进行主成分分析(PCA)、差异探针筛选、功能富集分析(KEGG、基因集富集分析GSEA),并通过Boruta算法与随机森林分析筛选具有诊断价值的关键甲基化探针。结果解读显示,PCA分析发现主成分2(PC2,解释4.9%方差)与主成分3(PC3,解释3.8%方差)与病例-对照状态显著相关,可清晰区分POI患者与对照;筛选得到2747个差异甲基化探针,其中大部分位于CpG岛区域,且POI患者的启动子相关区域呈现低甲基化趋势;功能富集分析显示差异甲基化基因富集于免疫代谢相关通路,其中SOAT1基因启动子区域的探针cg16074884在POI患者中呈现显著低甲基化(n=20,P<0.001);GSEA分析显示类固醇激素生物合成通路的启动子区域呈现高甲基化,提示该通路在POI患者中被抑制。
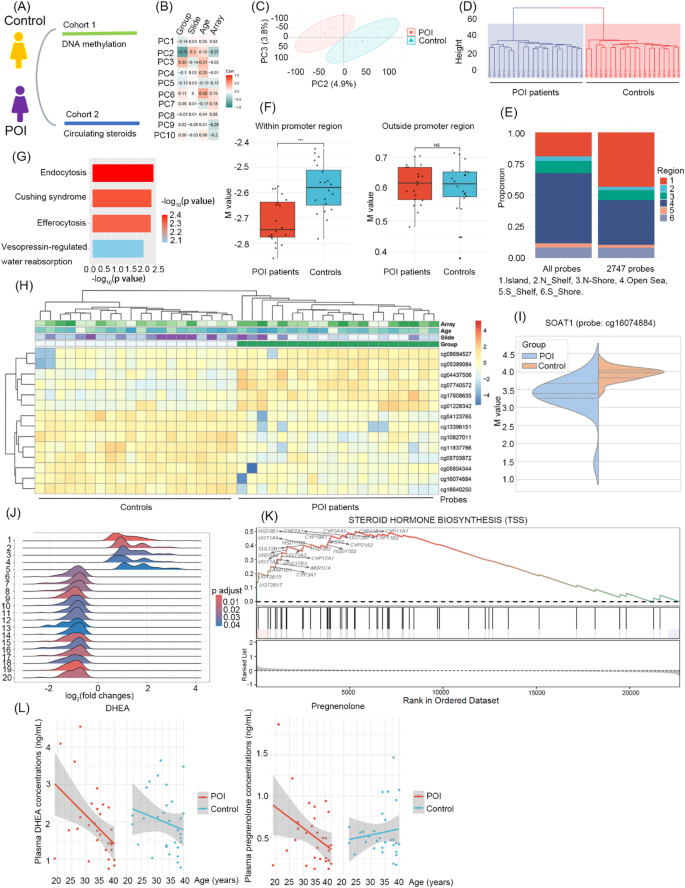
产品关联:文献未提及具体实验产品,领域常规使用Illumina甲基化芯片进行全基因组甲基化分析。
3.3 循环类固醇激素定量与关联分析
实验目的是验证甲基化组分析提示的类固醇生成通路改变,分析神经保护类固醇的水平变化及其与年龄的相关性,明确POI患者中类固醇代谢的异常特征。方法细节为对队列2的样本采用定量分析技术检测18种循环类固醇激素的水平,进行年龄校正后的组间比较,并通过Pearson相关分析评估年龄与神经保护类固醇脱氢表雄酮(DHEA)、孕烯醇酮水平的相关性。结果解读显示,POI患者的循环雄烯二酮、DHEA、醛固酮、皮质醇、可的松水平显著降低(n=30,P<0.05),而18-羟皮质酮水平略有升高;值得注意的是,仅在POI组中,DHEA与孕烯醇酮的水平随年龄增长呈现显著下降趋势(DHEA:R=-0.48,P=0.0073;孕烯醇酮:R=-0.39,P=0.033),而对照组中未观察到这种年龄相关性。产品关联:文献未提及具体实验产品,领域常规使用液相色谱-串联质谱(LC-MS/MS)定量循环类固醇激素。
4. Biomarker研究及发现成果解析
本研究发现的Biomarker包括表观遗传标志物SOAT1启动子低甲基化,以及循环类固醇激素标志物DHEA、孕烯醇酮,这些标志物通过“表观遗传调控→代谢通路→神经保护功能”的链条,共同介导POI患者的神经退行性风险升高。
Biomarker的筛选与验证逻辑为,SOAT1启动子低甲基化通过全基因组甲基化组分析筛选得到,经探针特异性验证与功能富集分析确认其与胆固醇代谢、类固醇生成通路的关联;DHEA、孕烯醇酮通过循环类固醇激素定量分析发现,经年龄相关性分析验证其在POI患者中的特异性改变。SOAT1启动子低甲基化的检测样本为外周血白细胞,通过甲基化芯片检测,结果显示POI患者中SOAT1启动子区域的甲基化水平显著低于对照(n=20,P<0.001);DHEA、孕烯醇酮的检测样本为外周血血浆,通过定量分析技术检测,POI患者中两者的水平显著降低,且仅在POI组中随年龄下降(n=30,P值分别为0.0073和0.033)。核心成果方面,SOAT1介导的胆固醇代谢异常会导致类固醇生成通路抑制,进而引起神经保护类固醇DHEA、孕烯醇酮的缺乏,而DHEA和孕烯醇酮具有抗氧化、抗炎、促进神经元存活等神经保护功能,其缺乏会加重神经退行性风险;本研究首次发现POI患者中SOAT1的表观遗传失调与神经保护类固醇的年龄依赖性下降,为POI相关神经退行性风险的机制研究提供了新的方向,同时这些Biomarker也有望成为POI患者神经退行性风险的预测指标,但目前尚未经过纵向临床研究的验证。推测:未来通过靶向SOAT1或补充神经保护类固醇,可能为降低POI患者的神经退行性风险提供新的治疗策略。
