1. 领域背景与文献引入
文献英文标题:The role of kinesin family members in hepatobiliary carcinomas: from bench to bedside;发表期刊:Biomark Res;影响因子:未公开;研究领域:肝胆肿瘤学、肿瘤分子生物学。
肝胆癌是消化系统高发恶性肿瘤,主要包括肝细胞癌(HCC)、胆管癌(CCA)及胆囊癌(GBC),严重威胁全球公共健康。其中HCC占原发性肝癌的90%,5年生存率约18%,预计2025年全球病例将突破百万,是癌症相关死亡的第三大原因;CCA占胃肠道恶性肿瘤的3%,尽管诊断与治疗技术有所进步,5年生存率仍仅为7%-20%;GBC因早期临床表现不典型,早期诊断难度大,5年生存率不足5%,预后极差。驱动蛋白(KIFs)是依赖微管的分子马达蛋白,负责细胞内物质运输,在有丝分裂、减数分裂过程中维持细胞增殖与遗传稳态,其异常激活会破坏细胞分裂的正常进程,导致遗传不稳定与肿瘤发生。目前领域内已报道多个KIF家族成员在肝胆癌中异常表达,但缺乏对其作用机制、预后价值及临床应用的系统性整合分析,这篇综述通过全面梳理现有研究,填补了这一空白,为肝胆癌的分子机制研究与临床转化提供了系统性参考。
2. 文献综述解析
本文采用“家族概况-分癌种机制-预后价值-靶向治疗”的逻辑框架,系统性综述了驱动蛋白家族成员在肝胆癌中的研究进展。作者首先明确驱动蛋白家族的分类、结构与基础功能,为后续阐述其肿瘤调控作用奠定理论基础;随后分别聚焦HCC、胆管癌(CCA与GBC),按驱动蛋白家族亚类逐一解析不同成员的致癌/抑癌作用及调控通路;接着整合临床研究数据,总结KIF成员在肝胆癌预后评估中的价值;最后梳理KIF靶向抑制剂的研究进展,搭建从基础研究到临床应用的桥梁。
现有研究已证实多个KIF家族成员在HCC中发挥关键调控作用,部分成员通过参与Akt、WNT/β-catenin等核心信号通路促进肿瘤增殖、侵袭及化疗耐药,如KIF14介导索拉非尼耐药,KIF11调控WNT/β-catenin通路;同时也发现少数成员具有抑癌功能,如KIF1B的单核苷酸多态性可降低HCC发病风险。现有研究的优势在于揭示了KIF成员与肿瘤关键信号通路的关联,为分子靶向治疗提供了潜在靶点,但局限性在于对胆管癌中KIF的研究较为匮乏,机制探索深度不足,且多数研究停留在细胞与动物模型阶段,临床转化的直接证据有限。本文的创新价值在于首次系统性整合了所有已报道的KIF家族成员在肝胆癌中的作用,明确了不同成员的功能异质性,同时梳理了KIF靶向抑制剂的研究现状,为后续的机制研究与临床转化提供了全面的参考框架。
3. 研究思路总结与详细解析
本文以系统性综述为核心研究方法,整体框架遵循“基础理论-癌种特异性机制-临床预后价值-靶向治疗进展”的逻辑链条,全面整合驱动蛋白家族在肝胆癌中的研究成果,为领域内研究提供系统性总结与未来方向指引。
3.1 驱动蛋白家族整体概况解析
实验目的是明确驱动蛋白家族的分类、结构特征与生物学功能,为后续阐述其在肿瘤中的调控作用奠定基础。方法为系统梳理已发表的驱动蛋白基础研究文献,整合家族分类、结构域功能及生理作用的核心信息。结果解读:驱动蛋白家族共包含45个成员,分为14个亚家族,结构上由头部马达结构域、颈部、杆状区及尾部结构域组成,头部结构域具有ATP结合与微管结合位点,为分子马达运动提供能量;根据头部结构域的位置可分为N-KIFs(介导微管正极方向运输)、C-KIFs(介导微管负极方向运输)、M-KIFs(介导微管解聚)。生理状态下,驱动蛋白参与细胞内细胞器运输、染色体分离等关键过程,维持细胞增殖与遗传稳态,其功能异常会导致纺锤体组装缺陷、染色体非整倍体等,进而诱发肿瘤发生。
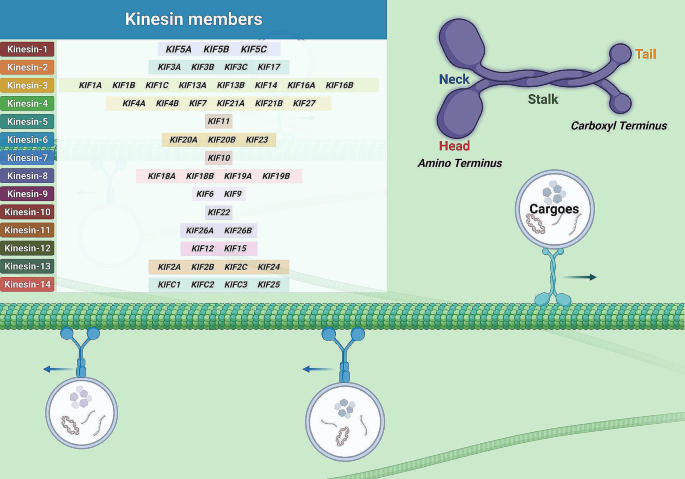
文献未提及具体实验产品,领域常规使用蛋白结构分析软件、免疫荧光染色试剂、微管结合实验试剂等研究驱动蛋白的结构与功能。
3.2 驱动蛋白家族成员在HCC中的作用机制解析
实验目的是系统总结不同驱动蛋白家族成员在HCC中的致癌/抑癌作用及调控通路,明确其功能异质性。方法为检索并整合所有关于KIF与HCC的研究文献,按驱动蛋白亚家族分类逐一阐述其作用机制。结果解读:多个KIF亚家族成员通过调控核心信号通路促进HCC进展,如驱动蛋白-2家族的KIF3B通过激活Akt通路促进肿瘤细胞增殖、抑制凋亡;驱动蛋白-3家族的KIF14通过与ETS1形成Akt通路正反馈环路,介导HCC细胞对索拉非尼的耐药性,沉默KIF14可显著增强肿瘤细胞对索拉非尼的敏感性;驱动蛋白-5家族的KIF11通过与ASPM形成复合物调控WNT/β-catenin通路,促进肿瘤细胞的侵袭与转移。同时部分KIF成员具有抑癌作用,如驱动蛋白-3家族的KIF1B单核苷酸多态性(rs17401966)可降低HBV相关HCC的发病风险,驱动蛋白-7家族的KIF10(CENP-E)在HCC组织中低表达,其表达水平与患者不良预后相关。不同KIF成员的功能存在显著异质性,同一信号通路(如Akt)可被多个KIF成员调控,形成复杂的调控网络。
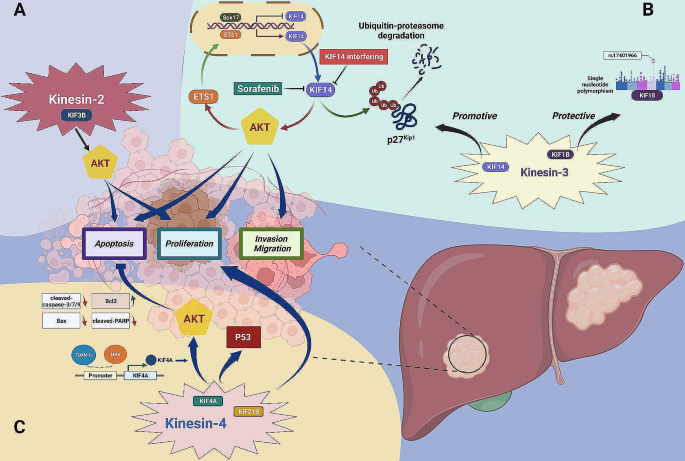
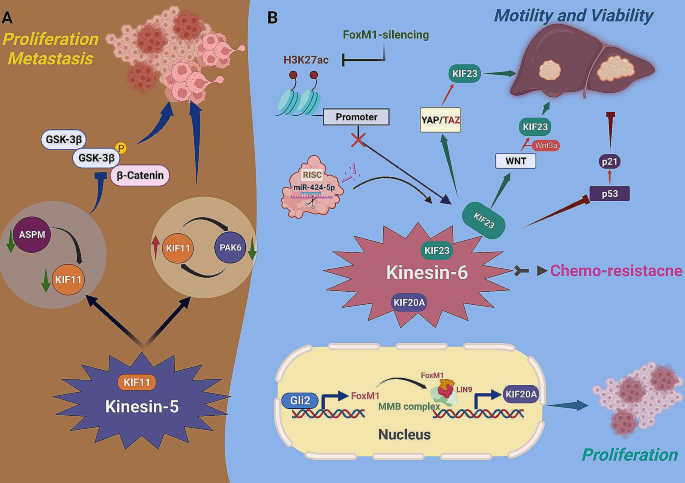
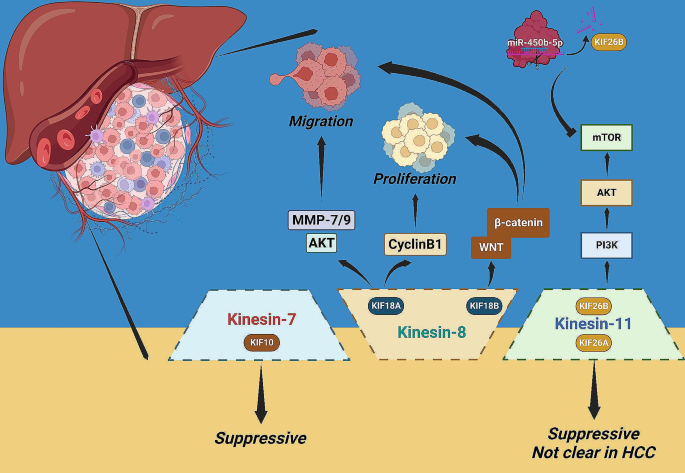
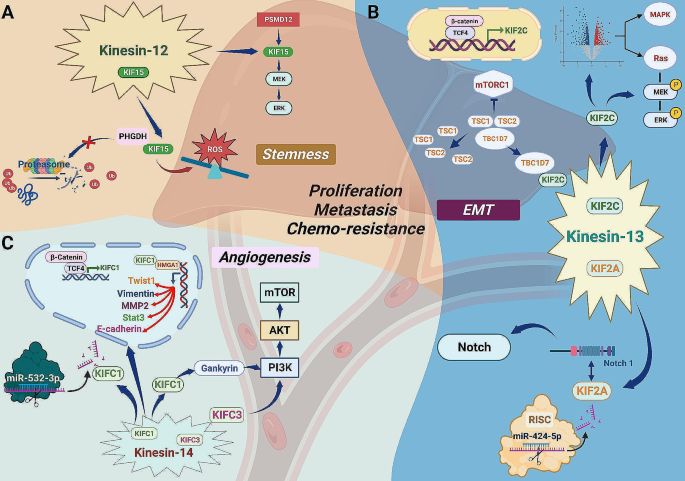
文献未提及具体实验产品,领域常规使用CRISPR基因编辑系统、HCC细胞系模型、裸鼠异种移植模型及信号通路检测试剂盒等开展相关研究。
3.3 驱动蛋白家族成员在胆管癌中的作用机制解析
实验目的是梳理驱动蛋白家族成员在CCA与GBC中的作用,明确胆管癌中KIF研究的现状与不足。方法为检索并整合已发表的KIF与胆管癌相关研究文献,总结有限的研究数据。结果解读:CCA中仅驱动蛋白-3家族的KIF1Bβ被报道为抑癌因子,通过USP9X/EGLN3信号通路诱导肿瘤细胞凋亡;GBC中驱动蛋白-5家族的KIF11通过激活ERBB2/PI3K/Akt通路促进肿瘤细胞增殖,其表达水平受组蛋白H3K27ac乙酰化修饰调控,使用组蛋白去乙酰化酶抑制剂可降低KIF11的表达;驱动蛋白-12家族的KIF15通过PI3K/Akt通路促进GBC细胞的增殖与迁移,沉默KIF15可显著抑制肿瘤生长。整体来看,胆管癌中KIF的研究较为匮乏,多数成员的作用及调控机制尚未被探索,研究深度远不及HCC。
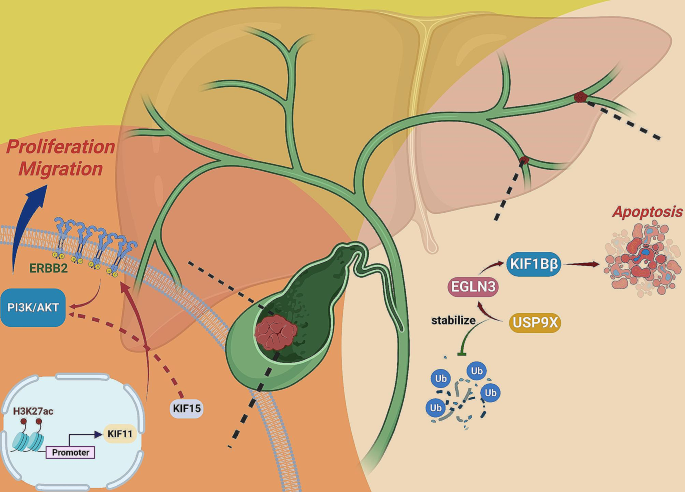
文献未提及具体实验产品,领域常规使用临床肿瘤样本分析、胆管癌细胞系模型及表观遗传修饰检测试剂等开展相关研究。
3.4 驱动蛋白家族成员的预后价值分析
实验目的是总结驱动蛋白家族成员在肝胆癌预后评估中的临床价值,明确其作为预后标志物的潜力。方法为整合已发表的临床研究数据,分析KIF成员表达水平与患者生存结局的关联。结果解读:HCC中多个KIF成员的表达水平与患者预后密切相关,如KIFC1在82例HCC样本中高表达与患者不良总生存期(OS)、无复发生存期(RFS)相关,在168例样本中进一步验证其与不良OS、无病生存期(DFS)及肿瘤进展相关;KIF11在108例HCC样本中表达水平升高8.3倍,高表达组中位OS为57.7个月,低表达组为155.6个月;KIF18A在216例HCC样本中高表达与不良OS、DFS相关,低表达组平均OS为55.06个月,高表达组为39.26个月。CCA中KIF4A高表达与患者不良OS相关,KIF18A在动物模型中被发现是潜在的早期诊断标志物;GBC中相关研究数据有限,尚未明确KIF成员的预后价值。
文献未提及具体实验产品,领域常规使用免疫组化(IHC)、实时荧光定量PCR(qRT-PCR)、Western blotting等技术检测临床样本中KIF成员的表达水平。
3.5 驱动蛋白靶向抑制剂的研究进展解析
实验目的是综述驱动蛋白靶向抑制剂在肿瘤治疗中的研究进展,明确其在肝胆癌中的临床应用潜力。方法为检索并整合KIF靶向抑制剂的基础与临床研究文献,总结其作用机制与研究现状。结果解读:目前研究最深入的是驱动蛋白-5家族的KIF11(Eg5)抑制剂,如Monastrol、Ispinesib等,通过抑制纺锤体组装诱导细胞周期阻滞,部分抑制剂已进入临床试验阶段,其中SB-743921在CCA细胞系及患者来源异种移植(PDX)模型中显示出显著的抗肿瘤活性;驱动蛋白-7家族的KIF10(CENP-E)抑制剂GSK923295在HCC的PDX模型中表现出抗肿瘤作用;此外还有KIF15抑制剂KIF15-IN-1、KIF2C抑制剂等处于临床前研究阶段。但肝胆癌中KIF靶向抑制剂的临床转化证据有限,仅SB-715992(KIF11抑制剂)开展了HCC的II期临床试验,未显示出单药治疗的优势,仍需进一步探索联合治疗方案。
实验所用关键产品:KIF11抑制剂Monastrol、SB-743921,CENP-E抑制剂GSK923295等。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker主要为不同驱动蛋白家族成员,筛选与验证逻辑为“细胞/动物模型发现异常表达→临床样本验证表达与预后的关联→部分成员探索调控机制”,形成了从基础到临床的完整验证链条。
这些Biomarker属于分子标志物(蛋白/RNA),涵盖促癌标志物与抑癌标志物两类,促癌标志物包括KIFC1、KIF14、KIF11、KIF4A等,抑癌标志物包括KIF1B、KIF10等。研究过程中,Biomarker的来源主要为临床肿瘤组织样本,部分为血液样本(如CCA中KIF18A在血浆中升高);验证方法包括免疫组化(IHC)、实时荧光定量PCR(qRT-PCR)、Western blotting等,其中IHC是临床样本中蛋白表达检测的主要方法;特异性与敏感性数据方面,HCC中KIF11在108例样本中表达升高8.3倍,高表达组与低表达组OS差异显著;KIF18A在216例样本中高表达与不良OS、DFS相关,低表达组平均OS较表达组高15.8个月。
核心成果方面,多个KIF成员可作为肝胆癌的独立预后标志物,如KIFC1、KIF2C、KIF4A等在HCC中高表达提示不良预后;部分成员可预测化疗耐药,如KIF14高表达提示HCC患者对索拉非尼耐药;创新性在于首次系统性总结了所有已报道的KIF成员作为肝胆癌Biomarker的证据,明确了其临床应用潜力。统计学结果显示,多数KIF成员的表达与患者生存结局的关联具有统计学意义,如KIF11在108例HCC样本中高表达与不良OS相关(P<0.05,文献未明确具体数值),KIFC1在82例样本中高表达与不良OS、RFS相关(文献未明确P值)。
