1. 领域背景与文献引入
文献英文标题:Transcriptomic analysis of transformed small-cell lung cancer from EGFR-mutated lung adenocarcinoma reveals distinct subgroups and precision therapy opportunities;发表期刊:Biomark Res;影响因子:未公开;研究领域:肺癌转化医学、肿瘤分子分型与精准治疗
表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)是EGFR突变非小细胞肺癌(NSCLC)的一线标准治疗方案,可显著延长患者生存期,但多数患者在治疗12-20个月后会出现获得性耐药。小细胞肺癌(SCLC)转化是EGFR-TKI耐药的重要机制之一,发生率为3%-14%,其本质是肺腺癌细胞获得SCLC谱系表型的谱系可塑性过程,目前具体转化机制尚未完全明确,已知RB1和TP53失活可促进该转化过程。
目前针对转化型SCLC(T-SCLC)的治疗主要沿用原发SCLC的铂类化疗方案,但疗效有限,既往回顾性研究显示患者中位无进展生存期(mPFS)仅为3.4个月,且缺乏基于分子特征的精准治疗策略。现有研究虽发现T-SCLC多数保留原EGFR突变但对EGFR-TKI不敏感,且存在一定异质性,但尚未明确其分子亚型分类及对应的亚型特异性治疗方案,也缺乏基于分子亚型的生存获益数据。因此,本研究通过多组学分析明确T-SCLC与肺腺癌(LUAD)、原发SCLC的分子差异,鉴定T-SCLC的分子亚型,并探索基于亚型的精准治疗策略,为T-SCLC的临床治疗提供新的依据。
2. 文献综述解析
作者对领域内现有研究的分类维度主要包括疾病发展阶段(EGFR-TKI耐药前LUAD、T-SCLC、原发SCLC)和治疗反应(化疗敏感/不敏感)。现有研究的关键结论包括:EGFR-TKI耐药后SCLC转化与RB1、TP53基因失活密切相关;T-SCLC对铂类化疗有一定客观反应但长期疗效不佳;多数T-SCLC保留原EGFR突变但对EGFR-TKI治疗不敏感。技术方法优势方面,既往回顾性研究通过临床数据验证了铂类化疗在T-SCLC中的初步疗效,转录组分析揭示了T-SCLC的神经内分泌特征,为其病理诊断提供了分子依据。但现有研究存在明显局限性:样本量普遍较小,缺乏多组学综合分析;未明确T-SCLC的分子亚型分类及亚型特异性治疗靶点;没有基于分子亚型的治疗生存获益数据,无法为临床精准治疗提供指导。
本研究的创新价值在于,首次通过转录组测序结合基因组、蛋白质组多组学分析,将T-SCLC分为LUAD样和非LUAD样两个明确的分子亚型;首次提出基于分子亚型的匹配治疗策略,并通过生存分析证实匹配治疗可显著延长患者mPFS;同时明确了T-SCLC与LUAD、原发SCLC的独特分子特征,弥补了现有研究在T-SCLC分子分型及精准治疗领域的空白。
3. 研究思路总结与详细解析
本研究的整体框架为:以明确T-SCLC的分子特征、鉴定分子亚型并探索亚型特异性治疗方案为核心目标,围绕“T-SCLC与LUAD、原发SCLC的分子差异”及“分子亚型与治疗反应的关联”两个核心科学问题,采用“回顾性样本收集→多组学检测→生物信息学分析→分子分型→生存分析验证”的闭环技术路线,最终明确了T-SCLC的分子亚型及对应的精准治疗策略。
3.1 临床样本收集与病理诊断
实验目的:获取符合纳入标准的LUAD、T-SCLC、原发SCLC临床样本,明确病理诊断及患者临床特征。
方法细节:回顾性收集2018年10月至2021年9月广东省人民医院的61例患者样本,包括18例LUAD、23例T-SCLC、20例原发SCLC,其中5例为SCLC转化前后的配对样本。纳入标准为:基线病理诊断为EGFR突变LUAD,接受EGFR-TKI治疗后出现获得性耐药,再活检证实为SCLC,且有足够样本用于检测;排除初始诊断为混合病理的患者。采用苏木精-伊红(H&E)染色和免疫组化(IHC)进行病理诊断,T-SCLC的诊断指标包括突触素(Syn)、嗜铬粒蛋白A(CgA)、CD56,LUAD的诊断指标包括TTF-1、CK7、NapsinA,由两名独立病理学家进行IHC结果评估。
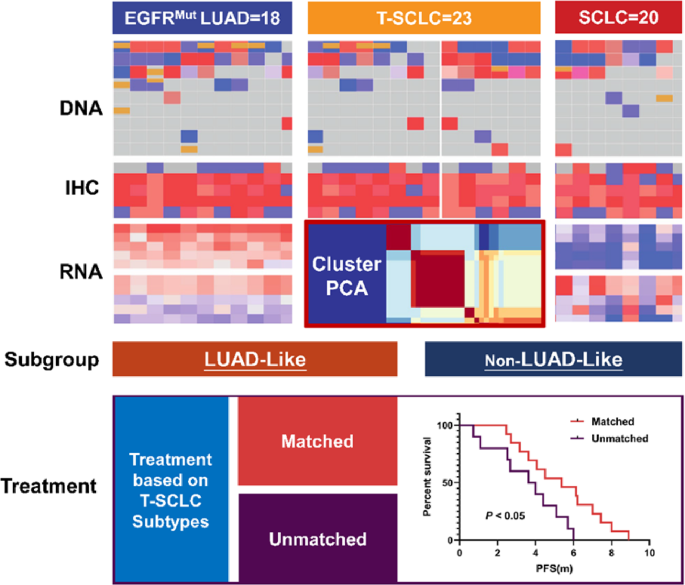
结果解读:患者临床特征分析显示,T-SCLC组78.3%为非吸烟者,而原发SCLC组65%为重度吸烟者;T-SCLC组多数保留原EGFR突变,其中19del突变占73.9%,L858R突变占26.1%。免疫组化结果证实T-SCLC样本高表达神经内分泌标志物,LUAD样本高表达肺腺癌特异性标志物,明确了三组样本的病理特征。
产品关联:实验所用关键产品:天根生化的RNAprep Pure FFPE Kit、TIANamp Genomic DNA kit;Illumina、Geneplus测序平台。
3.2 多组学检测与生物信息学分析
实验目的:检测三组样本的基因组、转录组、蛋白质组特征,分析T-SCLC与LUAD、原发SCLC的分子差异,鉴定T-SCLC的分子亚型。
方法细节:采用靶向捕获测序(覆盖至少139个肺癌相关基因)或扩增阻滞突变系统(ARMS)法检测基因组变异;采用RNA测序(RNA-seq)进行转录组分析,使用TIANSeq rRNA Depletion Kit去除rRNA,Agilent 2100生物分析仪验证RNA质量,STAR软件将测序reads比对到hg19参考基因组;采用免疫组化检测蛋白质表达水平。生物信息学分析包括:采用DESeq2鉴定差异表达基因(DEGs),clusterProfiler进行KEGG通路富集分析,GSEA分析基因集富集情况,pheatmap包进行层次聚类分析。
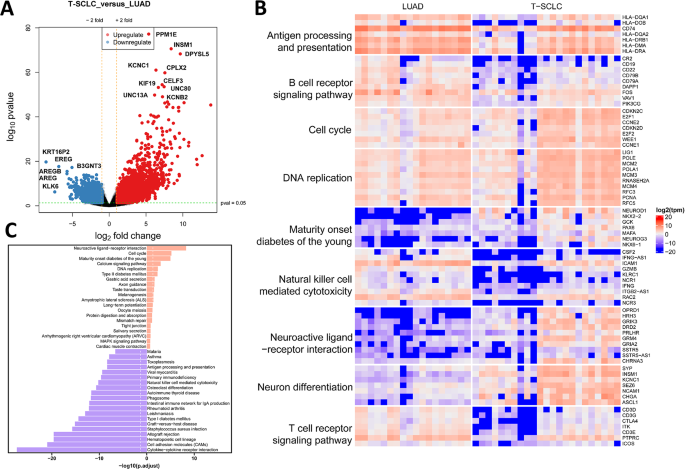
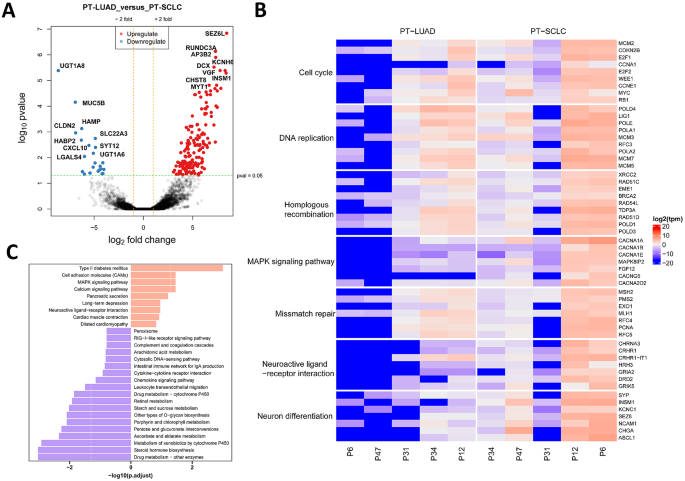
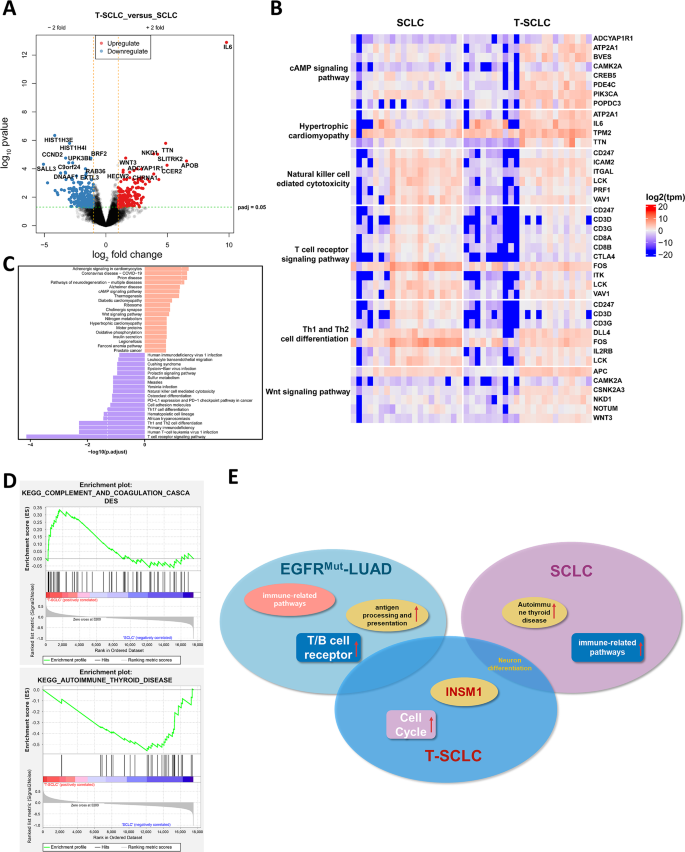
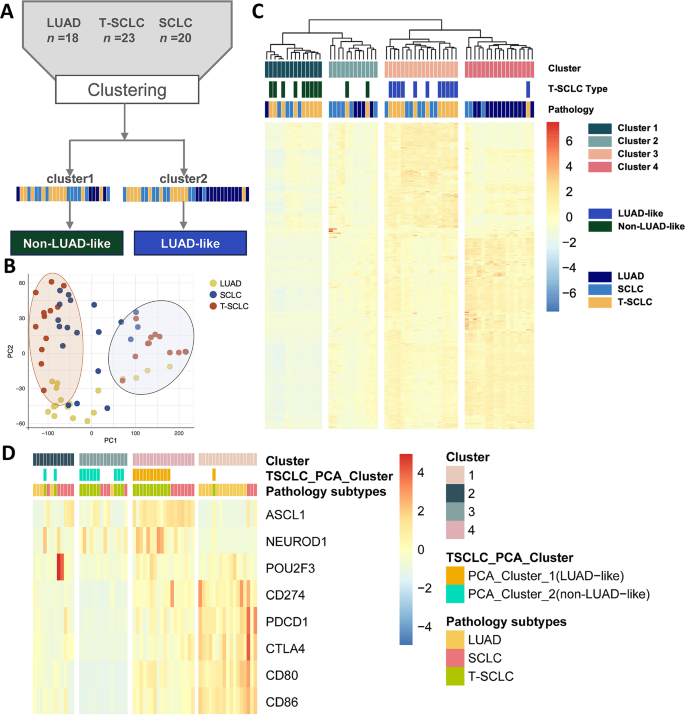
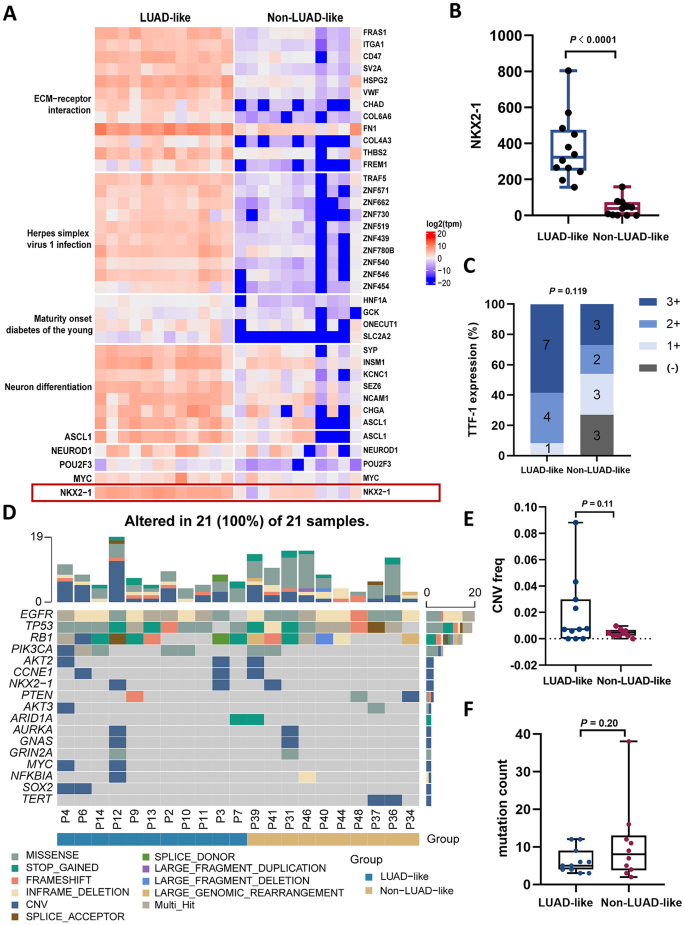
结果解读:转录组分析显示,T-SCLC与LUAD相比共有7499个DEGs,其中4899个基因显著上调,2600个基因显著下调;上调基因主要富集于细胞周期、神经分化通路,包括INSM1、PPM1E、KCNC1等神经内分泌标志物。与原发SCLC相比,T-SCLC有499个DEGs,差异通路主要涉及自身免疫性甲状腺疾病、补体和凝血级联反应。层次聚类分析将23例T-SCLC样本分为LUAD样(n=12)和非LUAD样(n=11)两个亚型,其中LUAD样亚型的NKX2-1(TTF-1编码基因)表达水平显著高于非LUAD样亚型(均值371.8 vs 41.8,P<0.0001)。基因组分析显示,95.2%的T-SCLC样本保留原EGFR突变,高频突变基因为EGFR、TP53、RB1、PIK3CA。
产品关联:实验所用关键产品:天根生化的TIANSeq rRNA Depletion Kit;Agilent 2100生物分析仪;R软件的pheatmap、clusterProfiler包。
3.3 基于分子亚型的治疗分组与生存分析
实验目的:验证基于T-SCLC分子亚型的匹配治疗策略对患者生存的影响,明确亚型特异性治疗方案。
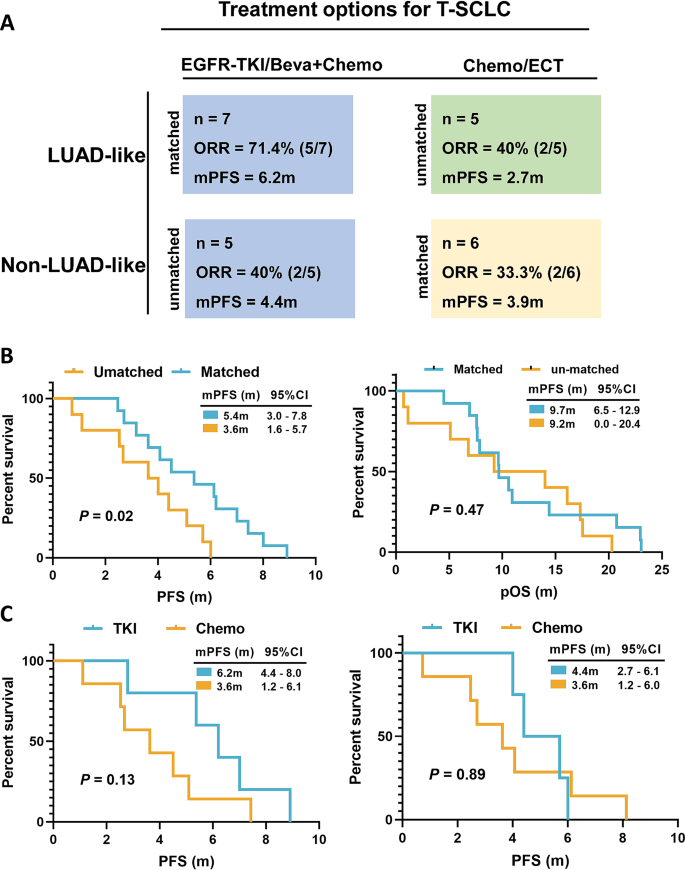
方法细节:根据分子亚型与治疗方案的匹配情况,将23例T-SCLC患者分为匹配组和不匹配组。匹配组定义为:LUAD样亚型患者接受EGFR-TKI或贝伐珠单抗联合化疗,非LUAD样亚型患者接受铂类化疗±免疫治疗;不匹配组为治疗方案与分子亚型不匹配的患者。采用Kaplan-Meier法绘制生存曲线,log-rank检验比较两组的无进展生存期(PFS)和总生存期(OS)差异。
结果解读:匹配组共13例患者,不匹配组共10例患者。生存分析显示,匹配组的mPFS显著长于不匹配组(5.4个月 vs 3.6个月,P=0.02),但两组OS无显著差异(9.7个月 vs 9.2个月,P=0.47)。进一步亚组分析显示,LUAD样亚型患者接受EGFR-TKI/贝伐珠单抗联合化疗的客观缓解率(ORR)为71.4%,mPFS为6.2个月,显著优于接受其他治疗的患者(ORR 40%,mPFS 2.7个月);而非LUAD样亚型患者继续使用EGFR-TKI治疗无临床获益(mPFS 4.4个月 vs 3.6个月,P=0.89)。
产品关联:文献未提及具体实验产品,领域常规使用GraphPad Prism、R软件进行生存分析与可视化。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究涉及的Biomarker主要包括分子亚型标志物NKX2-1(TTF-1)、神经内分泌转化标志物INSM1,以及治疗反应相关的EGFR突变。筛选与验证逻辑为:首先通过转录组测序筛选T-SCLC与LUAD、原发SCLC的差异表达基因,然后通过层次聚类分析鉴定出区分T-SCLC分子亚型的核心标志物NKX2-1;通过转录组测序和免疫组化验证神经内分泌标志物INSM1的表达;通过基因组测序验证EGFR突变的保留情况;最后通过生存分析验证这些Biomarker与治疗反应的关联,形成完整的筛选-验证-临床应用逻辑链条。
研究过程详述
NKX2-1来源于T-SCLC患者的肿瘤组织样本,通过RNA-seq检测其转录表达水平,结果显示LUAD样亚型的NKX2-1表达均值为371.8,非LUAD样亚型为41.8(P<0.0001);通过免疫组化检测其编码蛋白TTF-1的表达,LUAD样亚型的IHC评分更高,但因样本量限制未达到统计学差异(P=0.119)。INSM1通过RNA-seq检测,结果显示其在T-SCLC样本中显著上调,是SCLC转化的关键神经内分泌标志物。EGFR突变通过靶向捕获测序或ARMS法检测,95.2%的T-SCLC样本保留原EGFR突变。治疗反应方面,匹配组患者的mPFS为5.4个月(n=13,P=0.02),显著长于不匹配组,提示基于Biomarker的匹配治疗可显著改善患者生存。
核心成果提炼
NKX2-1可作为T-SCLC的分子亚型特异性Biomarker,有效区分LUAD样和非LUAD样亚型,其中LUAD样亚型患者接受EGFR-TKI或贝伐珠单抗联合化疗的mPFS为6.2个月(n=7,P=0.13),生存获益显著;INSM1作为神经内分泌转化的Biomarker,其上调与T-SCLC的发生发展密切相关,可作为潜在的治疗靶点;EGFR突变虽在T-SCLC中高比例保留,但仅LUAD样亚型患者可从EGFR-TKI治疗中获益,提示EGFR突变可作为LUAD样亚型患者的治疗反应预测Biomarker。本研究的创新性在于,首次在T-SCLC中鉴定出具有临床指导意义的分子亚型及对应Biomarker,首次证实基于Biomarker的匹配治疗可显著延长患者生存期,为T-SCLC的精准治疗提供了新的范式。
