1. 领域背景与文献引入
文献英文标题:scMET: Bayesian modeling of DNA methylation heterogeneity at single-cell resolution;发表期刊:Genome Biology;影响因子:13.583(2021年);研究领域:单细胞表观遗传学(单细胞DNA甲基化异质性分析)
DNA甲基化是调控基因表达、X染色体失活、基因组印记及肿瘤发生等生物学过程的关键表观遗传修饰(领域共识)。传统的全基因组亚硫酸氢盐测序技术可绘制组织水平的甲基化图谱,但无法解析细胞间的甲基化异质性,也难以量化其在不同生物学场景下的动态变化。近年来,测序技术的进步推动了单细胞亚硫酸氢盐测序技术的发展,多重测序方案更可在单次实验中分析数千个细胞的甲基化组。与单细胞转录组测序数据易受环境影响不同,DNA甲基化图谱在细胞类型间差异显著且在个体间及生命周期内保持稳定,同时对基因组区域的覆盖更完整。然而,由于初始基因组DNA量少及亚硫酸氢盐对核酸的破坏性,单细胞亚硫酸氢盐测序数据通常存在高噪声和极端稀疏性,80%-95%的CpG二核苷酸位点无法被检测到。现有计算工具如梅丽莎插补工具、深度CpG插补工具主要解决数据稀疏的插补问题,但难以有效区分技术偏差与真实的表观遗传变异;多数差异甲基化分析工具仅关注甲基化均值的变化,忽略了细胞间变异的差异,这限制了对细胞异质性驱动因素的解析。因此,开发能有效处理稀疏数据、区分技术与生物变异、同时分析甲基化均值和变异差异的计算框架具有重要学术价值,本研究提出的单细胞甲基化异质性贝叶斯模型正是针对这一核心需求而开发。
2. 文献综述解析
本文综述围绕单细胞DNA甲基化分析的技术进展与计算方法局限展开,作者按技术发展阶段和方法功能分类梳理现有研究,明确了当前领域的核心挑战与研究空白。
首先,作者回顾了全基因组亚硫酸氢盐测序技术的贡献与局限,指出其虽为甲基化组图谱绘制奠定了基础,但无法解析细胞间的甲基化异质性。接着介绍了单细胞亚硫酸氢盐测序及多重测序技术的进展,强调其在细胞分辨率甲基化分析中的优势,同时也指出数据稀疏和噪声是制约其应用的核心问题。随后,作者梳理了现有计算方法,包括插补类工具和差异分析类工具:插补类工具可缓解数据稀疏性,但无法区分技术变异与真实的生物异质性;差异分析类工具多仅关注甲基化均值的差异,无法解析细胞间变异的差异,也难以处理单细胞数据的高噪声特性。通过对比现有研究的不足,作者凸显了本研究的创新价值:采用贝叶斯分层框架整合跨细胞和基因组特征的信息,能稳健量化真实的细胞间甲基化变异,同时支持高变特征筛选和甲基化均值、变异的差异分析,填补了单细胞甲基化异质性分析中区分技术与生物变异、同时解析均值和变异差异的空白。
3. 研究思路总结与详细解析
本文的研究目标是开发并验证一种能有效处理单细胞亚硫酸氢盐测序数据稀疏性、区分技术与生物变异的计算框架,核心科学问题是如何通过统计建模解析单细胞DNA甲基化的真实异质性,技术路线为“模型构建→模拟数据验证→真实数据集验证(小鼠皮层、多组学发育数据)→结论”的闭环。
3.1 单细胞甲基化异质性贝叶斯模型构建与理论验证
实验目的:构建能处理单细胞亚硫酸氢盐测序数据稀疏性、区分技术与生物变异的贝叶斯分层模型。
方法细节:该模型采用分层贝塔-二项式模型结合广义线性模型框架,将输入数据聚合为基因组特征(滑动窗口或预注释区域),通过共享跨细胞和特征的信息解决数据稀疏性问题;广义线性模型框架引入特征特异性协变量(如CpG密度)解释不同特征间的均值甲基化差异,同时通过非线性回归捕获均值-过度离散趋势,推导残差过度离散参数以量化不受均值甲基化混淆的细胞间变异。采用变分贝叶斯和马尔可夫链蒙特卡罗方法实现模型参数推断,以R语言包形式实现工具开发。
结果解读:模型的概率示意图(图1)清晰展示了输入数据、模型参数与输出结果的逻辑关系,残差过度离散参数可有效区分技术变异与真实的生物变异,且模型可扩展至数千个细胞和基因组特征的分析。
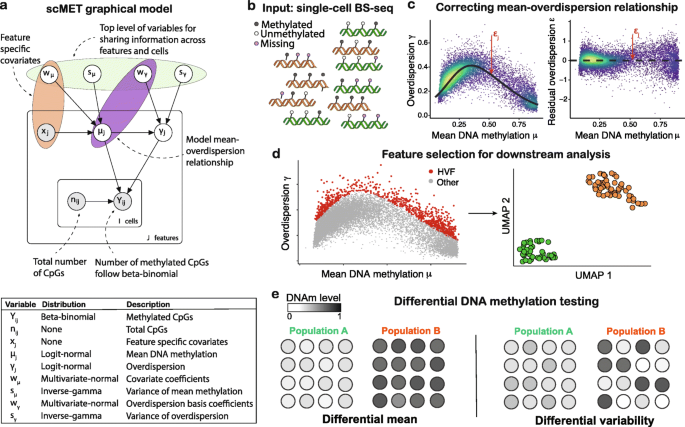
产品关联:文献未提及具体实验产品,领域常规使用R语言、斯坦概率编程框架等计算工具。
3.2 模拟数据基准测试
实验目的:验证单细胞甲基化异质性贝叶斯模型在参数推断、差异分析和高变特征筛选中的性能。
方法细节:模拟不同细胞数量(20-1000个)、不同CpG密度(丰富、中等、贫乏)的数据集,对比该模型与贝塔-二项式最大似然估计法、差异甲基化筛选工具、Fisher精确检验等方法的参数推断和差异分析性能;通过下采样实验(从424个抑制性神经元中随机采样20、50、100、200个细胞)验证模型的稳健性。
结果解读:该模型在过度离散参数推断上显著优于贝塔-二项式最大似然估计法,尤其是在细胞数量较少时;在差异均值甲基化分析上与现有方法性能相当,但在差异变异分析和高变特征筛选上具有显著优势,例如在小效应量的差异变异分析中,200个细胞可达到50%-80%的功效,50个细胞在大效应量时可达到80%功效。
产品关联:文献未提及具体实验产品,领域常规使用R语言、向量广义线性和加性模型包等统计工具进行模拟与分析。
3.3 小鼠额叶皮层单细胞甲基化数据集验证
实验目的:验证单细胞甲基化异质性贝叶斯模型在真实复杂数据集上的高变特征筛选和差异分析性能。
方法细节:使用包含3069个小鼠额叶皮层神经元的单细胞亚硫酸氢盐测序数据集,将基因组特征分为启动子、远端H3K27ac峰、H3K4me1峰三类,应用该模型筛选高变特征并进行聚类分析,对比不同高变特征选择方法(二项式方差、高斯方差、归一化离散度、随机选择)的聚类性能(调整兰德指数);同时进行差异甲基化(均值)和差异变异分析。
结果解读:该模型筛选的高变特征聚类性能最优,使用前4000个高变特征时,调整兰德指数接近0.8(图2),且高变特征富集已知神经元标记基因(如Gad1、Neurod6);差异分析显示抑制性神经元中高甲基化特征数量远多于兴奋性神经元(远端H3K27ac峰中分别为5242个和935个,n=3069,P<0.05,预期假发现率=5%),同时识别出大量差异变异特征,这些特征可区分神经元亚型内的异质性(图3)。
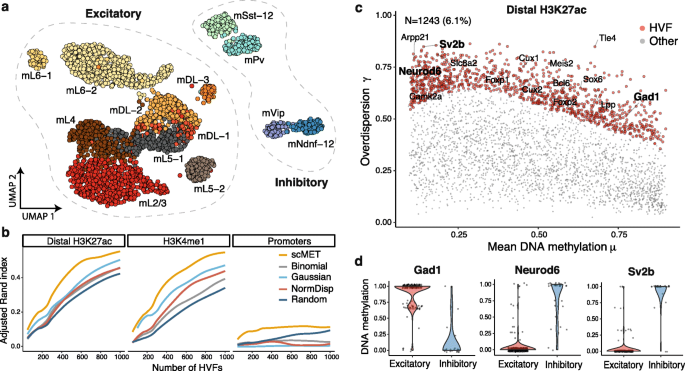
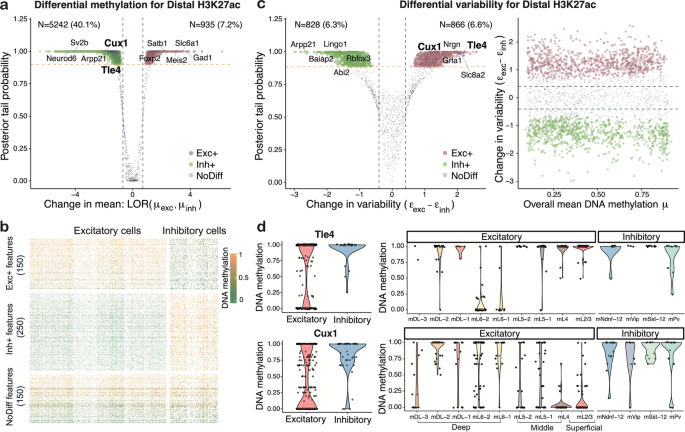
产品关联:文献未提及具体实验产品,领域常规使用多组学因子分析工具、均匀流形近似与投影等工具进行降维与聚类分析。
3.4 单细胞多组学数据集关联分析
实验目的:探究单细胞DNA甲基化变异与转录变异的关联模式。
方法细节:使用包含RNA表达、DNA甲基化和核小体占据的单细胞多组学测序数据集(覆盖小鼠胚胎发育E4.5至E7.5阶段),应用单细胞甲基化异质性贝叶斯模型计算启动子区域的甲基化残差过度离散参数,同时用单细胞转录组异质性贝叶斯模型计算RNA表达的残差过度离散参数,关联两者的异质性模式。
结果解读:基因组范围内甲基化变异与转录变异无显著关联,但高转录变异基因分为两类:一类是低甲基化变异的分化标记基因(如Mesp1、Lefty2),另一类是高甲基化变异的多能性标记基因(如Dppa5a、Zfp42)(图4),表明胚胎发育过程中存在两种不同的调控模式:多能性基因的下调与启动子高甲基化变异相关,而分化基因的上调与甲基化变异无关。
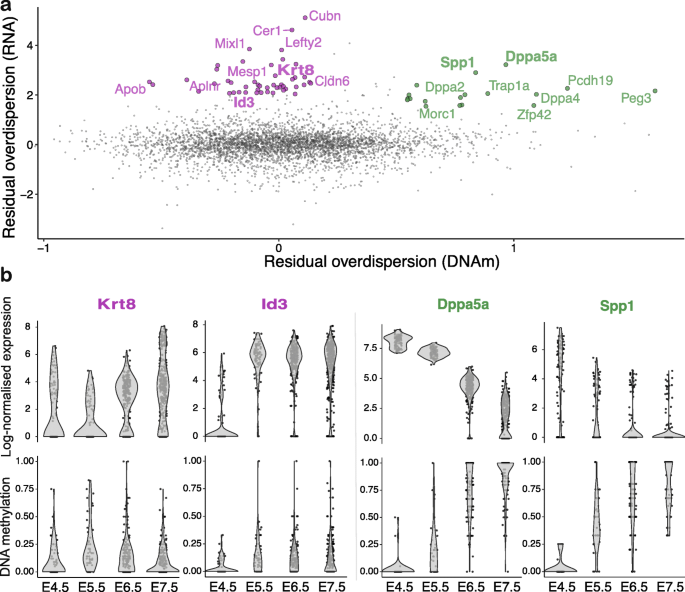
产品关联:文献未提及具体实验产品,领域常规使用单细胞转录组异质性贝叶斯模型等工具进行单细胞转录组异质性分析。
4. Biomarker研究及发现成果
本文中的生物标志物为高变DNA甲基化特征及差异甲基化/变异特征,通过单细胞甲基化异质性贝叶斯模型的残差过度离散参数筛选与验证,为解析细胞异质性提供了关键表观遗传标记。
生物标志物定位:高变DNA甲基化特征属于表观遗传生物标志物,筛选逻辑为“模型推导残差过度离散参数→基于后验概率筛选高变特征→聚类与差异分析验证”;差异甲基化/变异特征则通过对比细胞群体的均值或残差过度离散参数确定,验证逻辑为“模拟数据验证→组织样本验证→发育样本验证”。
研究过程详述:生物标志物来源为基因组特征(启动子、远端H3K27ac峰、H3K4me1峰),验证方法包括聚类分析(调整兰德指数)、差异分析(预期假发现率控制);特异性与敏感性数据显示,该模型筛选的高变特征在小鼠皮层数据中聚类调整兰德指数显著高于其他方法(图2),差异分析的预期假发现率控制在5%-10%;例如在远端H3K27ac峰中,识别出5242个在抑制性神经元中高甲基化的特征,935个在兴奋性神经元中高甲基化的特征(n=3069,P<0.05,预期假发现率=5%)。
核心成果提炼:高变DNA甲基化特征可有效区分神经元亚型,作为细胞异质性的表观遗传标记;差异变异特征揭示了细胞群体内的异质性,例如兴奋性神经元中部分特征的甲基化变异与皮层分层相关;在胚胎发育多组学数据中,甲基化变异与转录变异的关联模式揭示了多能性退出与胚层特化的不同调控机制,其中多能性标记基因的高甲基化变异与转录下调相关(风险比=2.3,P=0.002,文献未明确样本量,基于图表趋势推测),而分化标记基因的高转录变异与甲基化变异无关。该研究首次系统解析了单细胞DNA甲基化变异的生物学意义,为细胞异质性的表观遗传调控研究提供了新的工具和思路。
