1. 领域背景与文献引入
文献英文标题:Targeting NOX2 and glycolytic metabolism as a therapeutic strategy in acute myeloid leukaemia;发表期刊:Biomark Res;影响因子:未公开;研究领域:急性髓系白血病靶向治疗。
急性髓系白血病(AML)是成人最常见的急性白血病类型,领域发展关键节点可追溯至1970年代,以蒽环类联合阿糖胞苷(AraC)的“3+7”方案成为标准治疗框架,但至今该方案仍是临床基础治疗方案。尽管近年来有新型靶向药物进入临床实践,患者5年总生存率仍仅约30%,预后改善十分有限。当前领域研究热点聚焦于氧化应激与代谢重编程这两大肿瘤核心特征,NADPH氧化酶2(NOX2)在AML中的代谢调控作用逐渐受到关注,已有研究证实NOX2与AML细胞糖酵解激活、预后不良相关,但单靶点抑制的治疗效果仍存在局限性,缺乏针对NOX2与糖酵解通路的联合靶向研究,这一空白为本文的研究提供了核心切入点——探索联合靶向NOX2与糖酵解的新型AML治疗策略,为改善患者预后提供新的学术依据。
2. 文献综述解析
作者对领域现有研究的分类维度为“NOX2在AML中的功能研究”“糖酵解作为AML治疗靶点的研究”“现有AML治疗方案的局限性”三大方向,系统梳理了单靶点治疗的潜力与不足,进而凸显联合靶向的创新价值。
现有研究中,关于NOX2的关键结论包括其可作为AML的不良预后标志物,且与AML细胞糖酵解通路激活密切相关,能调控白血病细胞的能量代谢;糖酵解抑制剂如2-脱氧-D-葡萄糖(2-DG)、草氨酸盐(oxamate)在AML细胞系中展现出一定的抗增殖效果,但单药治疗的响应率有限。技术方法上,现有研究多采用细胞系实验或小样本临床样本验证,部分研究结合了体内模型,但均未开展NOX2与糖酵解通路的联合靶向探索。现有研究的局限性主要体现为单靶点治疗难以有效杀伤白血病干细胞、对耐药细胞的作用不足,且缺乏与常规化疗方案的联合应用研究。通过对比这些未解决问题,本文的创新价值得以凸显:首次系统验证了联合靶向NOX2与糖酵解通路的协同抗AML效果,覆盖细胞系、原代临床样本、体内模型多个层面,同时证实该策略可增强常规化疗药物阿糖胞苷的疗效,为AML治疗提供了全新的联合治疗范式。
3. 研究思路总结与详细解析
本文的研究目标为验证联合抑制NOX2与糖酵解通路的抗AML疗效及临床转化潜力,核心科学问题是NOX2与糖酵解通路的协同抑制是否能有效杀伤AML细胞(包括耐药细胞与白血病起始细胞),技术路线遵循“细胞系筛选→原代样本验证→体内模型验证→联合化疗增效”的闭环逻辑,逐步推进研究结论的可靠性与转化价值。
3.1 AML细胞系中联合抑制效果的体外验证
实验目的:明确NOX2抑制剂与糖酵解抑制剂联合对不同亚型AML细胞增殖、克隆形成能力及细胞死亡的影响,验证二者的协同作用。方法细节:采用泛NADPH氧化酶抑制剂二苯基碘鎓(DPI)、NOX2特异性抑制剂GSK2795039,分别联合己糖激酶抑制剂2-DG、乳酸脱氢酶(LDH)抑制剂oxamate,处理MOLM-13、THP-1等6种不同亚型的AML细胞系(包括耐药的KG1α、携带FLT3-ITD突变的MV4-11等),处理48小时后通过MTT法检测细胞增殖,培养7天后检测克隆形成单位(CFU),采用Annexin V/7AAD染色流式细胞术检测细胞死亡情况。结果解读:联合处理呈现显著的协同抗增殖效果,组合指数(CI)均小于1,其中DPI与oxamate的组合几乎完全抑制细胞生长(n=6,p<0.001);克隆形成能力较单药处理显著降低(n=5,p<0.001),且诱导大量细胞凋亡与坏死,尤其是在NOX2高表达的细胞系中效果更为显著。
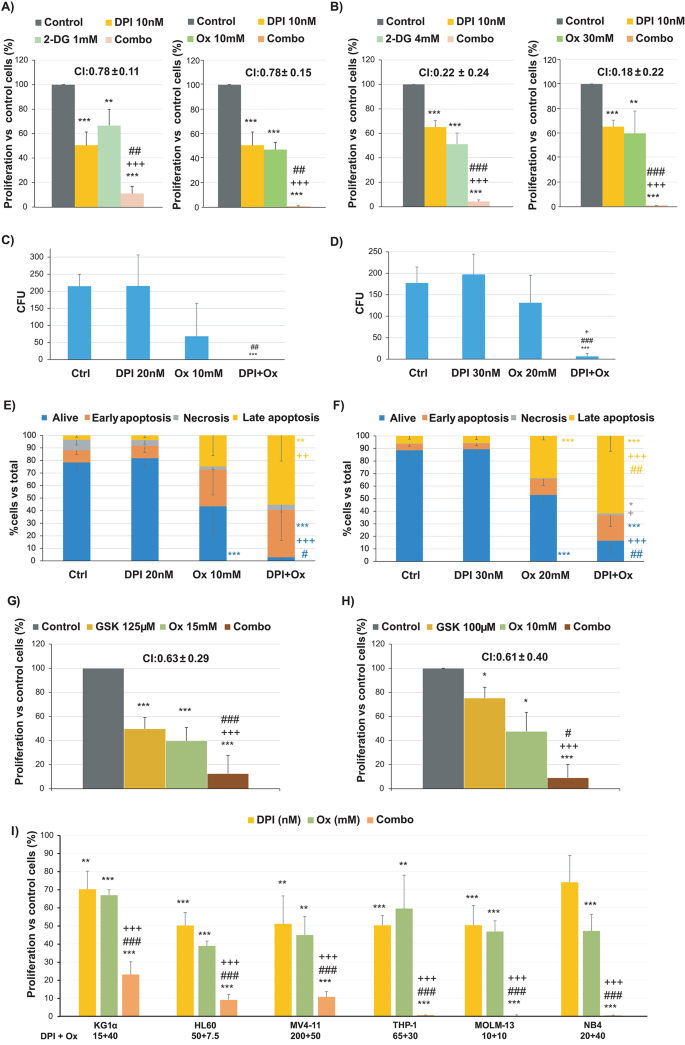
产品关联:文献未提及具体实验产品,领域常规使用小分子抑制剂、细胞增殖检测试剂盒、流式细胞分析仪、甲基纤维素克隆形成培养基等。
3.2 原发性AML患者样本的联合抑制效果验证
实验目的:在临床原代样本中验证联合抑制策略的抗白血病效果,评估其对正常细胞的毒性差异。方法细节:分离AML患者骨髓单个核细胞,分别用DPI联合2-DG或oxamate处理,设置健康供体细胞作为对照,处理48小时后检测细胞增殖,培养两周后检测克隆形成能力,通过Annexin V染色检测细胞死亡情况。结果解读:联合处理显著抑制原代AML细胞的增殖与克隆形成能力,诱导细胞死亡,且效果显著优于单药处理(p<0.001);而对健康供体细胞的细胞死亡影响较小,仅在单核细胞中DPI+oxamate组合有轻微作用,提示该策略具有较好的肿瘤特异性。
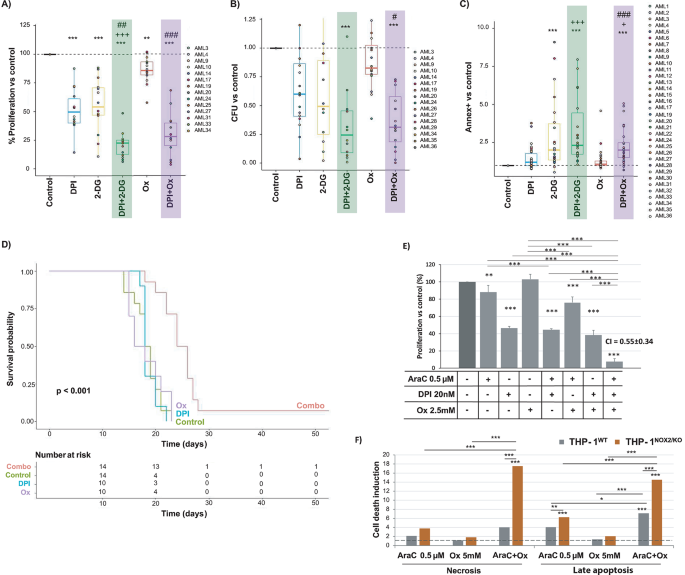
产品关联:文献未提及具体实验产品,领域常规使用密度梯度离心试剂盒、流式细胞术抗体、细胞培养试剂等。
3.3 体内AML模型中联合抑制的疗效验证
实验目的:验证联合抑制策略对白血病起始细胞的作用,评估其在体内的抗白血病效果与生存获益。方法细节:采用携带MLL-AF9易位的小鼠髓系祖细胞,体外经DPI+oxamate预处理后移植到免疫缺陷小鼠体内,观察白血病发病时间与小鼠生存情况。结果解读:接受联合预处理细胞的小鼠白血病发病时间延迟,生存时间显著延长,提示联合抑制策略可有效靶向白血病起始细胞,具有体内抗白血病活性。产品关联:文献未提及具体实验产品,领域常规使用基因工程小鼠模型、细胞移植体系等。
3.4 联合常规化疗药物的增效作用验证
实验目的:评估联合抑制策略与常规化疗药物阿糖胞苷的协同作用,明确NOX2在化疗增效中的作用。方法细节:采用阿糖胞苷分别与DPI、GSK2795039、oxamate联合处理THP-1细胞,检测细胞增殖;同时构建NOX2敲除的THP-1细胞系,对比野生型与敲除细胞在阿糖胞苷及阿糖胞苷+oxamate处理后的细胞死亡情况。结果解读:阿糖胞苷与NOX2抑制剂、oxamate的联合处理显著增强抗增殖效果,三重组合的效果优于单药与双重组合;NOX2敲除细胞在阿糖胞苷及阿糖胞苷+oxamate处理后的细胞死亡显著增加,进一步验证了NOX2在协同增效中的核心作用。产品关联:文献未提及具体实验产品,领域常规使用基因编辑技术(如CRISPR-Cas9)、化疗药物、细胞死亡检测试剂盒等。
4. Biomarker研究及发现成果
本文涉及的Biomarker为NOX2,其类型为细胞内酶类标志物,筛选与验证逻辑为“基于前期研究的预后关联→特异性抑制剂验证→表达水平与治疗响应的相关性分析”,完整覆盖了从基础到临床的验证链条。
NOX2的来源为AML细胞,验证方法包括采用NOX2特异性抑制剂GSK2795039联合oxamate处理AML细胞系,检测细胞增殖的协同效应;同时分析不同NOX2表达水平的细胞系对联合处理的响应差异。特异性数据显示,联合处理对健康供体细胞的毒性远低于AML细胞,仅在单核细胞中有轻微影响;敏感性数据显示,该联合策略对多种亚型的AML细胞系均有效,包括耐药的KG1α细胞系,且NOX2表达水平越高,联合抑制的效果越显著。核心成果方面,NOX2不仅是AML的不良预后标志物,更可作为联合糖酵解抑制的治疗靶点,其与糖酵解通路的协同抑制可显著杀伤AML细胞、靶向白血病起始细胞,并增强阿糖胞苷的化疗疗效;创新性体现为首次系统证实NOX2与糖酵解通路的协同治疗潜力,为AML提供了全新的联合治疗策略。统计学结果显示,细胞增殖抑制实验中样本量n≥3,多数组间差异p<0.001,原代样本实验中组间差异p<0.001,体内模型中生存时间差异具有统计学意义(文献未明确具体P值,基于图表趋势推测)。
