1. 领域背景与文献引入
文献英文标题:Soluble immune checkpoint molecules in cancer risk, outcomes prediction, and therapeutic applications;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫治疗、癌症生物标志物研究
领域共识:肿瘤免疫治疗已成为癌症治疗的核心范式,以程序性死亡蛋白1/配体1(PD-1/PD-L1)、细胞毒性T淋巴细胞相关抗原4(CTLA-4)为靶点的免疫检查点抑制剂(ICIs),通过阻断免疫抑制通路激活适应性免疫,在多种实体瘤治疗中展现显著疗效。然而,传统组织活检存在样本量有限、肿瘤异质性高的局限性,难以精准预测ICIs治疗反应,因此亟需开发微创、易获取、可动态监测的生物标志物。
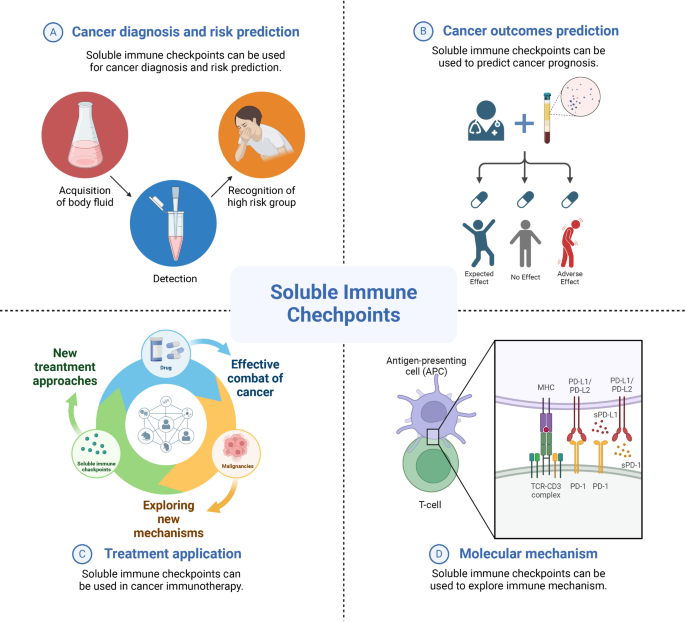
可溶性免疫检查点分子是免疫检查点分子的循环可溶亚型,可通过血液等体液便捷检测,能反映肿瘤微环境的免疫状态,具备作为癌症筛查、预后评估及治疗反应监测标志物的巨大潜力。近年来,随着检测技术的进步,针对可溶性免疫检查点的研究逐年增多,但不同研究结果存在异质性,其调控机制及临床转化应用仍不明确。本综述系统总结了可溶性免疫检查点在人类癌症风险预测、预后评估、治疗应用及潜在分子机制方面的最新研究,为其临床应用提供了全面的循证依据。
2. 文献综述解析
作者以可溶性免疫检查点的临床应用场景为核心分类维度,将现有研究划分为癌症风险筛查、预后预测、治疗应用及分子机制四大板块,系统梳理了领域内的研究证据。
现有研究已证实,多种可溶性免疫检查点分子与癌症风险密切相关:可溶性PD-1(sPD-1)在乙肝相关肝细胞癌、三阴性乳腺癌等患者中水平显著升高,与癌症易感性增加相关;可溶性PD-L1(sPD-L1)在小细胞肺癌、胃癌等多种癌症中水平升高,部分研究中其诊断ROC曲线下面积(AUC)可达0.96,展现出良好的筛查潜力。在预后预测方面,sPD-L1被多数研究认为是不良预后标志物,与非小细胞肺癌、胃癌等多种癌症的较短总生存期、无进展生存期相关;但sPD-1的预后价值存在争议,在部分癌症中是良好预后标志物,在另一些癌症中则相反,这种异质性可能与肿瘤类型、检测方法及患者人群有关。技术方法上,血液检测可溶性免疫检查点具有微创、可动态监测的优势,但不同研究采用的检测平台、 cutoff值不统一,导致结果难以横向比较,且多数研究为回顾性设计,缺乏前瞻性验证。
本综述的创新价值在于首次全面整合了可溶性免疫检查点在癌症全病程中的研究证据,涵盖风险筛查、预后评估到治疗应用的完整链条,同时深入解析了其双向调控的分子机制,明确指出了领域内存在的研究异质性、机制不明确等核心问题,为未来的研究方向提供了清晰的框架,弥补了现有综述多聚焦单一应用场景的局限性。
3. 研究思路总结与详细解析
本研究为系统综述,核心目标是全面总结可溶性免疫检查点分子在癌症中的临床应用价值及分子调控机制,核心科学问题是明确可溶性免疫检查点作为微创生物标志物和治疗靶点的潜力及关键调控通路,技术路线遵循“系统文献检索→按应用场景分类总结→分子机制解析→未来方向展望”的逻辑闭环。
3.1 文献检索与筛选
实验目的是全面收集2024年之前关于可溶性免疫检查点在癌症中应用的相关研究,确保综述的全面性和时效性。方法细节为系统检索PubMed、Embase等主流数据库,纳入符合预设标准的原创研究、综述及meta分析,排除重复研究、非人类研究及无法获取全文的文献。结果解读显示,最终筛选出大量涵盖多种癌症类型、多个可溶性免疫检查点分子的研究,为后续分类总结提供了充足的循证依据。文献未提及具体实验产品,领域常规使用数据库检索工具(如PubMed、Embase)及文献管理软件(如EndNote)完成文献筛选流程。
3.2 按临床应用场景分类总结
实验目的是梳理不同应用场景下可溶性免疫检查点的临床价值,明确其在癌症全病程中的作用。方法细节为将纳入研究划分为癌症风险筛查、预后预测、治疗应用三大板块,分别总结各可溶性免疫检查点分子(如sPD-1、sPD-L1、sCTLA-4、sLAG-3等)在不同癌症中的研究结论,重点关注统计学显著性数据。结果解读显示,sPD-L1在多数癌症中与较高风险及不良预后相关,sCTLA-4在部分癌症中与较短无进展生存期相关,而sPD-1的预后价值存在双向性;在治疗应用方面,可溶性免疫检查点可作为治疗靶点或与其他疗法联合增强抗肿瘤免疫。文献未提及具体实验产品,领域常规使用酶联免疫吸附实验(ELISA)、化学发光免疫分析等试剂检测可溶性免疫检查点分子的表达水平。
3.3 分子机制解析
实验目的是阐明可溶性免疫检查点调控肿瘤免疫的核心机制,为其临床应用提供理论基础。方法细节为总结现有机制研究,分析可溶性免疫检查点与膜型免疫检查点、免疫细胞及肿瘤细胞的相互作用。结果解读显示,可溶性免疫检查点具有双向调控作用:一方面可通过竞争结合膜型配体/受体,阻断免疫抑制通路,增强抗肿瘤免疫,如sPD-1可结合PD-L1,阻断其与膜型PD-1的相互作用,恢复T细胞功能;另一方面可直接抑制免疫细胞功能,促进肿瘤免疫逃逸,如sPD-L1可诱导T细胞耗竭,抑制外周T细胞活性。
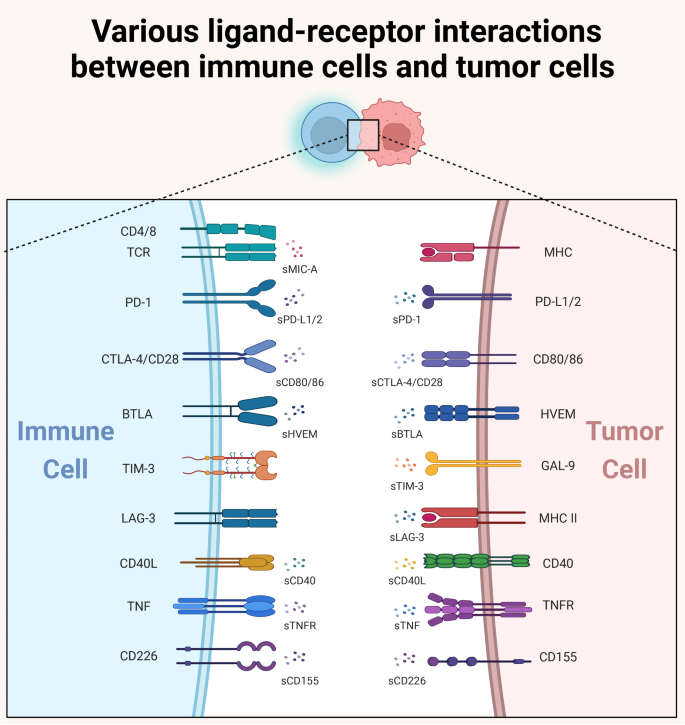
3.4 未来研究方向展望
实验目的是基于现有研究的局限性,提出领域内未解决的问题及未来研究重点。方法细节为分析现有研究的异质性来源、机制空白及临床转化障碍,提出针对性的研究建议。结果解读显示,未来需开展多中心前瞻性研究统一检测标准,深入解析可溶性免疫检查点的双向调控机制,推进其在联合治疗中的临床转化研究,尤其是针对sLAG-3、sTIM-3等新兴分子的研究。文献未提及具体实验产品,领域常规使用临床研究设计工具及分子生物学实验技术开展机制验证。
4. Biomarker研究及发现成果解析
Biomarker定位
本综述涵盖的Biomarker包括sPD-1、sPD-L1、sCTLA-4、sBTLA、sLAG-3、sTIM-3等多种可溶性免疫检查点分子,筛选/验证逻辑为“临床样本检测→流行病学关联分析→预后/治疗反应验证→机制解析”的完整链条:首先通过临床样本检测明确分子表达水平与癌症的关联,再通过大样本队列验证其风险预测、预后评估价值,最后解析其调控肿瘤免疫的机制。
研究过程详述
这些Biomarker的来源为患者的血清或血浆样本,验证方法主要包括ELISA、化学发光免疫分析等定量检测技术,部分研究结合流式细胞术、免疫印迹等方法辅助验证。特异性与敏感性数据方面,sPD-L1在胃癌诊断中的AUC为0.96(95%CI:0.93-0.99),展现出极高的诊断准确性;sTIM-3在基底细胞癌中的AUC为0.848(95%CI:0.721-0.919),可有效预测癌症易感性。预后评估数据显示,sPD-1在肝细胞癌中作为良好预后标志物,无进展生存期风险比HR=0.32(95%CI:0.14-0.74,n=文献未明确),总生存期HR=0.54(95%CI:0.30-0.98,n=文献未明确);sCTLA-4在经典霍奇金淋巴瘤中与较短无进展生存期相关,HR=4.30(95%CI:1.54-13.26,n=文献未明确)。
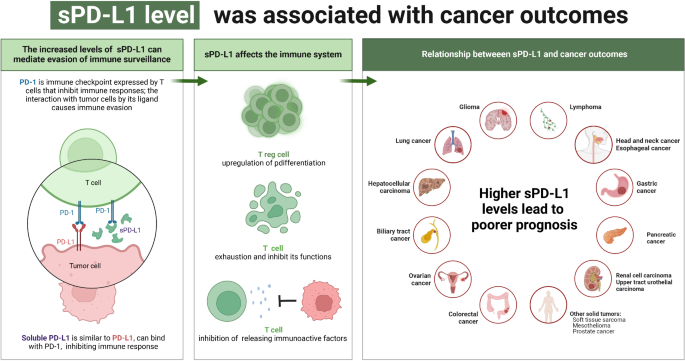
核心成果提炼
这些可溶性免疫检查点Biomarker的功能关联涵盖癌症全病程:作为风险标志物可早期筛查癌症,作为预后标志物可评估患者生存期,作为治疗反应标志物可预测ICIs治疗效果。创新性在于首次系统揭示了其双向调控的分子机制,即部分分子可增强抗肿瘤免疫,部分则促进免疫逃逸,同时提出了其作为治疗靶点的潜在价值,如通过靶向sMIC-A增强CD8+T细胞功能,或通过血浆置换降低sPD-L1水平增强ICIs疗效。统计学结果方面,多数研究均报告了显著的相关性(P<0.05),但部分分子的预后价值存在异质性,需进一步研究明确其适用人群。