1. 领域背景与文献引入
文献英文标题:Baseline extracellular vesicle miRNA-30c and autophagic CTCs predict chemoradiotherapy resistance and outcomes in patients with lung cancer;发表期刊:Biomarker Research;影响因子:未公开;研究领域:局部晚期非小细胞肺癌同步放化疗耐药生物标志物研究。
局部晚期非小细胞肺癌(NSCLC)是肺癌的主要亚型之一,同步放化疗(cCRT)是不可手术患者的标准治疗方案,但临床中约21%的患者对治疗无应答,且多数患者会出现疾病进展,其核心原因是肿瘤细胞产生放化疗耐药性,而自噬通路激活被认为是耐药发生的关键机制之一。领域共识:液体活检作为微创、可重复的检测技术,已成为组织活检的重要补充,细胞外囊泡(EVs)和循环肿瘤细胞(CTCs)是液体活检的核心生物标志物来源,可反映肿瘤异质性及动态变化。当前领域的核心问题是缺乏可有效预测局部晚期NSCLC患者cCRT疗效及预后的生物标志物,现有研究虽已关注EVs miRNA及CTCs在肺癌中的作用,但尚未将自噬激活CTCs与EVs miRNA联合分析,无法全面揭示放化疗耐药的分子机制及提供精准的预后预测指标。基于此,本研究旨在探索EVs miRNA与自噬激活CTCs作为cCRT疗效及预后预测生物标志物的价值,并验证其调控机制,为患者分层治疗提供依据。
2. 文献综述解析
作者的综述逻辑围绕“局部晚期NSCLC cCRT治疗的临床困境→液体活检的应用潜力→自噬与放化疗耐药的关联→现有研究的不足”展开,通过逐层递进的方式明确研究空白。
作者首先总结了局部晚期NSCLC的治疗现状,指出同步放化疗是标准方案,但缺乏有效的疗效预测生物标志物,导致患者无法得到精准分层治疗。随后阐述了液体活检的优势,说明细胞外囊泡和循环肿瘤细胞可提供肿瘤的纵向动态信息,弥补组织活检的局限性;同时强调自噬通路激活与肿瘤细胞放化疗耐药密切相关,细胞外囊泡可通过包裹miRNA调控自噬及肿瘤进展。作者进一步指出现有研究的局限性:已有研究虽关注了CTCs或EVs miRNA在同步放化疗患者中的作用,但尚未有研究整合自噬激活CTCs与EVs miRNA的联合分析,也未明确EVs miRNA对自噬通路的直接调控作用,无法为临床提供兼具预测性和功能性的生物标志物组合。基于此,本研究的创新价值在于首次将EVs miRNA与自噬激活CTCs联合分析,不仅筛选出具有高预测价值的生物标志物,还验证了miR-30c对自噬通路的调控功能,填补了领域内的研究空白。
3. 研究思路总结与详细解析
本研究的整体框架为“临床样本队列分析→生物标志物筛选与预后关联→细胞实验验证功能机制”,核心研究目标是筛选局部晚期NSCLC患者同步放化疗疗效及预后的预测生物标志物,明确miR-30c对自噬通路的调控作用,为临床患者分层治疗提供依据。
3.1 临床样本队列构建与分组
实验目的是建立局部晚期NSCLC同步放化疗患者队列,明确患者的疗效及预后结局,为后续生物标志物分析提供临床基础。研究采用前瞻性设计,纳入38例接受同步放化疗的局部晚期NSCLC患者,中位随访时间为16.4个月(范围0.1-69.1个月),同时纳入13例健康志愿者作为对照组;治疗后根据疗效将患者分为应答者与非应答者,统计患者的复发及生存情况。结果显示,21.1%的患者为非应答者,78.9%的患者出现疾病复发,73.7%的患者死亡,为后续生物标志物的关联分析提供了明确的临床终点。文献未提及具体实验产品,领域常规使用临床样本处理试剂盒、电子病历系统等。
3.2 细胞外囊泡分离鉴定与miRNA表达分析
实验目的是分离患者血浆中的细胞外囊泡,鉴定其特征并分析miRNA表达谱,筛选与同步放化疗疗效相关的miRNA。研究采用纳米颗粒跟踪分析(NTA)、透射电镜(TEM)及免疫印迹(WB)技术对细胞外囊泡进行鉴定,随后对9个与NSCLC放化疗耐药及自噬相关的miRNA进行定量分析。在纳入的38例患者中,26例患者的样本可用于miRNA分析(N=26),结果显示,患者血浆细胞外囊泡的浓度为2.30×10^9±3.25×10^8颗粒/ml,直径模式为126.4±8.5nm,且表达细胞外囊泡特异性标志物CD9和Flotillin-1;非应答者的基线细胞外囊泡miR-375、miR-200c及miR-30c水平显著低于应答者,其中miR-30c的受试者工作特征曲线(ROC曲线)下面积(AUC)为87.2%,具有较高的疗效预测价值。此外,健康志愿者的细胞外囊泡miR-30c水平显著高于患者(p=0.011)。
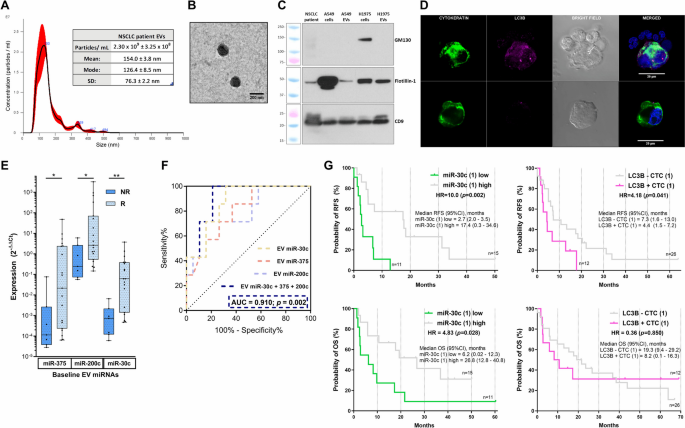
文献未提及具体实验产品,领域常规使用细胞外囊泡分离试剂盒、qRT-PCR试剂盒、免疫印迹相关抗体等。
3.3 自噬激活循环肿瘤细胞检测与分析
实验目的是检测患者外周血中循环肿瘤细胞的自噬激活水平,分析其与同步放化疗疗效及预后的关联。研究采用免疫荧光技术分离并鉴定循环肿瘤细胞,检测自噬标志物LC3B的表达水平,定义高表达LC3B的循环肿瘤细胞为自噬激活循环肿瘤细胞。结果显示,31.6%的患者基线存在自噬激活循环肿瘤细胞,非应答者在治疗期间的自噬激活循环肿瘤细胞比例显著高于应答者(p=0.043);进一步的预后分析显示,基线存在自噬激活循环肿瘤细胞的患者无复发生存期更短(P=0.041)。文献未提及具体实验产品,领域常规使用循环肿瘤细胞分离试剂盒、免疫荧光抗体、激光共聚焦显微镜等。
3.4 细胞实验验证miR-30c对自噬及放化疗敏感性的调控
实验目的是验证miR-30c对NSCLC细胞自噬通路及放化疗敏感性的直接调控作用。研究采用H1975和A549两种NSCLC细胞系,分别转染miR-30c模拟物或抑制剂,随后给予放疗或顺铂处理,检测细胞活力及自噬标志物LC3B、Beclin-1的表达水平。结果显示,转染miR-30c模拟物可显著降低NSCLC细胞的活力,同时抑制自噬标志物LC3B、Beclin-1的表达;而转染miR-30c抑制剂则显著提高细胞活力,促进自噬标志物的表达,表明miR-30c可抑制肿瘤细胞自噬,增强放化疗敏感性。
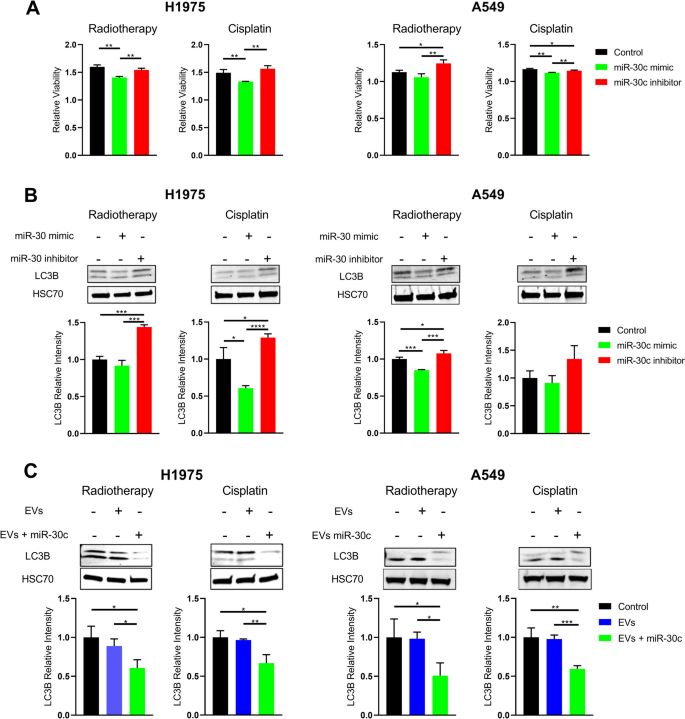
文献未提及具体实验产品,领域常规使用细胞系、RNA转染试剂、细胞活力检测试剂盒、免疫印迹抗体等。
3.5 细胞外囊泡包裹miR-30c的功能验证
实验目的是验证细胞外囊泡包裹的miR-30c对NSCLC细胞自噬通路的调控作用,模拟体内细胞外囊泡的功能传递。研究将miR-30c模拟物载入血浆来源的细胞外囊泡中,处理NSCLC细胞后检测自噬标志物的表达水平。结果显示,载入miR-30c的细胞外囊泡处理后,NSCLC细胞的自噬标志物LC3B表达显著降低,表明细胞外囊泡可有效传递miR-30c并抑制肿瘤细胞自噬,进一步验证了miR-30c的功能作用。文献未提及具体实验产品,领域常规使用细胞外囊泡转染试剂盒、免疫印迹抗体等。
4. Biomarker研究及发现成果解析
本研究筛选并验证了两种具有临床应用潜力的生物标志物——细胞外囊泡miR-30c及自噬激活循环肿瘤细胞,二者联合可有效预测局部晚期NSCLC患者同步放化疗的疗效及预后,同时明确了miR-30c对自噬通路的调控功能。
Biomarker定位方面,细胞外囊泡miR-30c属于循环miRNA类生物标志物,自噬激活循环肿瘤细胞属于细胞亚群类生物标志物;二者的筛选及验证逻辑为:基于临床样本队列筛选与同步放化疗疗效相关的EV miRNA及自噬激活CTCs→分析其与患者预后的关联→通过细胞实验验证miR-30c对自噬通路的调控功能,形成完整的“临床-基础”验证链条。
研究过程详述:细胞外囊泡miR-30c来源于患者外周血浆中的细胞外囊泡,采用qRT-PCR技术进行定量检测,其预测同步放化疗疗效的ROC曲线AUC为87.2%,具有较高的特异性与敏感性;自噬激活循环肿瘤细胞来源于患者外周血,采用免疫荧光技术检测LC3B表达进行鉴定,基线时31.6%的患者存在自噬激活循环肿瘤细胞。
核心成果提炼:低水平的基线细胞外囊泡miR-30c与自噬激活循环肿瘤细胞是局部晚期NSCLC患者无复发生存期(RFS)及总生存期(OS)缩短的独立预测因子,其中低miR-30c组患者的RFS显著短于高miR-30c组(P=0.002),OS也显著更短(P=0.028);自噬激活循环肿瘤细胞组患者的RFS显著短于无自噬激活CTCs组(P=0.041)。本研究的创新性在于首次证明细胞外囊泡miR-30c可直接抑制肿瘤细胞自噬,且联合自噬激活循环肿瘤细胞可作为同步放化疗患者分层及监测的生物标志物,为后续免疫治疗或自噬抑制剂联合治疗提供潜在的指导依据。
