1. 领域背景与文献引入
文献英文标题:Integrated analysis of spatial transcriptomics and CT phenotypes for unveiling the novel molecular characteristics of recurrent and non-recurrent high-grade serous ovarian cancer;发表期刊:Biomark Res;影响因子:未公开;研究领域:妇科肿瘤学-高级别浆液性卵巢癌精准医学。
领域共识:高级别浆液性卵巢癌(HGSOC)是妇科恶性肿瘤中致死率最高的亚型,10年生存率不足30%,约80%患者在接受标准手术与化疗后仍会复发,其高度异质性与晚期诊断特性是临床诊疗的核心难点。领域发展关键节点:2010年后单细胞转录组技术的应用推动了HGSOC肿瘤微环境细胞亚群的解析,2020年以来空间转录组技术的兴起为揭示肿瘤空间异质性提供了工具,放射基因组学结合影像与组学数据成为精准医学的前沿方向。当前研究热点聚焦于复发相关分子标志物、肿瘤微环境细胞互作机制、放射基因组学临床转化,未解决的核心问题包括:缺乏结合空间异质性与临床影像表型的复发预测模型,现有研究无法精准关联HGSOC复发的空间分子特征与CT影像表现。
针对上述研究空白,本研究首次整合空间转录组(ST)与CT表型的放射基因组学分析,旨在揭示HGSOC复发与非复发组的空间分子异质性,关联影像表型与分子通路,为HGSOC的精准诊断与治疗靶点筛选提供新依据,其学术价值在于填补了空间转录组与放射基因组学在HGSOC复发研究中的整合应用空白,为个性化诊疗提供新范式。
2. 文献综述解析
作者按技术维度(bulk转录组→单细胞转录组→空间转录组)与研究维度(肿瘤微环境→预后标志物→放射基因组学)对现有研究进行分类评述,系统梳理了HGSOC研究的技术演进与未解决问题。
bulk转录组研究揭示了HGSOC的核心预后通路如TNF-α、MYC靶点通路,但无法体现肿瘤内部的空间异质性;单细胞转录组解析了HGSOC肿瘤微环境的细胞亚群组成,包括肿瘤细胞、基质细胞、免疫细胞等,但缺乏空间定位信息,无法明确细胞亚群的区域分布与互作;放射基因组学研究结合CT影像与bulk转录组数据,发现了部分影像表型与基因表达的关联,但未整合空间转录组的区域特异性,无法精准定位复发相关分子特征的空间位置。现有研究的局限性在于未同时整合空间转录组的区域分辨率与CT影像的临床表型,无法全面解析HGSOC复发的空间分子机制。
通过对比现有研究的技术局限,本研究的创新点在于首次将空间转录组与CT表型进行整合分析,实现了HGSOC组织区域特异性分子特征与临床影像表型的精准关联,不仅揭示了复发与非复发组的空间细胞亚群差异,还鉴定了与CT表型相关的预后标志物,为放射基因组学在HGSOC中的应用提供了新的研究框架,弥补了现有研究在空间异质性与影像关联方面的不足。
3. 研究思路总结与详细解析
本研究的研究目标是揭示HGSOC复发与非复发组的空间分子特征及与CT表型的关联,核心科学问题是HGSOC复发的空间异质性分子机制及影像表型的分子基础,技术路线遵循“临床队列构建→多组学数据采集→空间分子特征解析→影像-组学关联→公共数据集验证”的闭环逻辑,全面解析了HGSOC复发的空间异质性与临床影像关联。
3.1 患者队列构建与临床样本采集
实验目的是建立具有明确复发结局的HGSOC临床队列,为后续多组学分析提供临床基础。方法细节为纳入8例初治III-IV期HGSOC患者,根据治疗后复发情况分为复发组(5例,定义为治疗后6个月内出现新发病灶)与非复发组(3例,定义为5年无复发),采集手术切除的肿瘤组织用于空间转录组测序,收集术前腹部盆腔增强CT影像用于表型分析,同时整理患者临床病理特征如CA125水平、BRCA突变状态、治疗方案等。结果解读显示,队列中位随访时间为67个月,复发组中位初始CA125水平为1893 IU,显著高于非复发组的1050 IU;所有患者均接受肿瘤细胞减灭术与6-9周期铂类化疗,4例携带BRCA1/2突变的患者中3例接受PARP抑制剂维持治疗,其中1例非复发患者因无复发未接受维持治疗。产品关联:文献未提及具体实验产品,领域常规使用组织固定液、RNA保存液及临床CT扫描仪器。
3.2 空间转录组文库构建与测序
实验目的是获取HGSOC组织的空间分辨率基因表达谱,明确基因表达的区域特异性。方法细节采用10× Genomics Visium空间基因表达解决方案,将肿瘤组织切片固定于Visium玻片,进行苏木精-伊红(HE)染色后,优化透化条件以捕获细胞mRNA,利用带有空间条形码的引物反转录合成cDNA,构建测序文库后,采用Illumina NovaSeq平台进行高通量测序,同时用Agilent 4200 TapeStation评估文库质量,KAPA qPCR试剂盒进行文库定量。结果解读显示,每个样本的空间微阵列包含4992个独特条形码spots,每个spot直径55μm、中心间距100μm,覆盖6.5×6.5mm²的组织区域,每个spots可捕获全转录组范围的基因表达信息,成功获得8例患者的空间基因表达矩阵。产品关联:实验所用关键产品:10× Genomics Visium Spatial Gene Expression Solution、Illumina NovaSeq 测序平台、Agilent Technologies 4200 TapeStation、KAPA qPCR Quantification Kit。
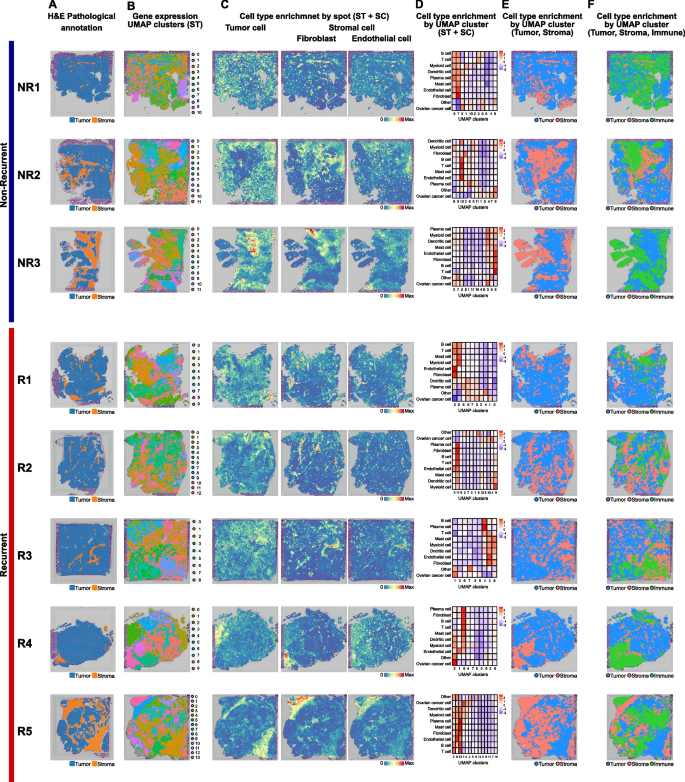
3.3 空间转录组数据处理与细胞类型富集分析
实验目的是解析HGSOC组织的空间细胞亚群分布与区域异质性。方法细节为用10× Genomics Space Ranger v2.0.0处理测序数据,以GRCh38为参考基因组进行基因计数,采用R语言Seurat v4.4.0包进行数据归一化、主成分分析(PCA)降维与聚类,结合公共HGSOC单细胞RNA-seq数据集(GSE180661,包含33例患者的322649个细胞),用Giotto v1.1.2包进行细胞类型富集分析,通过Spearman相关性分析细胞亚群的共定位模式。结果解读显示,通过细胞类型富集将组织区域分为肿瘤区(卵巢癌细胞富集)、基质区(成纤维细胞、内皮细胞富集)、免疫区(T细胞、B细胞、髓系细胞等富集);复发组与非复发组的细胞亚群共定位模式存在差异,复发组卵巢癌细胞与浆细胞的富集呈正相关(相关系数0.19),而非复发组无此关联,成纤维细胞与内皮细胞在两组中均呈强正相关(复发组0.77,非复发组0.75)。产品关联:文献未提及具体实验产品,领域常规使用R语言Seurat、Giotto等生物信息学分析包。

3.4 差异基因与通路富集分析
实验目的是筛选复发与非复发组的空间特异性差异表达基因及核心通路。方法细节为用Seurat的FindMarkers函数进行差异基因分析(调整P<0.05,log2FC>2或<-2),采用基因集富集分析(GSEA)对差异基因进行通路富集,分别分析肿瘤区、基质区、免疫区的差异通路。结果解读显示,复发组肿瘤区显著富集TNF-α通过NF-κB信号通路、氧化磷酸化、G2/M检查点、E2F靶点、MYC靶点v1通路,这些通路均为不良预后标志物;非复发组肿瘤区、基质区、免疫区的ERBB3表达均下调(肿瘤区log2FC=0.88,调整P≤0.001),基质区与免疫区的HMGA1表达下调(基质区log2FC=0.66,调整P≤0.001),这些基因均为已知的癌基因。产品关联:文献未提及具体实验产品,领域常规使用GSEA、edgeR等通路分析工具。
3.5 拷贝数变异与配体受体互作分析
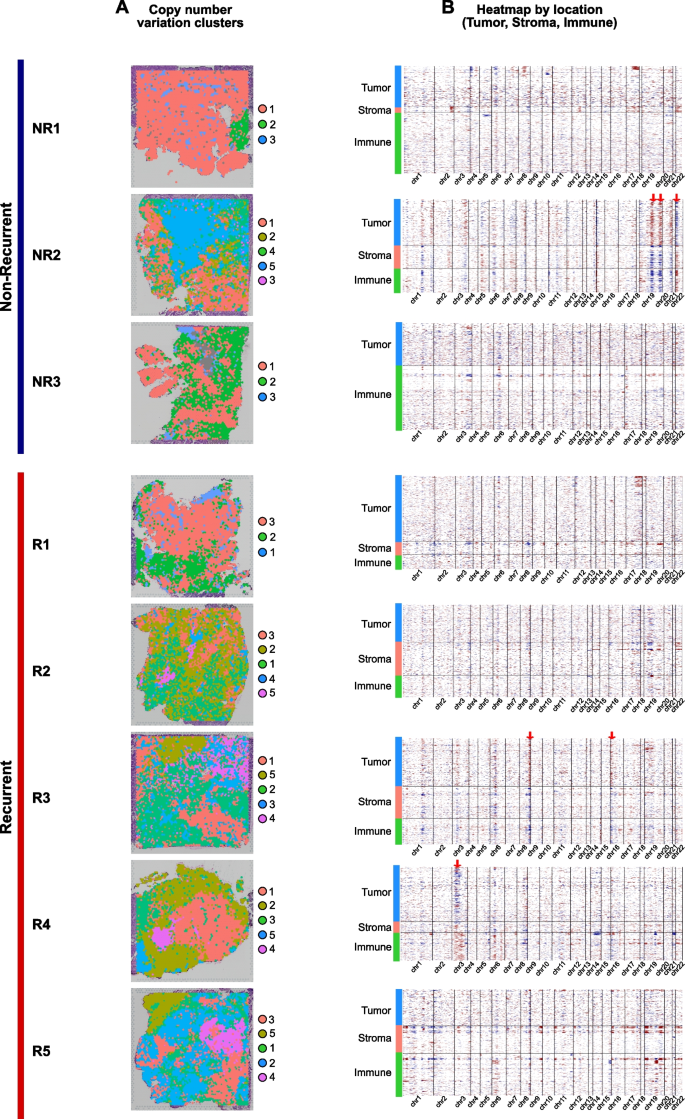
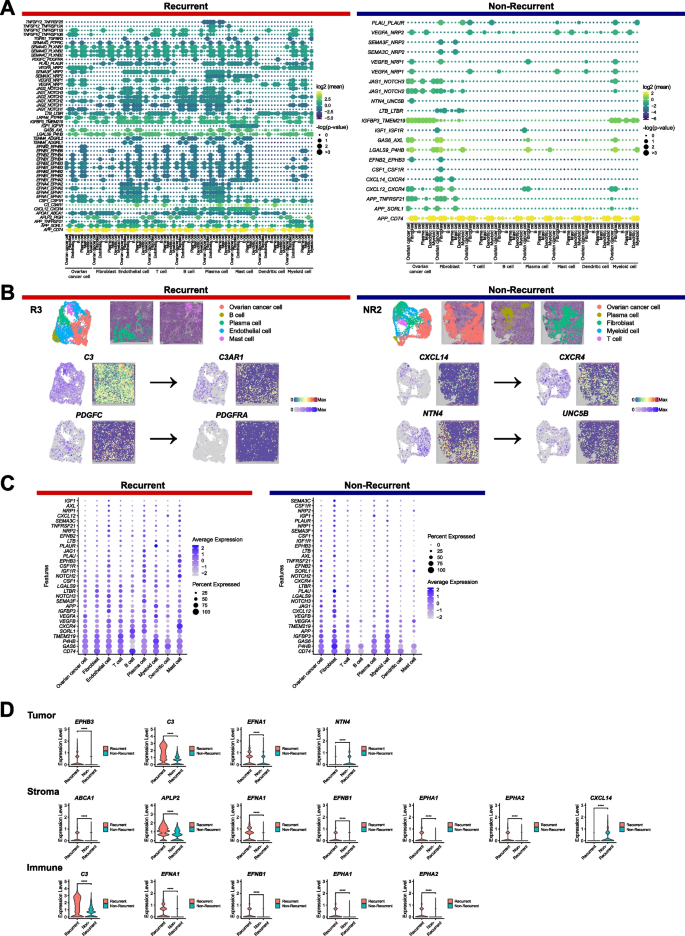
实验目的是解析HGSOC组织的空间拷贝数变异(CNV)差异与细胞间通讯异质性。方法细节为用SpatialInferCNV v0.1.0进行空间CNV分析,分别进行无监督与有监督分析并可视化空间分布;用CellPhoneDB v5.0.0进行配体受体(LR)互作分析,筛选在≥20%细胞中表达的配体与受体,通过置换检验计算显著性。结果解读显示,CNV谱在肿瘤区、基质区、免疫区存在显著差异,例如复发组R3患者肿瘤区存在染色体8的扩增,基质区与免疫区存在染色体16的缺失;LR互作分析显示复发组有51个独特LR对,其中TNF家族配体受体对(如TNFSF10-TNFRSF10B)、血小板衍生生长因子通路LR对仅在复发组存在,非复发组有21个LR对,其中趋化相关的CXCL14-CXCR4、NTN4-UNC5B对为非复发组特有,提示细胞间通讯异质性与复发结局相关。产品关联:文献未提及具体实验产品,领域常规使用SpatialInferCNV、CellPhoneDB等生物信息学分析工具。
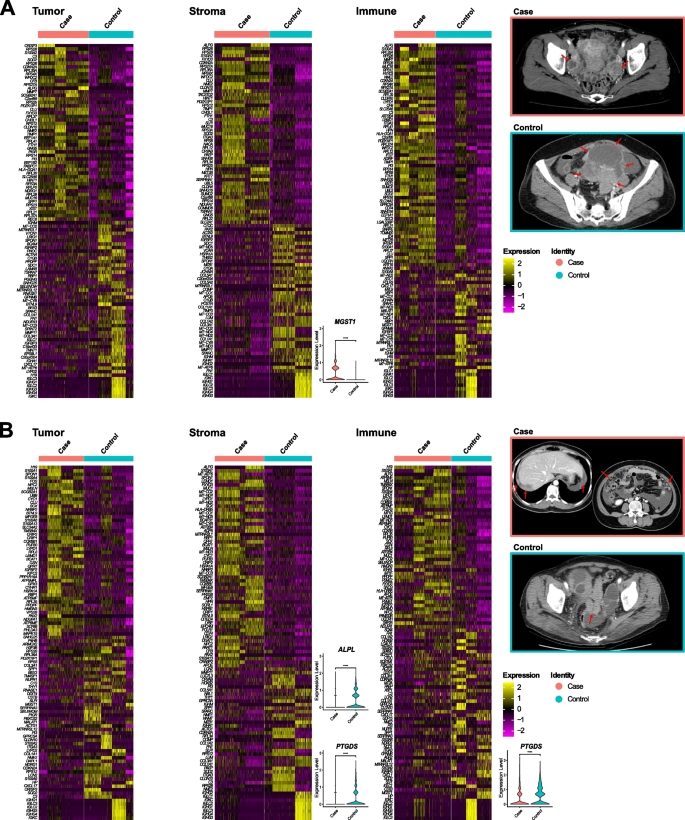
3.6 CT表型分析与放射基因组学关联验证
实验目的是关联HGSOC的CT影像表型与空间分子特征,验证预后标志物的临床价值。方法细节为由放射医师评估CT表型,包括卵巢肿块大小、种植转移模式、部位数量等,筛选出4种与复发相关的CT表型(肿块直径≥7.8cm、结节型种植转移、结肠旁沟种植、种植部位≥3个),结合内部8例样本与TCGA/TCIA公共40例样本,分析CT表型与差异基因的关联,采用通路富集分析关联CT表型与核心通路。结果解读显示,种植部位≥3个与PTGDS的下调相关,复发组肿瘤区与基质区的PTGDS表达显著低于非复发组(肿瘤区log2FC=-0.42,调整P<0.001;基质区log2FC=-0.31,调整P<0.001);免疫调节相关基因DAPL1(肿瘤区)、RNASE1(基质区)为非复发组的良好预后标志物;结肠旁沟种植、种植部位≥3个等CT表型与复发组富集的通路(如TNF-α/NF-κB、氧化磷酸化)显著关联。产品关联:文献未提及具体实验产品,领域常规使用CT影像分析软件及生物信息学整合分析工具。
4. Biomarker研究及发现成果解析
本研究鉴定了HGSOC复发相关的两类Biomarker,包括复发不良预后Biomarker与非复发良好预后Biomarker,筛选逻辑遵循“空间转录组差异筛选→CT表型关联→公共数据集验证”的完整链条,为HGSOC的预后预测与精准诊疗提供了新的靶点。
Biomarker定位
不良预后Biomarker包括TNF-α通过NF-κB信号通路基因、氧化磷酸化通路基因、G2/M检查点通路基因等,筛选逻辑为空间转录组复发组差异通路富集→CT表型关联验证;良好预后Biomarker包括PTGDS、CXCL14、NTN4、DAPL1、RNASE1,筛选逻辑为空间转录组非复发组差异基因筛选→CT表型关联→公共数据集验证。
研究过程详述
不良预后Biomarker的来源为HGSOC肿瘤区、基质区的基因表达数据,验证方法为GSEA通路富集分析与公共数据集关联,其与复发组及不良CT表型(如种植部位≥3个、结肠旁沟种植)显著关联,通路富集的标准化富集评分(NES)均>2,调整P<0.001;良好预后Biomarker中,PTGDS来源为肿瘤与基质组织,验证方法为空间转录组差异分析与TCGA/TCIA公共数据集验证,其下调与种植部位≥3个相关(n=48,调整P<0.001);CXCL14、NTN4为趋化相关标志物,来源为基质区与肿瘤区,在非复发组高表达(CXCL14 log2FC=-2.73,n=8,调整P<0.001;NTN4 log2FC=-1.89,n=8,调整P<0.001);DAPL1、RNASE1为免疫调节标志物,在非复发组肿瘤区与基质区高表达,调整P<0.001。
核心成果提炼
PTGDS作为预后标志物,首次在空间转录组中被证实与HGSOC复发及种植转移相关,其低表达提示不良预后,功能关联为其编码的前列腺素D2可抑制卵巢癌细胞生长;CXCL14、NTN4首次被鉴定为非复发组的空间特异性良好预后标志物,CXCL14可抑制血管生成,NTN4与肿瘤转移负相关;不良预后通路如TNF-α/NF-κB、氧化磷酸化首次被关联到CT表型,为通过影像表型预测复发风险提供了分子基础;统计学结果显示所有Biomarker的调整P值均<0.001,样本量为内部8例+公共40例,置信区间数据未提及。
