1. 领域背景与文献引入
文献英文标题:SYT7 regulates the progression of chronic lymphocytic leukemia through interacting and regulating KNTC1;发表期刊:Biomarker Research;影响因子:未公开;研究领域:慢性淋巴细胞白血病的分子机制与靶向治疗
慢性淋巴细胞白血病(CLL)是西方最常见的淋巴增殖性疾病,以CD5+/CD19+恶性B细胞的克隆性扩增为特征,细胞在血液、骨髓、淋巴结等组织中蓄积,临床病理异质性极高,伴随染色体畸变、反复突变及微环境参与。现有治疗手段包括布鲁顿酪氨酸激酶(BTK)、B细胞淋巴瘤-2(BCL-2)抑制剂等小分子靶向药物,以及标准化学免疫治疗,但仍有部分患者治疗耐受性差,且因疾病异质性存在短期复发或进展的情况。尽管已有多种遗传变异被证实与CLL进展相关,且靶向治疗推动CLL进入精准医学时代,但仍有大量未知调控通路待挖掘,新靶点的鉴定对CLL的预后预测和治疗至关重要。
领域共识:Synaptotagmins家族是多功能钙传感器,其中Synaptotagmin 7(SYT7)在实体瘤中被证实具有促癌作用,可通过调控细胞增殖、侵袭、凋亡等恶性行为参与胃癌、非小细胞肺癌、甲状腺癌的进展,但SYT7在血液系统肿瘤尤其是CLL中的作用尚未见报道。因此,本研究旨在探索SYT7在CLL中的功能及分子机制,为CLL的精准治疗提供新靶点。
2. 文献综述解析
作者围绕CLL的临床治疗困境与SYT7的肿瘤调控功能展开综述,通过对比实体瘤与血液系统肿瘤的研究空白,明确本研究的必要性与创新性。
作者首先对CLL领域的现有研究进行分类梳理:一是临床特征与治疗现状,指出CLL的高异质性导致治疗反应差异大,现有治疗虽有进展但仍存在局限性;二是分子机制研究,已发现多种遗传变异与CLL进展相关,但仍有大量未知调控通路待挖掘。现有研究的优势在于明确了CLL的核心驱动突变及部分靶向治疗靶点,推动了精准治疗的发展,局限性在于对非经典信号通路及跨组织的分子调控机制研究不足,尤其是SYT7这类在实体瘤中功能明确但在CLL中未被探索的分子。
针对SYT7的研究,作者综述了其在实体瘤中的促癌机制,包括促进胃癌肝转移、非小细胞肺癌上皮间质转化、甲状腺癌中调控HMGB3泛素化等,这些研究明确了SYT7的促癌功能,但均未涉及血液系统肿瘤。本研究的创新价值在于首次将SYT7的研究拓展至CLL领域,揭示了其通过SYVN1介导KNTC1泛素化的新调控机制,填补了SYT7在血液系统肿瘤中功能研究的空白,为CLL的靶向治疗提供了新的潜在靶点。
3. 研究思路总结与详细解析
本研究整体遵循“表达验证→功能验证→机制探索→靶点确认”的逻辑闭环,研究目标是明确SYT7在CLL中的功能及分子机制,核心科学问题是SYT7如何调控CLL细胞的恶性行为,技术路线为:首先检测SYT7在CLL组织与细胞中的表达水平,然后通过体内外实验验证SYT7对CLL细胞增殖、凋亡、迁移等恶性行为的影响,再通过基因芯片、免疫共沉淀等技术探索其下游靶点及调控机制,最后验证下游靶点KNTC1在SYT7促CLL进展中的作用。
3.1 SYT7在CLL组织与细胞中的表达验证
实验目的:明确SYT7在CLL患者组织及细胞系中的表达模式,为后续功能研究提供基础。方法细节:收集179例CLL患者肿瘤组织和27例正常淋巴组织构建组织芯片,采用免疫组化(IHC)检测SYT7蛋白表达;采用qPCR检测CLL细胞系(MEC-2、M01043)、原代CLL细胞及正常B细胞中SYT7 mRNA的表达水平。结果解读:免疫组化结果显示,CLL组织中SYT7阳性表达率显著高于正常淋巴组织(P<0.001),qPCR结果显示CLL细胞系及原代CLL细胞中SYT7 mRNA表达水平显著高于正常B细胞,提示SYT7在CLL中呈高表达状态。
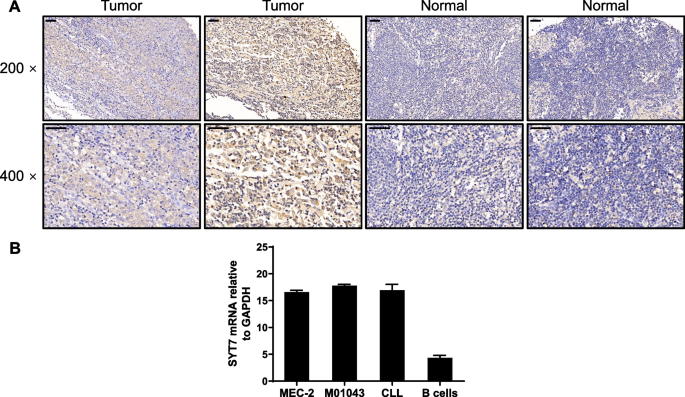
产品关联:文献未提及具体实验产品,领域常规使用免疫组化检测试剂盒、qPCR试剂盒、组织芯片制备服务等。
3.2 SYT7敲低对CLL细胞体外恶性行为的影响
实验目的:验证SYT7对CLL细胞体外增殖、凋亡、周期分布及迁移能力的调控作用。方法细节:构建靶向SYT7的shRNA慢病毒载体,感染MEC-2和M01043细胞,筛选出敲低效率最高的shRNA序列;采用CCK8试剂盒检测细胞增殖活性,流式细胞术检测细胞凋亡率及周期分布,Transwell实验检测细胞迁移能力,人凋亡抗体芯片检测凋亡相关蛋白表达变化。结果解读:SYT7敲低后,CLL细胞增殖活性显著降低(n=3,P<0.001),凋亡率显著升高(n=3,P<0.001),细胞周期阻滞于G2期(n=3,P<0.001),迁移能力显著下降(n=3,P<0.001);凋亡抗体芯片结果显示,抗凋亡蛋白Bcl-2、Bcl-w、cIAP-2等表达显著下调,促凋亡相关通路激活。
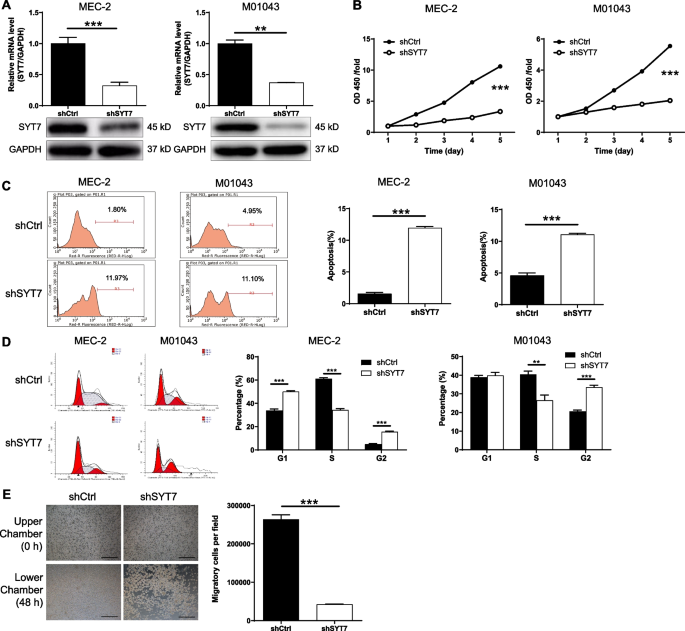
产品关联:实验所用关键产品:慢病毒载体(上海翊贝瑞)、CCK8试剂盒(Sigma)、Transwell小室(Corning)、流式细胞仪(BD Biosciences)、人凋亡抗体芯片(R&D Systems)等。
3.3 SYT7过表达对CLL细胞体外恶性行为的影响
实验目的:反向验证SYT7对CLL细胞恶性行为的调控作用。方法细节:构建SYT7过表达慢病毒载体,感染MEC-2细胞,通过qPCR和WB验证过表达效率;采用CCK8、流式细胞术、Transwell实验检测细胞增殖、凋亡、周期及迁移能力。结果解读:SYT7过表达后,CLL细胞增殖活性显著增强(n=3,P<0.001),对细胞凋亡影响较小(文献未明确提供该数据,基于图表趋势推测),细胞周期G2期比例显著降低(n=3,P<0.001),对细胞迁移无显著影响(因MEC-2细胞本身迁移能力较强)。
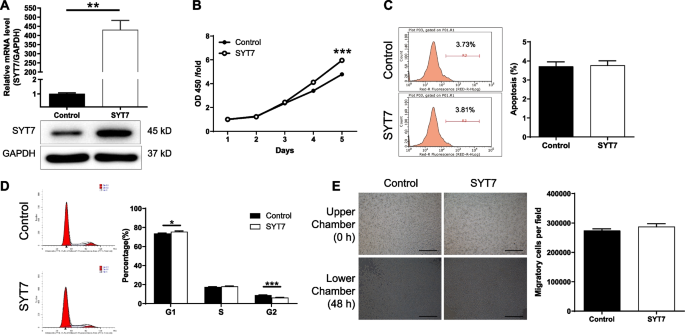
产品关联:文献未提及具体实验产品,领域常规使用过表达载体构建服务、WB检测试剂盒等。
3.4 SYT7敲低对CLL体内成瘤的影响
实验目的:验证SYT7在体内对CLL肿瘤生长的调控作用。方法细节:将SYT7敲低的MEC-2细胞及对照细胞分别接种于BALB/c裸鼠皮下,每周2-3次测量肿瘤体积及小鼠体重,接种11天后腹腔注射D-荧光素进行生物发光成像,检测肿瘤负荷;处死小鼠后取肿瘤组织,采用免疫组化检测Ki-67表达以评估细胞增殖活性。结果解读:SYT7敲低组肿瘤体积、重量及生物发光强度均显著低于对照组(n=10,P<0.001),Ki-67阳性率显著降低,提示SYT7敲低可显著抑制CLL细胞的体内成瘤能力。
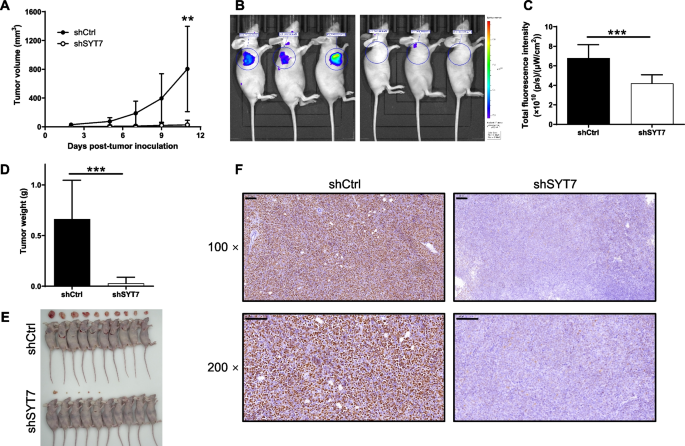
产品关联:实验所用关键产品:BALB/c裸鼠(北京维通利华)、D-荧光素(上海乾辰)、生物发光成像系统(Perkin Elmer)、Ki-67抗体等。
3.5 SYT7调控CLL的分子机制探索
实验目的:揭示SYT7调控CLL进展的下游靶点及分子机制。方法细节:采用基因芯片分析SYT7敲低前后MEC-2细胞的差异表达基因,筛选出候选下游靶点KNTC1;采用免疫组化检测KNTC1在CLL组织中的表达;通过蛋白稳定性实验、泛素化实验、Co-IP实验验证SYT7对KNTC1的调控机制。结果解读:基因芯片结果显示KNTC1在SYT7敲低后显著下调,免疫组化结果显示KNTC1在CLL组织中高表达且与SYT7表达正相关;蛋白稳定性实验显示SYT7敲低可降低KNTC1蛋白稳定性,泛素化实验显示SYT7敲低可促进KNTC1的泛素化,Co-IP实验证实SYT7与E3泛素连接酶SYVN1相互作用,抑制其介导的KNTC1泛素化,从而稳定KNTC1蛋白。
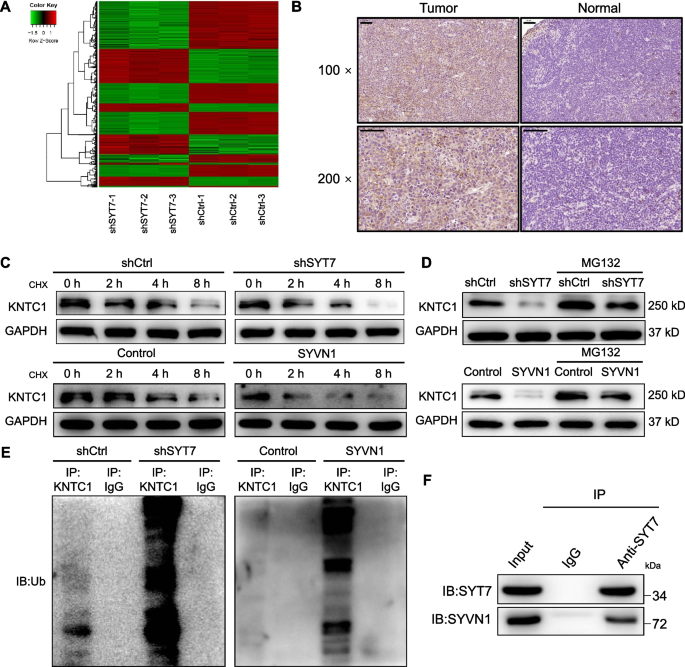
产品关联:文献未提及具体实验产品,领域常规使用基因芯片(Affymetrix)、Co-IP试剂盒、泛素化检测试剂等。
3.6 KNTC1在SYT7促CLL中的作用验证
实验目的:验证KNTC1是SYT7调控CLL进展的关键下游靶点。方法细节:构建KNTC1敲低及SYT7过表达联合KNTC1敲低的MEC-2细胞系,采用CCK8、流式细胞术、Transwell实验检测细胞增殖、凋亡、周期及迁移能力。结果解读:KNTC1敲低可显著抑制CLL细胞增殖(n=3,P<0.001)、促进凋亡(n=3,P<0.001)、阻滞细胞周期于G2期(n=3,P<0.001)、抑制迁移(n=3,P<0.001);同时,KNTC1敲低可逆转SYT7过表达对CLL细胞恶性行为的促进作用,提示KNTC1是SYT7调控CLL进展的关键下游功能靶点。
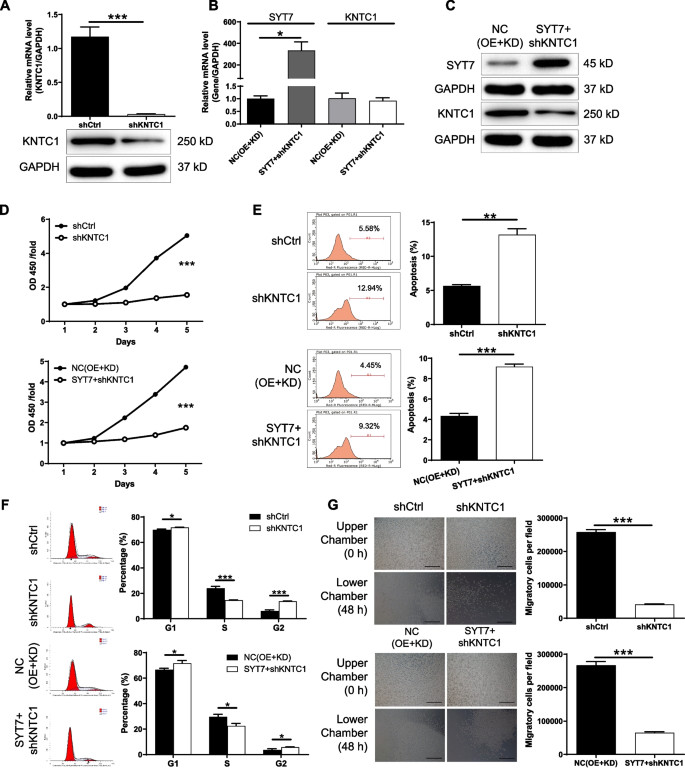
产品关联:文献未提及具体实验产品,领域常规使用shRNA载体构建服务、细胞功能检测试剂盒等。
4. Biomarker研究及发现成果解析
本研究鉴定了SYT7和KNTC1作为CLL进展的潜在分子Biomarker,明确了二者的表达模式、调控机制及功能关联,为CLL的靶向治疗提供了新的候选靶点。
Biomarker定位:SYT7和KNTC1属于CLL的促癌分子Biomarker,筛选逻辑为:首先通过临床组织样本检测发现二者在CLL组织中高表达,然后通过细胞和动物实验验证其促癌功能,最后通过机制研究明确二者的调控关系。SYT7的筛选路径为“临床组织表达验证→细胞功能验证→体内成瘤验证→机制探索”,KNTC1的筛选路径为“基因芯片差异表达筛选→临床组织表达验证→功能回补验证”。
研究过程详述:SYT7的来源为179例CLL患者组织样本及CLL细胞系,验证方法包括免疫组化、qPCR、WB,特异性表现为CLL组织中SYT7阳性率显著高于正常组织(P<0.001),敏感性未提供具体数据;KNTC1的来源为CLL组织样本及细胞系,验证方法包括免疫组化、qPCR、WB、泛素化实验,特异性表现为CLL组织中KNTC1表达与SYT7正相关,敏感性未提供具体数据。
核心成果提炼:SYT7通过抑制SYVN1介导的KNTC1泛素化稳定KNTC1蛋白,从而促进CLL细胞的增殖、抗凋亡、迁移等恶性行为,二者具有协同促癌作用;本研究首次揭示了SYT7在CLL中的功能及新调控机制,创新性在于将SYT7的研究拓展至血液系统肿瘤,为CLL的靶向治疗提供了新的潜在靶点;目前尚未提供SYT7和KNTC1作为预后Biomarker的临床数据,如风险比(HR)、ROC曲线等,需进一步临床研究验证其预后价值。
