1. 领域背景与文献引入
文献英文标题:IL1RAP is an immunotherapeutic target for normal karyotype triple-mutated acute myeloid leukemia;发表期刊:Biomarker Research;影响因子:未公开;研究领域:急性髓系白血病免疫治疗靶点研究
急性髓系白血病(AML)是一类高度异质性的血液系统恶性肿瘤,基于细胞遗传学和分子遗传学特征可分为不同亚型,其中正常核型AML(NK-AML)约占所有AML的40%-50%。欧洲白血病网络(ELN)将携带NPM1突变(NPM1c)的NK-AML归为预后良好亚型,但当同时伴随FLT3内部串联重复突变(FLT3-ITD)时,预后显著变差。进一步的研究发现,部分NPM1c NK-AML还同时存在DNMT3A突变,这类被称为正常核型三突变AML(NKt-AML)的亚型,对现有化疗和造血干细胞移植(HSCT)的响应率低,5年总生存率不足20%,是AML治疗中的难点之一。领域共识:AML的免疫治疗依赖于特异性细胞表面抗原的识别,然而目前已获批的免疫治疗靶点(如CD33)存在与正常造血干细胞交叉表达的问题,导致治疗相关毒性,因此亟需筛选出仅在白血病细胞尤其是白血病干细胞(LSC)表面高表达的特异性抗原。
针对NKt-AML治疗的困境,本研究通过整合多组学技术,系统分析NKt-AML的表面蛋白质组特征,旨在发现具有临床转化潜力的特异性免疫治疗靶点,为这类难治性AML患者提供新的治疗策略。
2. 文献综述解析
作者在综述部分围绕AML免疫治疗靶点的研究现状、现有局限性及NKt-AML的治疗需求三个核心维度展开评述。现有研究中,AML表面抗原的筛选主要依赖于单一转录组分析或小样本蛋白质组学技术,存在无法精准反映蛋白表面定位、样本代表性不足等问题;已报道的AML免疫治疗靶点如CD33、CD123等,虽然在AML细胞表面表达,但也在正常造血干细胞或造血祖细胞中存在不同程度的表达,导致治疗后可能出现严重的骨髓抑制等不良反应;针对NKt-AML的研究显示,这类亚型具有独特的基因表达谱和细胞表面特征,但目前尚未发现特异性的治疗靶点,现有治疗方案仍以化疗联合FLT3抑制剂为主,但FLT3抑制剂易出现耐药,且无法有效清除白血病干细胞,导致患者复发率高。
与现有研究相比,本研究采用了整合表面蛋白质组、bulk转录组和单细胞转录组的多组学策略,首次在大样本AML队列中系统分析了NKt-AML的表面蛋白质组特征,筛选出IL1RAP这一在NKt-AML原始细胞高表达、而在正常造血干细胞低表达的特异性抗原,解决了现有靶点特异性不足的问题,同时验证了其作为抗体药物偶联物(ADC)靶点的可行性,为NKt-AML的精准免疫治疗提供了新方向。
3. 研究思路总结与详细解析
本研究的核心目标是筛选NKt-AML的特异性免疫治疗靶点,核心科学问题是NKt-AML是否存在仅在白血病细胞尤其是白血病干细胞表面高表达的特异性表面抗原,技术路线遵循“多组学筛选→表达验证→预后关联→功能验证”的闭环逻辑。
3.1 多组学分析筛选NKt-AML表面抗原
实验目的:通过多组学技术筛选NKt-AML中特异性高表达的表面蛋白。方法细节:对100例原发性AML样本(其中12例为NKt-AML)进行表面蛋白质组富集分析,同时对691例原发性AML样本进行转录组分析,对23例原发性AML样本进行单细胞RNA测序。利用自主开发的表面蛋白注释工具(SPAT)对筛选到的蛋白进行表面定位评分,结合正常组织和造血细胞的表达数据,筛选出具有潜在安全性的候选抗原。结果解读:表面蛋白质组分析显示,NKt-AML与其他AML亚型相比,有412个蛋白表达上调,其中88个蛋白的SPAT评分≥8,提示为潜在的表面蛋白。通过与正常组织和造血细胞的表达数据对比,最终筛选出CTSG、ADGRG5和IL1RAP三个候选抗原,其中IL1RAP在NKt-AML的原始细胞中高表达,而在正常骨髓造血干细胞中低表达。

实验所用关键产品:表面蛋白质组富集采用质谱分析(未提及具体品牌),转录组和单细胞转录组分析采用常规测序平台(未提及具体品牌),SPAT工具为自主开发。
3.2 IL1RAP表达的多维度验证
实验目的:验证IL1RAP在NKt-AML中的特异性表达模式。方法细节:利用单细胞RNA测序数据对比6例NKt-AML样本和正常骨髓样本中IL1RAP的表达,同时对76例原发性AML样本(含19例NKt-AML)进行流式细胞术分析,检测IL1RAP在白血病细胞表面的表达比例。结果解读:单细胞RNA测序结果显示,IL1RAP在所有6例NKt-AML的AML细胞和类造血干细胞(HSC-like)AML细胞中均均匀高表达,而在正常骨髓的HSC-like细胞中表达极低。流式细胞术结果显示,NKt-AML中表达IL1RAP的白血病细胞比例显著高于其他AML亚型(n=19,P<0.01)。
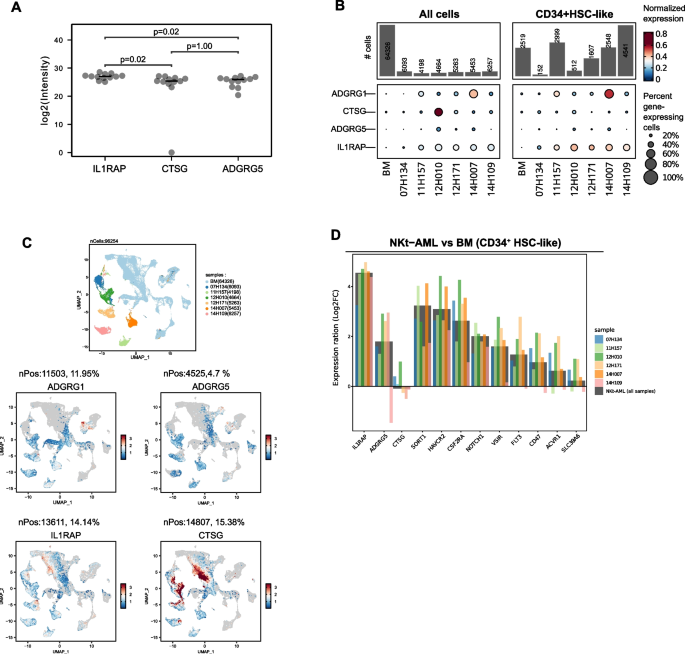
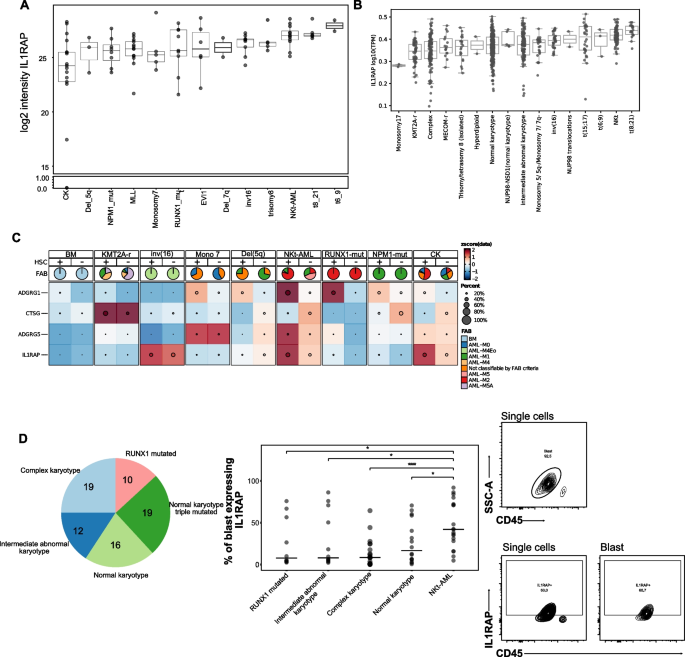
实验所用关键产品:流式细胞术采用R&D Systems的抗IL1RAP-PE抗体(货号FAB676P)、BD Biosciences的CD45抗体(货号560777)、BioLegend的GPR56抗体(货号358206),数据采集使用BD FACSFortessa流式细胞仪。
3.3 IL1RAP表达与临床预后的关联分析
实验目的:分析IL1RAP表达与AML患者临床预后的关联。方法细节:利用Leucegene队列中691例AML患者的转录组数据和临床信息,将中危AML患者(n=316)根据IL1RAP表达水平分为高表达组(第3四分位数以上)和低表达组,分析两组的总生存率(OS)和无复发生存率(RFS),以及接受HSCT患者的预后差异。结果解读:高IL1RAP表达的中危AML患者总生存率显著低于低表达组(HR=1.61,95% CI 1.17-2.24,P<0.01),无复发生存率也显著降低(HR=1.58,95% CI 1.08-2.30,P=0.02)。对于接受HSCT的患者(n=66),高IL1RAP表达组的总生存率(HR=2.82,95% CI 1.35-5.89,P<0.01)和无复发生存率(HR=2.46,95% CI 1.23-4.93,P=0.01)均显著低于低表达组,提示IL1RAP高表达可预测HSCT无响应。
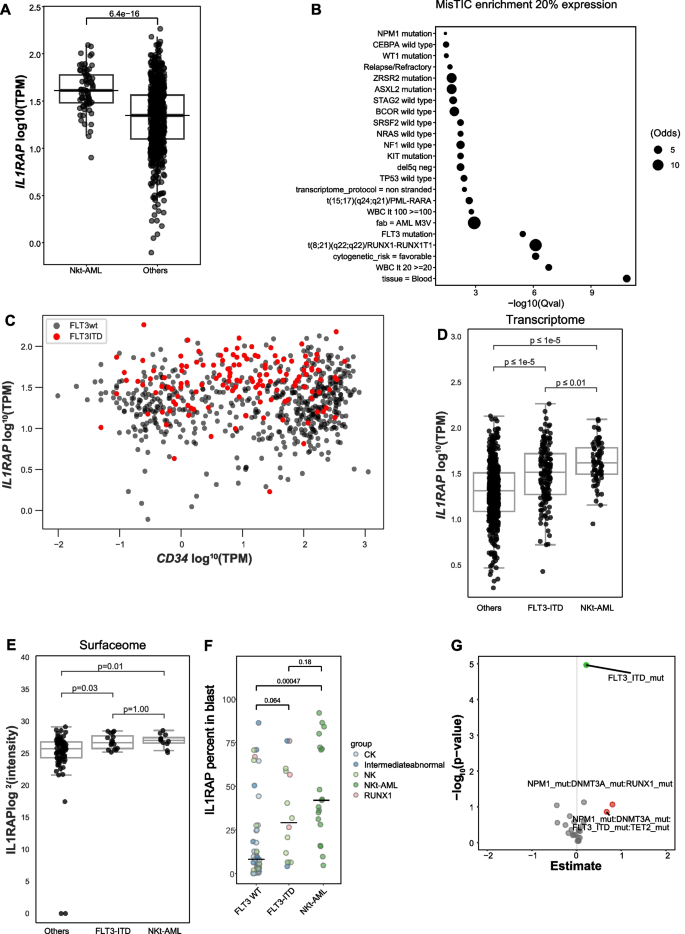
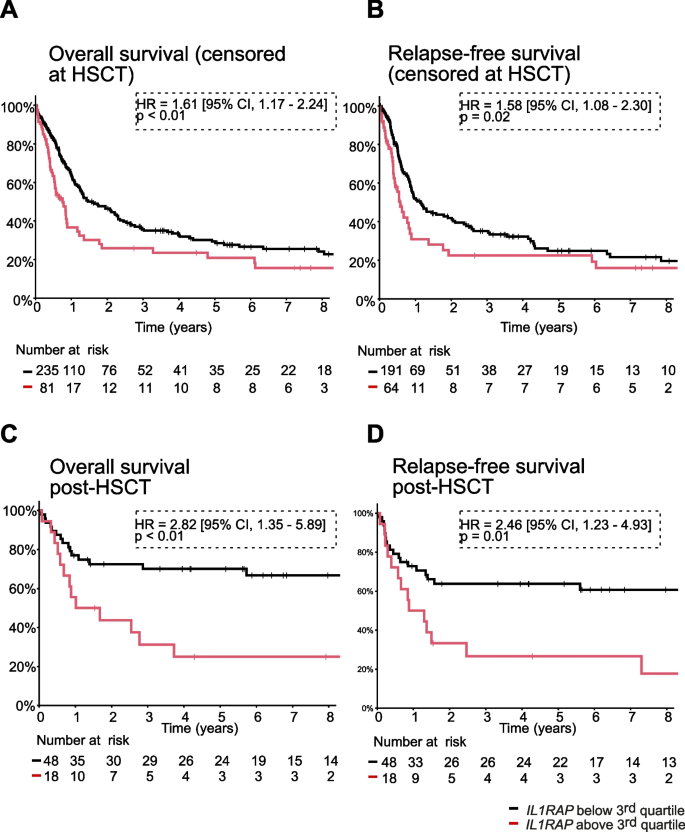
文献未提及具体实验产品,领域常规使用生存分析软件如R语言survival包。
3.4 IL1RAP作为免疫治疗靶点的功能验证
实验目的:验证IL1RAP作为抗体药物偶联物(ADC)靶点的可行性。方法细节:首先通过流式细胞术分析正常骨髓中IL1RAP的表达,评估靶点的安全性;然后在OCI-AML3细胞系中进行IL1RAP抗体的内化实验,检测抗体与IL1RAP结合后的内化效率;最后在AML5细胞系中进行ADC抑制实验,评估靶向IL1RAP的ADC对白血病细胞的杀伤作用。结果解读:正常骨髓中IL1RAP主要表达于CD34-细胞,CD34+造血干细胞中仅少量表达,提示靶向IL1RAP的治疗可能具有较低的骨髓毒性。内化实验显示,IL1RAP抗体与细胞结合后30分钟,二级抗体信号降低50%,表明IL1RAP可随抗体内化进入细胞,符合ADC靶点的要求。ADC抑制实验显示,Nadunolimab(抗IL1RAP抗体)联合PNU偶联的二级抗体对AML5细胞的IC50为0.041 nM,而单独PNU偶联二级抗体的IC50为4.22 nM,IL1RAP阴性的U266细胞对该ADC无响应,提示靶向IL1RAP的ADC可特异性杀伤IL1RAP阳性的白血病细胞。
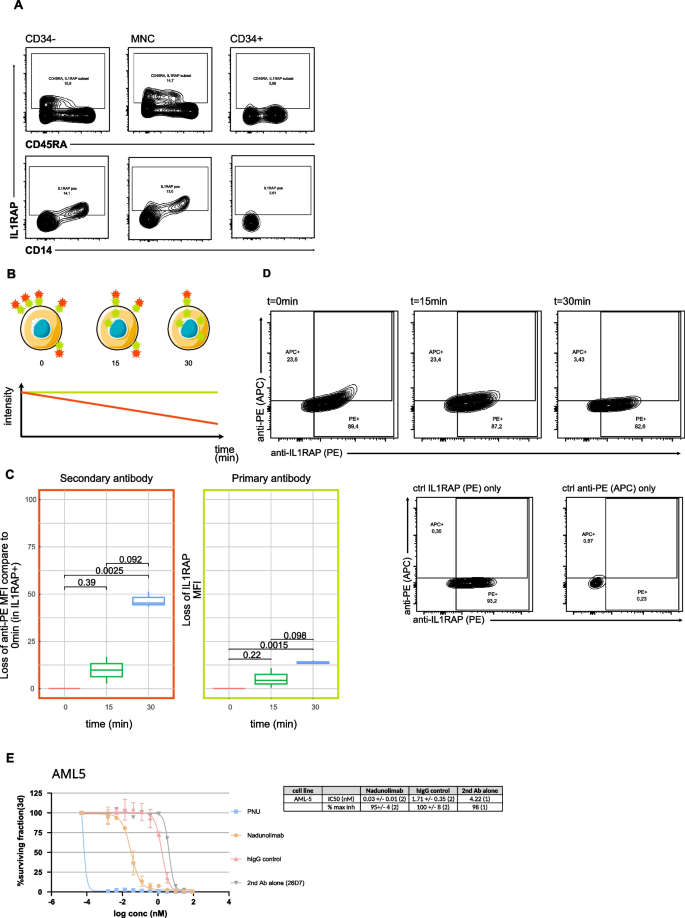
实验所用关键产品:内化实验采用R&D Systems的抗IL1RAP-PE抗体(货号FAB676P)、BioLegend的抗PE-APC抗体(货号408107);ADC抑制实验采用Nadunolimab(Cantargia公司)、PNU偶联的抗人Fc抗体,细胞活力检测采用Promega的CellTiter-Glo®试剂盒。
4. Biomarker研究及发现成果
Biomarker定位:本研究发现的Biomarker为IL1RAP,属于细胞表面跨膜蛋白,筛选逻辑为通过整合表面蛋白质组、bulk转录组和单细胞转录组的多组学分析,从100例AML样本的表面蛋白质组数据中筛选出差异表达蛋白,结合正常组织和造血细胞的表达数据缩小候选范围,再通过单细胞转录组和流式细胞术验证其在NKt-AML中的特异性表达。
研究过程详述:IL1RAP的表达来源为原发性NKt-AML细胞的表面,验证方法包括流式细胞术检测细胞表面蛋白表达、多组学数据分析转录和蛋白水平表达,特异性表现为在NKt-AML的原始细胞(包括类造血干细胞的白血病细胞)中高表达,而在正常骨髓造血干细胞中低表达,流式细胞术显示NKt-AML中表达IL1RAP的白血病细胞比例显著高于其他AML亚型(n=19,P<0.01);敏感性方面,在NKt-AML中IL1RAP的表达具有较高的一致性,所有6例单细胞测序样本的白血病细胞均高表达IL1RAP。
核心成果提炼:IL1RAP作为NKt-AML的预后Biomarker,高表达与患者不良总生存率(HR=1.61,95% CI 1.17-2.24,P<0.01)和无复发生存率(HR=1.58,95% CI 1.08-2.30,P=0.02)相关,同时可预测造血干细胞移植无响应(HSCT患者HR=2.82,95% CI 1.35-5.89,P<0.01);创新性在于首次发现IL1RAP是NKt-AML的特异性免疫治疗靶点,且其内化特性使其适合作为ADC靶点,为NKt-AML的精准治疗提供了新的方向,同时该靶点在t(8;21)、t(6;9)等其他AML亚型中也有较高表达,具有潜在的广谱应用价值。
