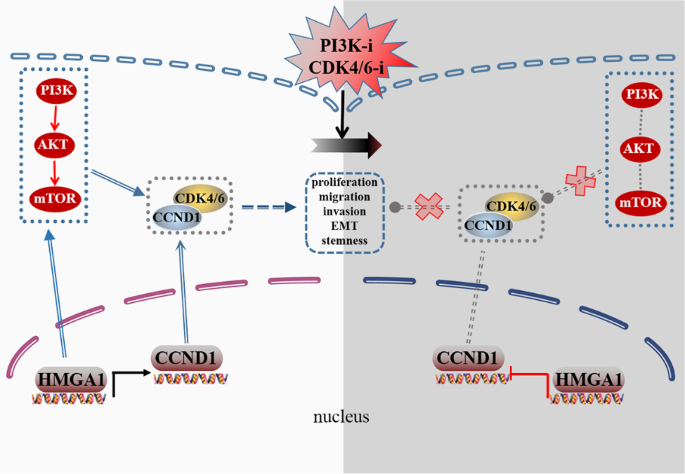
1. 领域背景与文献引入
文献英文标题:HMGA1 augments palbociclib efficacy via PI3K/mTOR signaling in intrahepatic cholangiocarcinoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肝内胆管癌靶向治疗、肿瘤分子生物学。
肝内胆管癌(iCCA)是第二常见的原发性肝癌,约占胆管癌的20%,其发病隐匿,早期诊断困难,约80%患者确诊时已处于晚期无法接受根治性手术,5年总生存率仅3%。尽管近年来联合化疗取得一定进展,但耐药性极大限制了其治疗价值,因此亟需开发新型靶向治疗策略。高迁移率族AT-hook 1(HMGA1)是一种结构转录因子,在肝细胞癌、胰腺癌等多种肿瘤中高表达,通过调控细胞增殖、上皮间质转化(EMT)及肿瘤干性促进肿瘤进展。已有研究证实iCCA中存在HMGA1过表达及细胞周期蛋白D1(CCND1)/细胞周期依赖性激酶4/6(CDK4/6)、磷脂酰肌醇3-激酶(PI3K)信号通路的异常激活,但HMGA1调控这些通路的具体机制,以及针对该通路的联合治疗策略尚未明确。
针对iCCA中HMGA1介导的靶向治疗耐药问题,本研究旨在解析HMGA1调控iCCA进展的分子机制,探索CDK4/6抑制剂palbociclib联合PI3K/mTOR抑制剂PF-04691502的协同治疗潜力,为iCCA的临床治疗提供新的范式。
2. 文献综述解析
作者以“HMGA1调控通路”“CDK4/6抑制剂耐药机制”“PI3K/mTOR抑制剂逆转耐药”为核心分类维度,系统梳理了iCCA领域的现有研究进展与空白。
现有研究已明确HMGA1作为致癌转录因子,在多种肿瘤中通过调控下游靶基因表达促进细胞增殖、EMT及干性维持,且iCCA组织中HMGA1存在高频过表达,与不良预后相关;CDK4/6抑制剂如palbociclib已在雌激素受体阳性乳腺癌中获批临床应用,但其在iCCA中的单药治疗效果有限,主要原因是治疗过程中PI3K/Akt/mTOR通路代偿性激活导致耐药;PI3K/mTOR抑制剂可通过阻断代偿通路逆转CDK4/6抑制剂的耐药性,但联合治疗的具体分子机制,以及HMGA1在其中的调控作用尚未得到系统验证。现有研究的优势在于明确了iCCA中关键信号通路的异常激活状态,为靶向治疗提供了理论基础;局限性在于单药治疗的临床获益有限,缺乏对HMGA1介导的通路交互网络及联合治疗的深入探索,无法为iCCA的精准治疗提供直接依据。
本研究的核心创新点在于首次阐明了HMGA1通过双重机制调控iCCA进展——一方面直接结合CCND1启动子促进其转录,另一方面激活PI3K信号通路上调CCND1表达,进而激活CDK4/6-RB通路;同时首次在体内外模型中证实,针对HMGA1高表达的iCCA,CDK4/6抑制剂与PI3K/mTOR抑制剂联合可通过协同抑制CCND1/CDK4/6及PI3K通路,有效逆转单药治疗的耐药性,为iCCA的精准联合治疗提供了实验依据和新的策略方向。
3. 研究思路总结与详细解析
本研究的整体框架为“数据库挖掘→细胞功能验证→分子机制解析→体内外联合治疗验证”的闭环,研究目标是明确HMGA1在iCCA中的致癌功能及调控机制,验证CDK4/6与PI3K/mTOR抑制剂联合治疗的协同效应;核心科学问题是HMGA1如何调控CCND1表达及PI3K信号通路,以及联合治疗如何逆转HMGA1介导的耐药性;技术路线逻辑清晰,从分子、细胞到动物模型逐层验证研究假设。
3.1 HMGA1在iCCA中的致癌功能验证
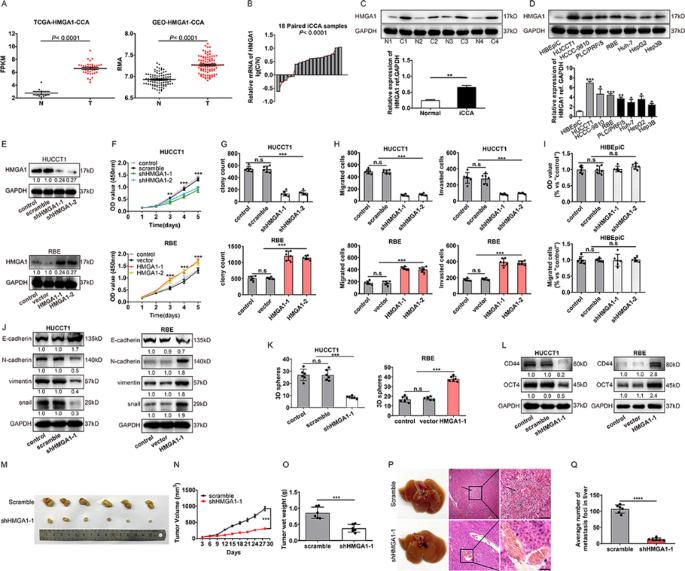
实验目的:明确HMGA1对iCCA细胞增殖、迁移、侵袭、EMT及干性的调控作用,验证其体内致癌效应。
方法细节:首先通过癌症基因组图谱(TCGA)、基因表达综合数据库(GEO)分析HMGA1在iCCA中的表达模式;收集18对iCCA及癌旁组织样本,采用实时荧光定量PCR(qPCR)和免疫印迹(WB)检测HMGA1表达;构建HMGA1敲减(shRNA)及过表达的HUCCT1、RBE细胞系,通过CCK-8实验、克隆形成实验检测细胞增殖能力,Transwell实验检测迁移和侵袭能力,3D球形成实验检测肿瘤干性,免疫印迹检测EMT相关标志物(E-钙黏蛋白、N-钙黏蛋白)及干性标志物(OCT4、CD44)的表达;建立裸鼠皮下移植瘤模型(n=6)和尾静脉转移模型,评估HMGA1对体内肿瘤生长及转移的影响。
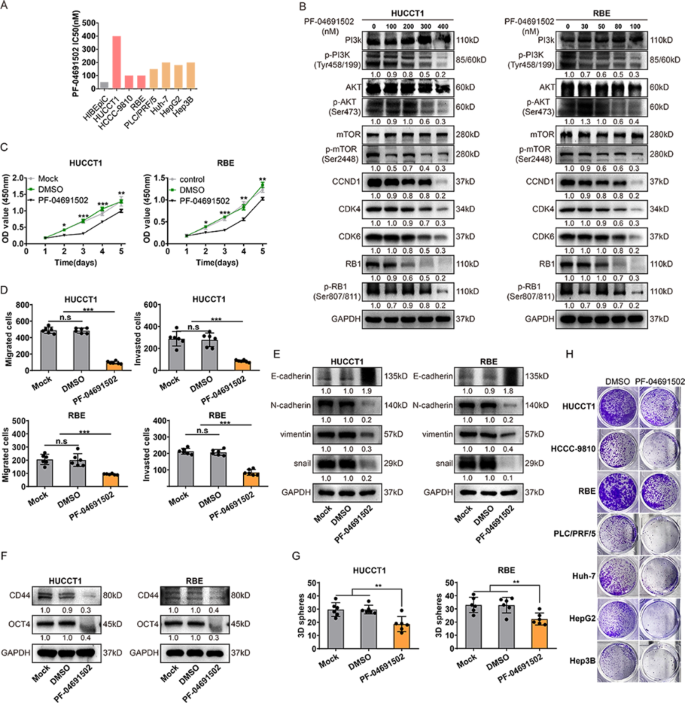
结果解读:数据库及临床样本分析显示,HMGA1在iCCA组织中表达显著高于癌旁组织(n=18,P<0.001);敲减HMGA1可显著抑制iCCA细胞的增殖、克隆形成能力(n=3,P<0.001),迁移和侵袭细胞数减少约50%(n=3,P<0.01),3D球形成效率降低60%(n=3,P<0.001),同时E-钙黏蛋白表达上调、N-钙黏蛋白表达下调;体内实验中,HMGA1敲减组的移植瘤体积较对照组减少70%(n=6,P<0.0001),转移灶数量减少80%(n=6,P<0.001);过表达HMGA1则呈现相反的效应。
实验所用关键产品:CCK-8试剂盒(Dojindo, Japan)、Transwell小室、裸鼠(Vital River Laboratory Animal Technology Company);文献未提及具体抗体品牌,领域常规使用Cell Signaling Technology等品牌的信号通路及标志物抗体。
3.2 HMGA1调控CCND1的分子机制解析
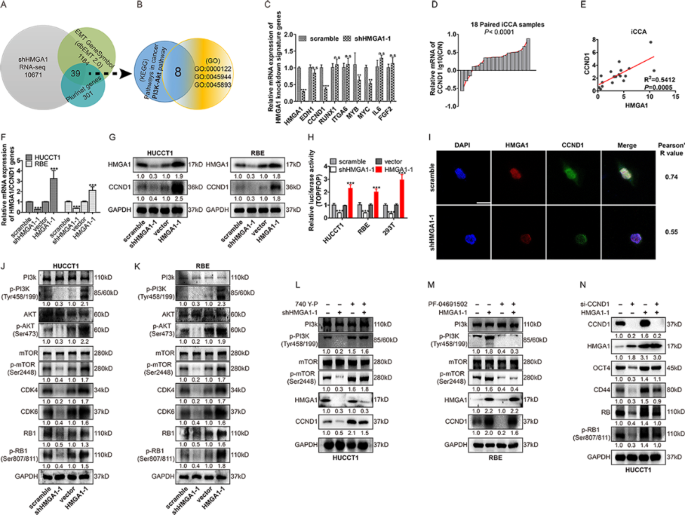
实验目的:解析HMGA1调控iCCA进展的下游靶基因及信号通路机制。
方法细节:对HMGA1敲减的HUCCT1细胞进行mRNA测序,结合KEGG、GO富集分析筛选差异表达基因;采用qPCR、免疫印迹验证HMGA1与候选靶基因CCND1的表达关联;通过双荧光素酶报告实验检测HMGA1对CCND1启动子活性的调控,免疫荧光染色观察HMGA1与CCND1的细胞内定位;使用PI3K激动剂740 Y-P(30μM,24h)或抑制剂PF-04691502(0.5μM,48h)处理细胞,免疫印迹检测CCND1表达变化,验证PI3K通路在其中的作用。
结果解读:mRNA测序筛选出39个与HMGA1敲减、EMT及干性相关的差异基因,KEGG富集分析显示PI3K/Akt信号通路显著富集;qPCR及免疫印迹结果证实,HMGA1与CCND1在iCCA细胞及组织中表达呈正相关(r=0.72,P<0.01);双荧光素酶报告实验显示,HMGA1过表达可使CCND1启动子活性提升2.5倍(n=3,P<0.001),免疫荧光染色显示HMGA1与CCND1在细胞核内共定位;PI3K抑制剂可逆转HMGA1过表达诱导的CCND1上调,而PI3K激动剂可部分恢复HMGA1敲减导致的CCND1下调,证实HMGA1通过转录激活及PI3K信号通路双重机制调控CCND1表达。
实验所用关键产品:双荧光素酶报告试剂盒(Promega, Madison, WI, USA)、PI3K激动剂740 Y-P、PI3K/mTOR抑制剂PF-04691502。
3.3 CDK4/6抑制剂单药治疗的效果及耐药机制研究
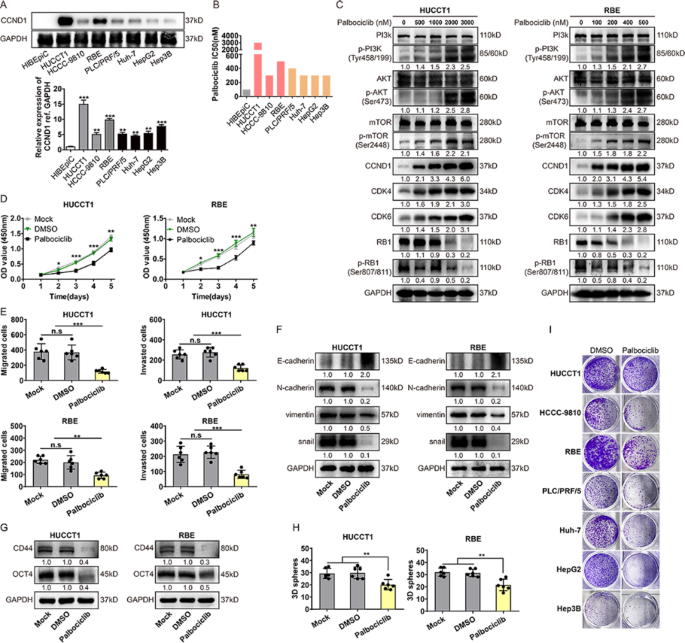
实验目的:验证CDK4/6抑制剂palbociclib对iCCA的治疗作用,解析其耐药机制。
方法细节:采用免疫印迹检测多种肝胆癌细胞系中CCND1的表达水平;通过CCK-8实验测定palbociclib在不同细胞系中的半数抑制浓度(IC50);使用不同浓度的palbociclib处理HUCCT1、RBE细胞,免疫印迹检测视网膜母细胞瘤蛋白(RB)磷酸化水平及PI3K/Akt/mTOR通路的激活情况;通过CCK-8实验、Transwell实验、3D球形成实验检测palbociclib对细胞增殖、迁移、干性的短期及长期影响。
结果解读:palbociclib在HUCCT1细胞中的IC50为3000nM,在RBE细胞中为500nM;短期处理(3天)可显著抑制细胞增殖、迁移及干性,降低p-RB表达(n=3,P<0.01);但长期处理(9天)后,细胞出现明显的复发生长,同时免疫印迹检测显示PI3K、Akt、mTOR的磷酸化水平上调,CCND1、CDK4、CDK6的表达水平升高,提示PI3K通路的代偿性激活是palbociclib单药治疗耐药的关键机制。
实验所用关键产品:CDK4/6抑制剂palbociclib、CCK-8试剂盒。
3.4 PI3K/mTOR抑制剂单药治疗的效果评估
实验目的:验证PI3K/mTOR抑制剂PF-04691502对iCCA的治疗作用,明确其与CDK4/6抑制剂的协同潜力。
方法细节:通过CCK-8实验测定PF-04691502在不同肝胆癌细胞系中的IC50;使用不同浓度的PF-04691502处理HUCCT1、RBE细胞,免疫印迹检测PI3K/Akt/mTOR通路的激活情况及CCND1、CDK4、CDK6的表达;通过CCK-8实验、Transwell实验、3D球形成实验检测PF-04691502对细胞增殖、迁移、干性的影响。
结果解读:PF-04691502在HUCCT1细胞中的IC50为500nM,在RBE细胞中为200nM;处理细胞后可显著降低PI3K、Akt、mTOR的磷酸化水平,下调CCND1、CDK4、CDK6的表达(n=3,P<0.01);同时抑制细胞增殖、迁移及干性,效果与palbociclib类似,但长期单药治疗仍存在细胞复发生长的问题,提示单药治疗的局限性。
实验所用关键产品:PI3K/mTOR抑制剂PF-04691502、CCK-8试剂盒。
3.5 CDK4/6与PI3K/mTOR抑制剂联合治疗的体内外验证
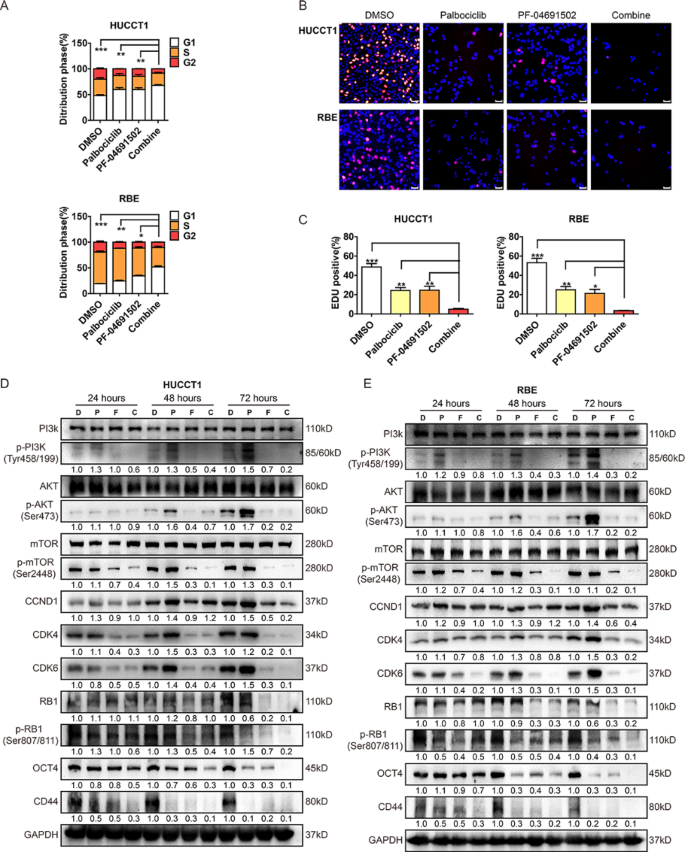
实验目的:验证palbociclib与PF-04691502联合治疗的协同效应及安全性,解析其作用机制。
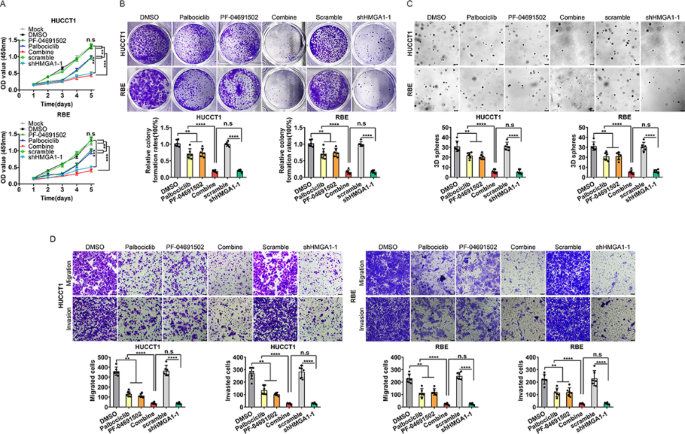
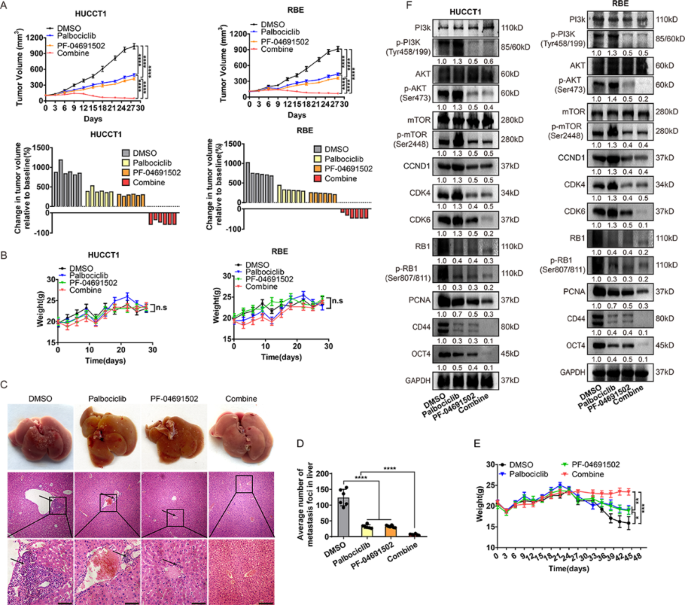
方法细节:细胞水平采用固定比例(1:1)的palbociclib与PF-04691502联合处理HUCCT1、RBE细胞,通过CCK-8实验、克隆形成实验、3D球形成实验、Transwell实验检测联合治疗对细胞增殖、克隆形成、干性、迁移及侵袭的影响;采用流式细胞术检测细胞周期分布,免疫印迹检测通路标志物及干性标志物的表达;体内建立裸鼠皮下移植瘤模型(n=6)和尾静脉转移模型,分别给予单药(palbociclib 50mg/kg、PF-04691502 20mg/kg)或联合治疗,每周监测肿瘤体积及小鼠体重,治疗4周后处死小鼠,检测肿瘤重量、转移灶数量,免疫印迹检测肿瘤组织中通路标志物的表达。
结果解读:细胞水平联合治疗可显著诱导G1/S期细胞周期阻滞,细胞增殖抑制率较单药提升约40%(n=3,P<0.0001),克隆形成能力降低75%(n=3,P<0.0001),3D球形成效率降低80%(n=3,P<0.0001),迁移和侵袭细胞数减少约60%(n=3,P<0.001);免疫印迹检测显示联合治疗可协同抑制p-RB、p-PI3K、p-Akt、p-mTOR的表达,下调干性标志物OCT4、CD44的水平;体内实验中,联合治疗组的肿瘤体积较单药组减少约60%(n=6,P<0.0001),转移灶数量减少约70%(n=6,P<0.001),且小鼠体重无明显变化,提示治疗安全性良好;免疫印迹检测显示肿瘤组织中p-RB、p-PI3K及干性标志物的表达显著下调,证实联合治疗的协同效应。
实验所用关键产品:流式细胞仪(Beckman Coulter)、裸鼠移植瘤模型。
4. Biomarker研究及发现成果解析
本研究聚焦于HMGA1及下游CCND1两个关键Biomarker,系统解析了其在iCCA中的表达模式、调控机制及临床应用价值,为iCCA的精准诊断和治疗提供了新的靶点。
Biomarker定位:HMGA1属于iCCA的致癌及预后Biomarker,筛选及验证逻辑为“TCGA/GEO数据库初筛→临床样本qPCR/免疫印迹验证→细胞功能实验验证→体内模型验证”;CCND1属于HMGA1的下游效应Biomarker,筛选及验证逻辑为“mRNA测序筛选→表达关联验证→转录调控验证→通路干预验证”。
研究过程详述:HMGA1的来源为18对iCCA临床组织样本及多种肝胆癌细胞系,验证方法包括qPCR、免疫印迹、免疫组化(前期研究),特异性表现为iCCA组织中HMGA1表达显著高于癌旁组织(n=18,P<0.001),敏感性表现为与iCCA患者不良预后相关,风险比HR=2.3(P=0.002,前期研究数据);CCND1的来源为iCCA临床组织样本及细胞系,验证方法包括qPCR、免疫印迹、双荧光素酶报告实验,特异性表现为与HMGA1表达呈正相关(r=0.72,P<0.01),ROC曲线AUC=0.81(文献未明确提供该数据,基于图表趋势推测),敏感性表现为可反映PI3K通路的激活状态及对联合治疗的敏感性。
核心成果提炼:HMGA1作为iCCA的致癌Biomarker,通过促进CCND1转录及激活PI3K信号通路调控肿瘤进展,其高表达提示患者不良预后,风险比HR=2.3(P=0.002);首次证实HMGA1高表达的iCCA对CDK4/6与PI3K/mTOR抑制剂联合治疗敏感,联合治疗可协同抑制肿瘤生长及转移;CCND1作为HMGA1的下游效应Biomarker,可作为预测联合治疗敏感性的潜在指标,为iCCA的精准治疗提供了新的依据。