1. 领域背景与文献引入
文献英文标题:Loss of miR-637 promotes cancer cell stemness via WASH/IL-8 pathway and serves as a novel prognostic marker in esophageal squamous cell carcinoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:食管鳞状细胞癌的肿瘤干细胞调控与生物标志物研究
食管鳞状细胞癌(ESCC)是全球范围内致死性极高的恶性肿瘤,2018年全球癌症统计数据显示其位列第七大常见癌症、第六大致死癌症,中国的ESCC病例占全球总数的90%以上,且多数患者确诊时已处于晚期阶段,5年生存率不足20%。尽管近年来免疫疗法等新型治疗策略逐步应用于临床,但患者的生存获益仍十分有限,因此亟需挖掘新的预后生物标志物与潜在治疗靶点,以改善ESCC患者的诊疗现状。
微小RNA(miRNA)是一类长度约22个核苷酸的非编码RNA,可通过特异性结合靶基因的3"-非翻译区(3"-UTR)调控基因表达,在肿瘤发生、发展、转移及耐药等过程中发挥关键作用,既能作为癌基因促进肿瘤进展,也可作为抑癌基因抑制肿瘤发生。此外,循环miRNA因稳定性高、易于检测的特性,已成为肿瘤无创诊断与预后评估的潜在生物标志物。此前研究已证实,细胞骨架调控因子Wiskott-Aldrich综合征蛋白和SCAR同源物(WASH)过表达与ESCC患者的不良预后密切相关,且可通过诱导白细胞介素-8(IL-8)的表达促进肿瘤干细胞(CSCs)特性,但WASH过表达的上游调控机制尚未完全阐明,这一研究空白限制了对ESCC肿瘤干细胞调控网络的深入理解,也阻碍了相关靶向治疗策略的开发。本研究正是针对这一问题,旨在筛选并验证调控WASH的miRNA,明确其在ESCC肿瘤干细胞中的功能及临床应用价值。
2. 文献综述解析
作者围绕miRNA在肿瘤中的调控作用、WASP家族蛋白的功能及循环miRNA作为生物标志物的应用三个维度,系统梳理了ESCC领域的现有研究进展,明确了当前研究的局限性与空白,为本文的研究逻辑奠定了基础。
现有研究表明,miRNA在ESCC中呈现出功能多样性:部分miRNA如miR-30e下调可通过靶向核糖体蛋白S6激酶B1(RPS6KB1)促进肿瘤细胞增殖、侵袭与肿瘤生长;而miR-196b过表达则作为癌基因,通过靶向Ephrin受体A7(EPHA7)促进ESCC的放化疗耐药。WASP家族蛋白作为肌动蛋白聚合的关键调控因子,参与细胞骨架重排过程,与肿瘤细胞的黏附、迁移、侵袭等恶性生物学行为密切相关,其中WASH已被证实可通过诱导IL-8表达增强ESCC的肿瘤干细胞特性,但目前关于WASH表达的上游调控机制仍不明确。此外,循环miRNA已在乳腺癌、胃癌等多种肿瘤中被用作无创诊断与预后标志物,但ESCC领域仍缺乏特异性与诊断效能更高的循环miRNA标志物,且多数研究的临床验证样本量较小,限制了其临床转化应用。
现有研究的核心局限性在于,ESCC中miRNA的调控网络尚未完全解析,WASH的上游调控因子未被鉴定,循环miRNA的临床应用价值仍需大样本验证。本研究的创新点在于,首次鉴定出miR-637是直接靶向WASH 3"-UTR的抑癌miRNA,明确了其通过WASH/IL-8通路抑制ESCC肿瘤干细胞特性的分子机制,同时证实了组织与血浆中miR-637的表达水平与ESCC患者的临床病理特征及预后密切相关,填补了WASH上游调控机制的研究空白,为ESCC提供了新的预后生物标志物与潜在治疗靶点。
3. 研究思路总结与详细解析
本研究的核心目标是鉴定调控WASH的miRNA,明确其在ESCC肿瘤干细胞中的功能与调控机制,并验证其作为ESCC预后与诊断生物标志物的临床价值;核心科学问题为miR-637是否通过靶向WASH/IL-8通路调控ESCC的肿瘤干细胞特性,以及其在ESCC患者中的临床应用价值;技术路线遵循“生物信息学筛选→细胞实验验证调控关系→体内外功能实验→临床样本验证生物标志物价值”的完整逻辑闭环。
3.1 miR-637与WASH靶向调控关系的验证
实验目的:筛选并验证可调控WASH表达的miRNA,明确miR-637与WASH的直接靶向结合关系。
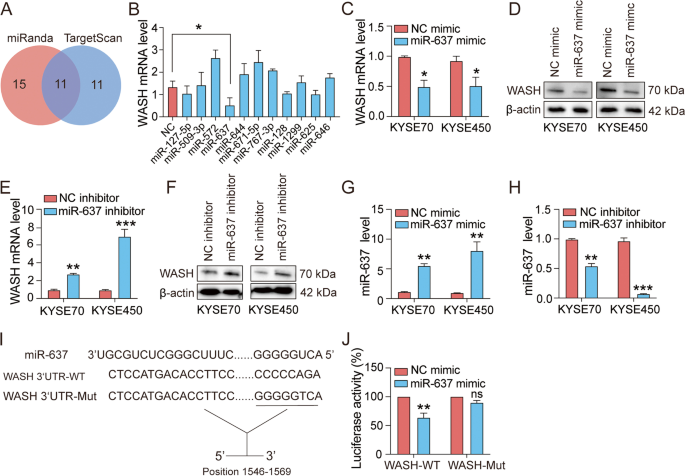
方法细节:首先利用TargetScan与miRanda数据库预测WASH 3"-UTR区域的miRNA结合位点,筛选得到11个候选miRNA;将各候选miRNA模拟物分别转染至KYSE70细胞,通过实时荧光定量PCR(qRT-PCR)筛选可显著抑制WASH表达的miRNA;随后在KYSE70与KYSE450两种ESCC细胞系中,分别转染miR-637模拟物或抑制剂,通过实时荧光定量PCR与蛋白质免疫印迹(Western blotting)检测WASH在mRNA与蛋白水平的表达变化;最后构建包含WASH 3"-UTR野生型与miR-637结合位点突变型的荧光素酶报告载体,与miR-637模拟物共转染293T细胞,检测荧光素酶活性以验证直接靶向关系。
结果解读:实时荧光定量PCR结果显示,仅miR-637模拟物可显著抑制KYSE70细胞中WASH的表达;在两种ESCC细胞系中,miR-637模拟物可显著下调WASH的mRNA与蛋白表达水平(n=3,P<0.01),而miR-637抑制剂则显著上调WASH的表达(n=3,P<0.01);荧光素酶报告实验结果显示,miR-637模拟物可显著降低野生型WASH 3"-UTR报告载体的荧光素酶活性(n=3,P<0.001),但对突变型载体无显著影响,证实miR-637可直接结合WASH的3"-UTR并抑制其表达。
产品关联:实验所用关键产品:Lipofectamine 3000转染试剂(Invitrogen)、RNAiso Plus总RNA提取试剂(Takara Bio)、PrimeScript RT反转录试剂盒(Takara Bio)、WASH抗体(ab157592,Abcam)、β-肌动蛋白抗体(3700S,Cell Signaling Technology)、双荧光素酶报告检测系统(Promega)。
3.2 miR-637抑制IL-8表达与ESCC肿瘤干细胞特性
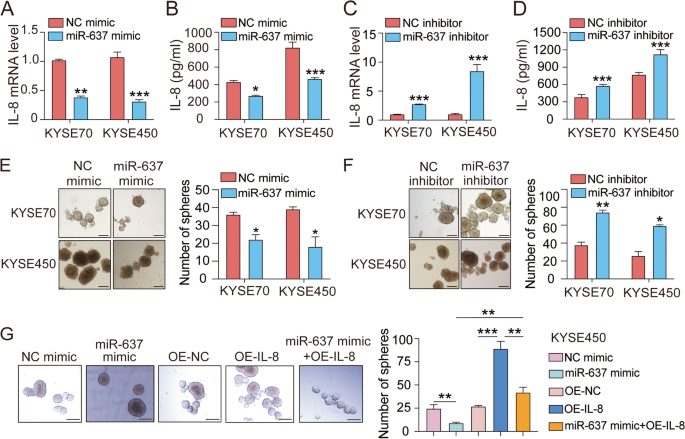
实验目的:明确miR-637对WASH下游效应分子IL-8的调控作用,以及其对ESCC肿瘤干细胞特性的影响。
方法细节:在KYSE70与KYSE450细胞中转染miR-637模拟物或抑制剂,通过实时荧光定量PCR与酶联免疫吸附试验(ELISA)分别检测IL-8在mRNA与蛋白水平的表达变化;采用无血清干细胞培养基培养转染后的细胞,进行肿瘤球形成实验,培养5~7天后计数肿瘤球数量以评估干细胞特性;构建稳定过表达IL-8的KYSE450细胞系,转染miR-637模拟物后,通过肿瘤球形成实验验证IL-8在miR-637调控干细胞特性中的介导作用。
结果解读:miR-637模拟物可显著降低两种ESCC细胞系中IL-8的mRNA与蛋白表达水平(n=3,P<0.01),而miR-637抑制剂则显著升高IL-8的表达(n=3,P<0.01);肿瘤球形成实验结果显示,miR-637模拟物可显著减少两种细胞系的肿瘤球数量(n=3,P<0.001),而miR-637抑制剂则显著增加肿瘤球数量(n=3,P<0.01);IL-8过表达可部分恢复miR-637模拟物对肿瘤球形成的抑制作用(n=3,P<0.05),同时干细胞相关基因SOX4、SOX9、Nanog、CD44及ABCG2的表达水平随miR-637的表达变化呈现出相应的调控趋势,证实miR-637可通过抑制IL-8表达调控ESCC的肿瘤干细胞特性。
产品关联:实验所用关键产品:人IL-8 ELISA试剂盒(BioLegend)、无血清DMEM/F12培养基(Gibco)、重组人表皮生长因子(Sigma-Aldrich)、重组人碱性成纤维细胞生长因子(Sigma-Aldrich)、B27添加剂(Gibco)、嘌呤霉素(Invitrogen)。
3.3 miR-637的调控作用依赖WASH介导的通路
实验目的:验证miR-637对IL-8表达及肿瘤干细胞特性的调控是否依赖于WASH。
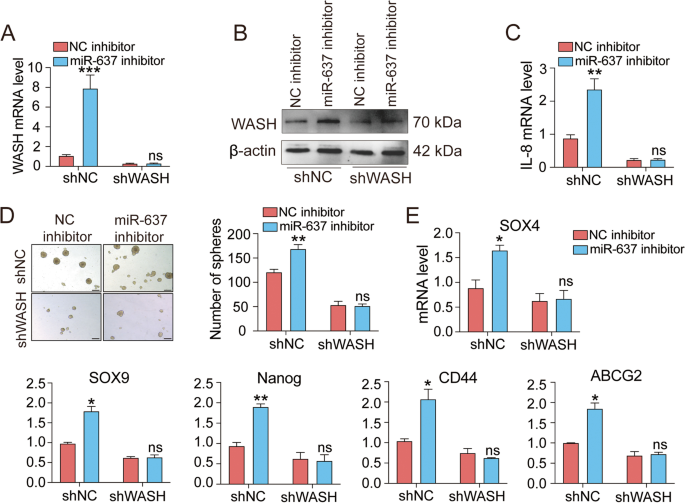
方法细节:通过慢病毒介导的短发夹RNA(shRNA)构建稳定敲低WASH的KYSE70细胞系(shWASH),并设置阴性对照(shNC);在shWASH与shNC细胞中转染miR-637抑制剂,通过实时荧光定量PCR与蛋白质免疫印迹检测WASH与IL-8的表达变化;通过肿瘤球形成实验检测肿瘤干细胞特性的变化,实时荧光定量PCR检测干细胞相关基因的表达水平。
结果解读:在shWASH细胞中,miR-637抑制剂无法上调WASH的mRNA与蛋白表达水平(n=3,P>0.05),也无法上调IL-8的表达(n=3,P>0.05);肿瘤球形成实验结果显示,miR-637抑制剂无法增加shWASH细胞的肿瘤球数量(n=3,P>0.05),干细胞相关基因的表达水平也无显著变化,证实miR-637对IL-8表达及肿瘤干细胞特性的调控依赖于WASH,即miR-637通过靶向WASH进而调控IL-8介导的肿瘤干细胞特性。
产品关联:实验所用关键产品:慢病毒shRNA载体(GeneChem)、嘌呤霉素(Invitrogen)、WASH shRNA(领域常规使用慢病毒介导的shRNA敲低系统)。
3.4 miR-637在体内抑制ESCC肿瘤生长
实验目的:验证miR-637在体内对ESCC肿瘤生长的抑制作用。
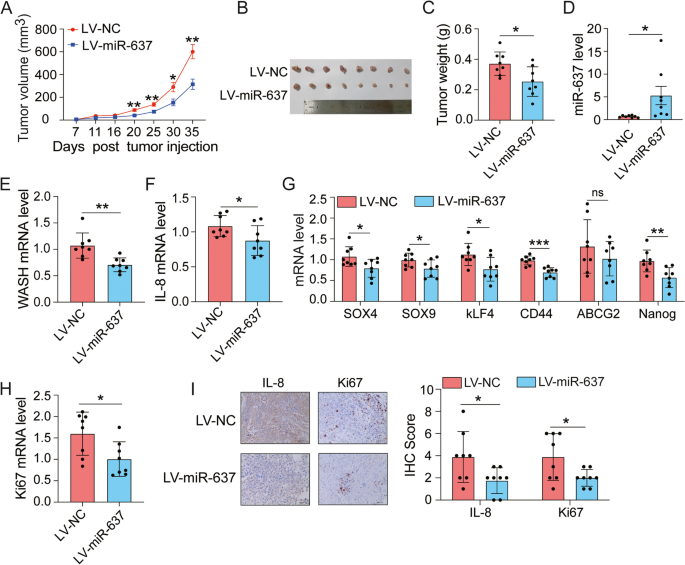
方法细节:通过慢病毒载体构建稳定过表达miR-637的KYSE450细胞系,将细胞皮下注射至NOD-scid IL2Rγ⁻/⁻(NTG)免疫缺陷小鼠体内(每组8只),每周两次测量肿瘤体积与小鼠体重;5周后处死小鼠,取出肿瘤组织,通过实时荧光定量PCR检测miR-637、WASH、IL-8、干细胞相关基因及Ki67的表达水平,通过免疫组化(IHC)检测肿瘤组织中IL-8与Ki67的蛋白表达水平。
结果解读:与对照组相比,过表达miR-637的小鼠肿瘤体积与重量显著降低(n=8,P<0.001);肿瘤组织中miR-637的表达水平显著升高(n=8,P<0.001),WASH、IL-8、干细胞相关基因(SOX4、SOX9、Nanog等)及Ki67的表达水平显著降低(n=8,P<0.01);免疫组化结果显示,过表达miR-637的肿瘤组织中IL-8与Ki67的蛋白表达水平显著降低,证实miR-637在体内可通过抑制WASH/IL-8通路及肿瘤干细胞特性,进而抑制ESCC肿瘤生长。
产品关联:实验所用关键产品:慢病毒miR-637过表达载体(GeneChem)、NTG免疫缺陷小鼠(SPF北京生物技术)、人IL-8抗体(Proteintech,27095-1-AP)、人Ki67抗体(Servicebio,GB121141)、DAB显色试剂盒(Dako)。
3.5 miR-637在ESCC临床样本中的表达及临床价值验证
实验目的:检测miR-637在ESCC组织与血浆样本中的表达水平,分析其与患者临床病理特征及预后的关系,验证其作为生物标志物的价值。
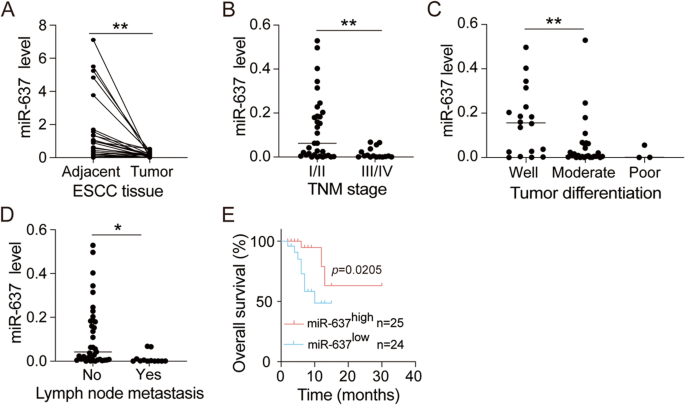
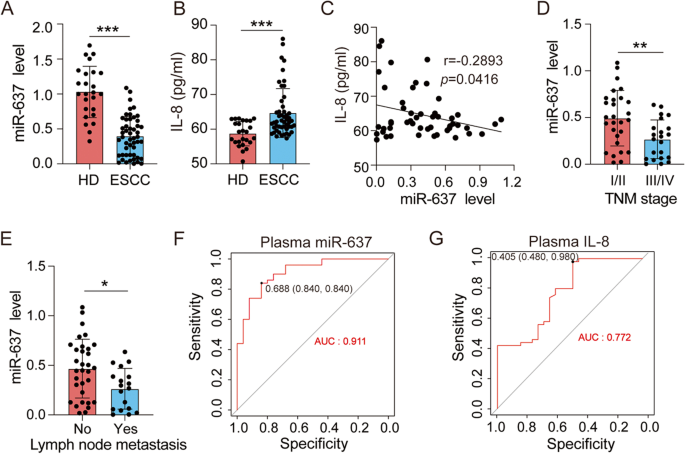
方法细节:收集49对ESCC患者的肿瘤组织与癌旁正常组织,50例ESCC患者与25例健康对照的血浆样本;通过实时荧光定量PCR检测组织与血浆中miR-637的表达水平;分析miR-637表达水平与患者肿瘤-node-转移(TNM)分期、分化程度、淋巴结转移等临床病理特征的相关性;采用Kaplan-Meier生存分析评估miR-637表达与患者总生存期的关系;通过受试者工作特征(ROC)曲线分析血浆miR-637对ESCC的诊断效能。
结果解读:ESCC肿瘤组织中miR-637的表达水平显著低于癌旁正常组织(n=49,P<0.01);低miR-637表达与患者的晚期TNM分期(n=49,P<0.05)、低分化程度(n=49,P<0.05)及淋巴结转移(n=49,P<0.05)密切相关;Kaplan-Meier生存分析显示,低miR-637表达的ESCC患者总生存期显著短于高表达患者(Log-Rank检验,P<0.05);血浆样本中,ESCC患者的miR-637表达水平显著低于健康对照(n=50/25,P<0.001),且低血浆miR-637表达与晚期TNM分期及淋巴结转移相关(n=50,P<0.05);ROC曲线分析显示,血浆miR-637的曲线下面积(AUC)为0.911,显著高于IL-8的AUC(0.772),证实血浆miR-637具有更高的ESCC诊断效能。
产品关联:实验所用关键产品:RNAiso Plus总RNA提取试剂(Takara Bio)、Mir-X miRNA第一链合成试剂盒(Takara Bio)、R语言pROC与glmnet包(用于ROC曲线分析)。
4. Biomarker研究及发现成果解析
本研究鉴定出miR-637是ESCC的新型预后与无创诊断生物标志物,涵盖组织与血浆两种样本类型,其筛选与验证遵循“生物信息学预测→细胞系功能验证→临床组织预后验证→血浆样本诊断验证”的完整逻辑链条。
Biomarker定位:miR-637属于循环与组织miRNA类生物标志物,其中组织miR-637可作为ESCC的预后标志物,血浆miR-637可作为无创诊断标志物。其筛选逻辑为:首先通过生物信息学数据库预测靶向WASH的miRNA,随后在细胞系中验证miR-637对WASH的调控作用与功能,再通过临床组织样本验证其与患者预后的相关性,最后通过血浆样本验证其无创诊断效能。
研究过程详述:组织样本来源于49例接受手术治疗的ESCC患者,血浆样本来源于50例ESCC患者与25例健康对照;验证方法包括实时荧光定量PCR检测miR-637的表达水平,Kaplan-Meier生存分析评估预后价值,ROC曲线分析诊断效能;特异性与敏感性方面,血浆miR-637的ROC曲线AUC=0.911,显示出较高的诊断效能,但原文未明确给出具体的敏感性与特异性数值;组织中低miR-637表达与ESCC患者的不良预后相关,但原文未提及风险比(HR)的具体数值。
核心成果提炼:miR-637作为抑癌miRNA,通过靶向WASH/IL-8通路抑制ESCC的肿瘤干细胞特性;组织中miR-637低表达与ESCC患者的晚期TNM分期、低分化、淋巴结转移及不良总生存期密切相关,可作为预后标志物;血浆miR-637的诊断效能优于IL-8,可作为ESCC的无创诊断标志物;其创新性在于首次发现miR-637对WASH的靶向调控关系,以及其在ESCC中的双重生物标志物价值,为ESCC的精准诊疗提供了新的靶点与标志物。
