1. 领域背景与文献引入
文献英文标题:Histamine N-methyltransferase (HNMT) as a potential auxiliary biomarker for predicting adaptability to anti-HER2 drug treatment in breast cancer patients;发表期刊:Biomarker Research;影响因子:未公开;研究领域:乳腺癌精准诊疗与抗HER2治疗生物标志物研究
乳腺癌是全球女性最常见的恶性肿瘤,其中人表皮生长因子受体2阳性(HER2+)亚型占所有病例的14%-30%,具有侵袭性强、预后差的特点。曲妥珠单抗等抗HER2治疗的应用显著改善了HER2+患者的生存结局,但临床数据显示,仍有高达23%的早期患者在接受曲妥珠单抗联合化疗后10年内复发,同时部分HER2低表达患者却能从新型抗体药物偶联物(ADC)如德曲妥珠单抗(T-Dxd)治疗中获益,这表明仅依赖HER2作为单一诊断标志物预测抗HER2药物疗效存在明显局限性。当前领域研究热点聚焦于寻找可用于临床的辅助生物标志物,以实现抗HER2治疗的精准患者分层,但HER2低表达患者的治疗响应机制及对应的蛋白水平生物标志物仍未明确。
本文针对这一核心研究空白,提出组胺N-甲基转移酶(HNMT)与HER2的相互作用可作为曲妥珠单抗响应的辅助预测因子,同时HNMT对HER2表达的转录调控机制可能解释HER2低表达患者对T-Dxd的响应现象,为抗HER2治疗的精准筛选提供了新的靶点与理论依据,具有重要的临床转化价值。
2. 文献综述解析
本文综述围绕抗HER2治疗的临床局限性、现有生物标志物研究的不足及蛋白相互作用在乳腺癌耐药中的作用展开,通过分类梳理现有研究的优势与缺陷,凸显HNMT作为辅助生物标志物的创新性与必要性。
现有研究中,抗HER2治疗已形成包括抗体药物(曲妥珠单抗、帕妥珠单抗)、小分子抑制剂(拉帕替尼、奈拉替尼)、ADC(T-DM1、T-Dxd)在内的完整治疗体系,其中T-Dxd为HER2低表达患者带来了新的治疗选择,但单一HER2标志物无法有效区分治疗响应者与非响应者:部分HER2阳性患者出现原发性或继发性耐药,而部分HER2低表达患者却能从T-Dxd治疗中获益。生物标志物研究方面,基于基因组和蛋白质组分析的预测模型逐渐兴起,但多聚焦于基因表达谱,缺乏可用于临床常规检测的蛋白水平辅助标志物。蛋白相互作用研究显示,HER2与CDCP1、NRF2等蛋白的相互作用可影响其信号通路及耐药性,但HNMT与HER2的相互作用及调控机制尚未被报道,这一空白限制了抗HER2治疗精准分层的进一步发展。
本研究的创新价值在于首次揭示了HNMT与HER2的相互作用及其对HER2表达的转录调控机制,将HNMT作为辅助生物标志物用于抗HER2治疗的患者筛选,不仅解决了单一HER2标志物的局限性,还为HER2低表达患者的治疗响应提供了分子解释,填补了该领域的关键研究空白。
3. 研究思路总结与详细解析
本研究的整体目标是验证HNMT作为抗HER2治疗辅助生物标志物的临床价值,并解析其调控HER2表达及治疗敏感性的分子机制;核心科学问题为HNMT如何通过与HER2的相互作用影响抗HER2治疗的敏感性;技术路线遵循“临床样本关联分析→细胞与动物模型功能验证→分子机制解析→临床转化价值验证”的闭环逻辑,从临床现象出发,逐步深入到分子机制,最终回归临床应用。
3.1 临床样本与细胞模型验证HNMT与HER2的表达关联及预后价值
实验目的:明确HNMT在不同亚型乳腺癌中的表达特征,及其与HER2表达、患者预后的关联。
方法细节:利用癌症基因组图谱(TCGA)、癌症细胞系百科全书(CCLE)数据库分析HNMT与HER2的mRNA表达相关性;收集766例乳腺癌患者配对肿瘤与正常组织样本,采用实时定量PCR(qRT-PCR)检测HNMT mRNA表达;构建包含211例乳腺癌组织的芯片,通过免疫组化(IHC)检测HNMT与HER2蛋白表达,并进行组织评分;采用Kaplan-Meier法分析HNMT表达与患者总生存率的关联。
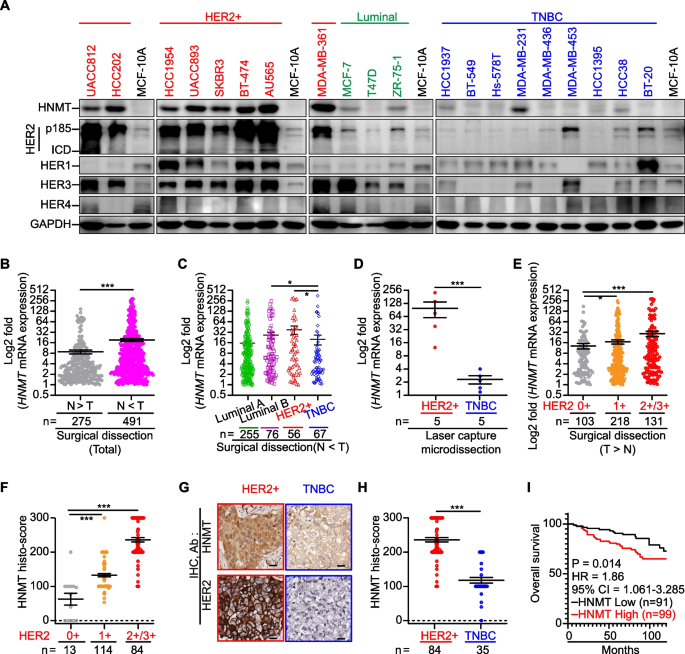
结果解读:Western blot结果显示HNMT在HER2阳性细胞系中的表达显著高于三阴性乳腺癌(TNBC)、luminal型细胞系及正常上皮细胞(Fig1A);CCLE数据库分析显示HNMT与HER2 mRNA表达呈中度正相关(n=54,R²=0.4126,P<0.01);临床样本qRT-PCR结果显示,491例患者肿瘤组织HNMT mRNA表达高于正常组织,其中HER2阳性亚型患者的HNMT表达显著高于TNBC亚型(n=5 per group,P<0.05,Fig1D);IHC组织评分显示HNMT蛋白表达与HER2阳性呈正相关(n=211,P<0.001,Fig1F-H);Kaplan-Meier分析显示高HNMT表达患者10年总生存率更低(P<0.05,Fig1I)。
产品关联:实验所用关键产品包括Invitrogen的细胞培养试剂、Abnova的HNMT抗体(货号H00003176-M12)、Santa Cruz的HER2抗体(货号sc-284)、Roche的曲妥珠单抗、Daiichi-Sankyo/AstraZeneca的T-Dxd等。
3.2 体内外模型验证HNMT对HER2表达及抗HER2治疗敏感性的影响
实验目的:验证HNMT过表达或敲除对HER2表达、肿瘤恶性表型及抗HER2治疗敏感性的调控作用。
方法细节:构建HNMT过表达(231-HN)及敲除(231-HNMT KO)的MDA-MB-231细胞系,通过细胞活力实验、划痕实验、软琼脂克隆形成实验检测细胞恶性表型;建立异种移植瘤模型,给予曲妥珠单抗(15mg/kg,每周两次)或T-Dxd(4mg/kg,每周一次)治疗,监测肿瘤生长;采用Western blot检测肿瘤组织中HER2表达,采用流式细胞术检测T-Dxd的细胞摄取。
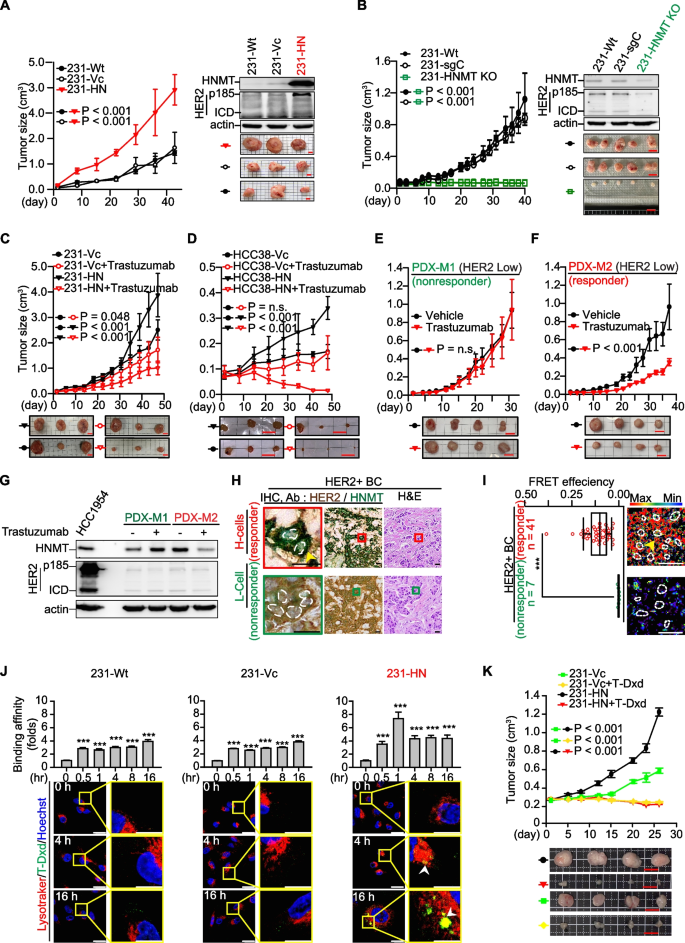
结果解读:HNMT过表达的MDA-MB-231细胞HER2蛋白表达上调,肿瘤生长速度加快(n=3,P<0.001,Fig2A),而HNMT敲除则抑制肿瘤生长(n=5,P<0.001,Fig2B);HNMT过表达的TNBC异种移植瘤对曲妥珠单抗敏感性增加,肿瘤生长受到显著抑制(n=3,P<0.001,Fig2C-D);HER2低表达的患者来源异种移植瘤(PDX)模型中,高HNMT表达的肿瘤对曲妥珠单抗响应更好(n=4,P<0.001,Fig2E-F);T-Dxd处理后,231-HN细胞的药物摄取速度更快,且在溶酶体中积累(Fig2J),异种移植瘤对T-Dxd的敏感性显著高于对照组(n=4,P<0.001,Fig2K)。
产品关联:实验所用关键产品包括Jackson Immunological Research Laboratories的荧光二抗、Promega的Luciferase报告基因试剂盒、Sony的流式细胞仪(SA3800)、Beckman Coulter的流式细胞仪(CytoFLEX)等。
3.3 分子机制解析:HNMT与HER2的相互作用及HER2-ICD的核转位与转录调控
实验目的:解析HNMT调控HER2表达及治疗敏感性的分子机制,明确蛋白相互作用、核转位及转录调控的关键环节。
方法细节:采用Förster共振能量转移(FRET)、荧光寿命成像显微镜(FLIM)检测HNMT与HER2的相互作用;采用免疫共沉淀(IP)验证蛋白复合物形成;采用免疫荧光、DeltaVision显微镜观察HNMT/HER2-ICD的核转位;采用染色质免疫沉淀测序(ChIP-seq)及ChIP-PCR分析HNMT/HER2-ICD对HER2启动子的结合;采用Luciferase报告基因实验验证转录调控作用。
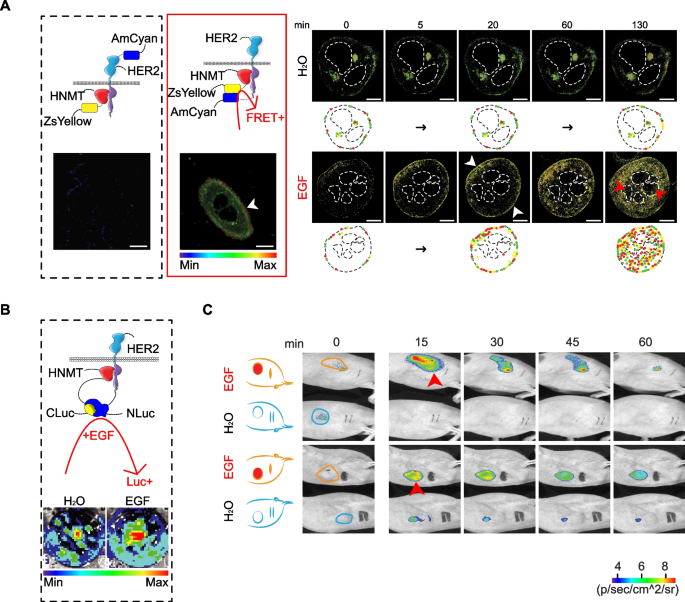
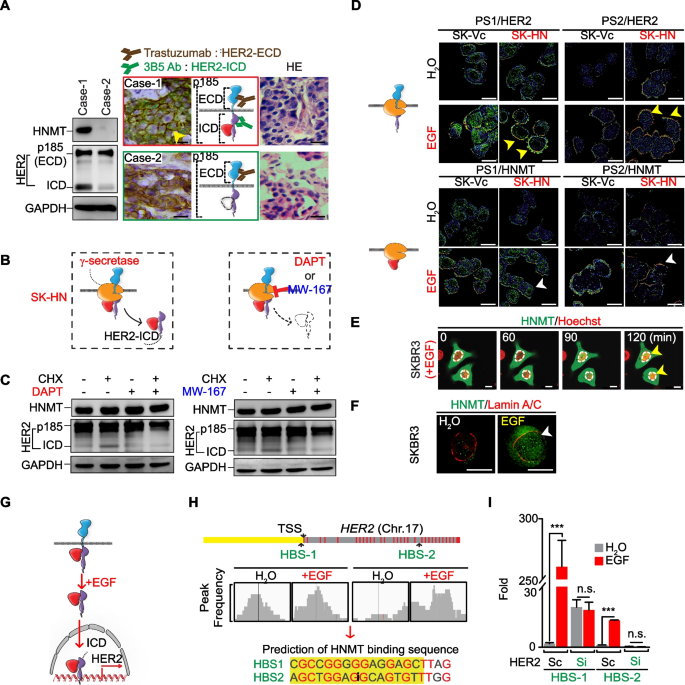
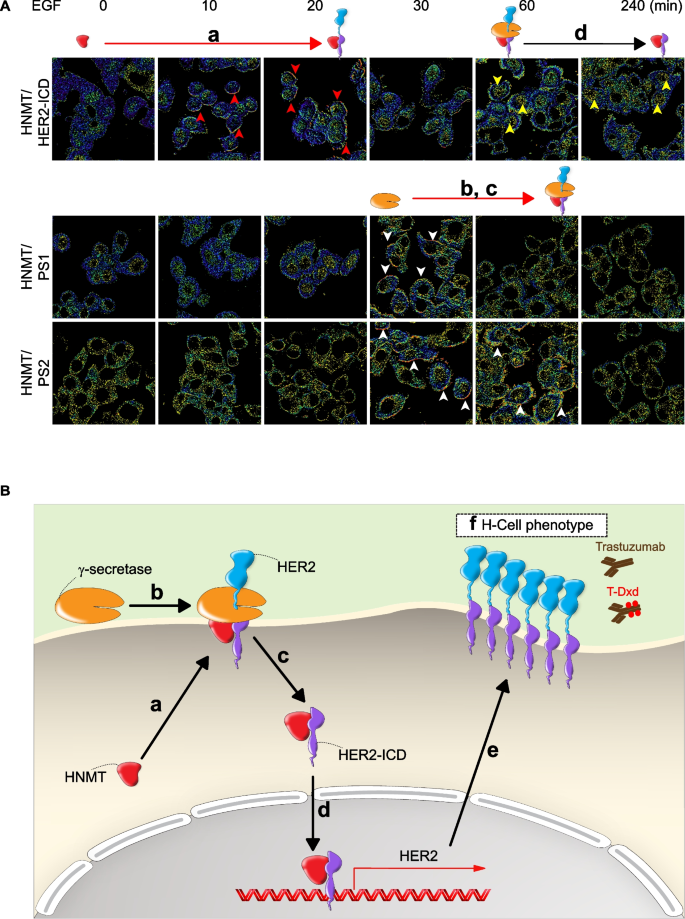
结果解读:EGF处理后,HNMT在20分钟内从细胞质转位至细胞膜,与HER2形成复合物(Fig3A),FRET分析显示两者的相互作用在曲妥珠单抗响应者肿瘤组织中显著增强(响应者n=41,非响应者n=7,P<0.001,Fig2I);HNMT与HER2的相互作用可招募γ-分泌酶切割HER2产生胞内域(HER2-ICD),随后HNMT/HER2-ICD复合物转位至细胞核(Fig4E-F);ChIP-seq及ChIP-PCR结果显示,该复合物结合到HER2启动子的HNMT结合位点1(HBS-1),激活HER2的转录(n=3,P<0.001,Fig4I);Luciferase报告基因实验验证了HBS-1位点在转录激活中的关键作用,EGF处理后HER2阳性细胞的报告基因活性显著升高(Fig4G)。
产品关联:实验所用关键产品包括Leica的TCS SP5共聚焦光谱成像系统、GE Healthcare的DeltaVision显微镜、Illumina的RNA测序试剂盒等。
4. Biomarker研究及发现成果解析
核心信息段:本研究将HNMT定位为抗HER2治疗的蛋白水平辅助生物标志物,通过完整的“临床关联-功能验证-机制解析-临床响应”链条,明确了其在HER2阳性及HER2低表达乳腺癌患者中的治疗预测价值,为临床精准分层提供了新的检测靶点。
Biomarker定位:HNMT属于可用于临床检测的蛋白辅助生物标志物,筛选逻辑为“临床样本表达关联分析→细胞与动物模型功能验证→分子机制解析→临床治疗响应验证”,从临床现象出发,逐步验证其作为治疗响应预测因子的可靠性与特异性。
研究过程详述:HNMT的来源为乳腺癌患者肿瘤组织及细胞系,验证方法包括免疫组化、qRT-PCR、FRET、体内外治疗响应实验等。特异性方面,HNMT在HER2阳性肿瘤组织中高表达,与HER2表达呈正相关(CCLE中n=54,R²=0.4126,P<0.01);敏感性方面,FRET分析显示曲妥珠单抗响应者肿瘤组织中HNMT与HER2的相互作用显著增强(响应者n=41,非响应者n=7,P<0.001),T-Dxd治疗后HNMT表达上调,进一步增强药物结合亲和力;临床样本验证显示,高HNMT表达的HER2阳性患者对曲妥珠单抗的响应率更高,而HNMT过表达的TNBC患者对T-Dxd的敏感性显著提升。
核心成果提炼:HNMT作为辅助生物标志物,可有效预测HER2阳性患者对曲妥珠单抗的响应,以及HER2低表达(TNBC)患者对T-Dxd的响应;功能关联上,HNMT通过与HER2相互作用,调控HER2-ICD的核转位及HER2的转录激活,从而增强肿瘤细胞对抗HER2药物的敏感性;创新性方面,首次发现HNMT与HER2的相互作用机制,为HER2低表达患者的治疗响应提供了分子解释,填补了该领域的研究空白。统计学结果显示,高HNMT表达的HER2阳性患者预后更差(Kaplan-Meier分析,P<0.05,n=211),但对曲妥珠单抗的响应率更高(FRET效率,P<0.001,n=48);HNMT过表达的TNBC细胞对T-Dxd的IC₅₀显著降低(n=3,P<0.001)。
