1. 领域背景与文献引入
文献英文标题:MicroRNA-based signatures impacting clinical course and biology of ovarian cancer: a miRNOmics study;发表期刊:Biomarker Research;影响因子:未公开;研究领域:卵巢癌miRNA生物标志物研究
在西方发达国家,卵巢癌是导致妇科癌症死亡的首要原因,其中上皮性卵巢癌占比超过90%。由于疾病异质性强且早期症状隐匿,约三分之二的患者确诊时已处于晚期,伴随弥漫性腹膜扩散,难以通过根治性手术切除。目前标准治疗方案为减瘤手术联合铂类化疗,但约25%的患者会在6个月内复发,即铂耐药型卵巢癌;即使初始治疗应答的患者,也有多数会在2-3年内因获得性耐药出现疾病进展。近年来PARP抑制剂等靶向药物的应用改善了部分患者的预后,但卵巢癌整体5年总生存率仍仅约45%,临床亟需更精准的早期诊断、预后评估及疗效预测生物标志物。
现有生物标志物如CA125、人附睾蛋白4(HE4)及卵巢恶性风险算法(ROMA)指数的联合应用虽提升了诊断性能,但仍存在特异性不足的问题。MicroRNA(miRNA)作为一类长度为19-23nt的非编码RNA,可通过靶向mRNA的3"UTR区域调控约30%的人类基因表达,其在癌症组织中的表达失调已被广泛报道,且具有稳定性高、可在组织及体液中检测的优势,是极具潜力的癌症生物标志物。已有研究显示miRNA在卵巢癌的化疗耐药、转移潜能、上皮间质转化(EMT)及癌症干细胞调控中发挥重要作用,但多数研究基于小样本单队列,缺乏多队列验证,且不同研究结果存在矛盾,同时对miRNA调控的通路网络研究不够系统。针对这一研究空白,本研究通过单中心队列(IRE)结合癌症基因组图谱(TCGA)大样本队列,筛选并验证具有预后及铂耐药预测价值的miRNA特征,并解析其参与的生物学通路,为卵巢癌的精准诊疗提供新的生物标志物及分子机制依据。
2. 文献综述解析
作者的综述评述逻辑按照“卵巢癌临床诊疗困境→miRNA生物学功能与癌症研究现状→卵巢癌中miRNA研究进展与局限性”的层级展开,先明确临床需求,再聚焦miRNA的研究价值,最后指出现有研究的不足。
现有研究的关键结论包括:miRNA在卵巢癌组织中存在广泛表达失调,部分miRNA可作为预后或化疗耐药的预测标志物;miRNA可通过调控EMT、DNA损伤修复、癌症干细胞等通路影响卵巢癌的发生发展及耐药性。技术方法优势方面,miRNA检测技术成熟,可通过芯片、测序等高通量方法实现大规模筛选,且miRNA在体液中稳定性高,适合作为非侵入性生物标志物。但现有研究也存在明显局限性:多数研究样本量较小,仅基于单中心队列,结果的外推性有限;不同研究中同一miRNA的预后或预测价值存在矛盾,如miR-148a-3p在部分研究中被认为是预后良好的标志物,而在另一些研究中则与不良预后相关;对miRNA调控的下游通路及分子网络研究不够深入,难以明确其具体的生物学功能。
本研究的创新价值在于,首次通过单中心队列结合TCGA大样本队列,系统筛选并验证了同时具有预后及铂耐药预测价值的miRNA特征,解决了现有研究样本量小、队列单一的问题;同时通过生物信息学分析构建了miRNA-mRNA调控网络,系统解析了miRNA特征参与的关键通路,弥补了现有研究中功能机制分析不足的缺陷,为卵巢癌的miRNA生物标志物研究提供了更可靠的依据。
3. 研究思路总结与详细解析
本研究的整体框架为:以卵巢癌临床诊疗中的预后评估及铂耐药预测需求为导向,通过IRE队列的miRNA芯片分析筛选差异表达miRNA,结合TCGA队列验证差异表达的一致性,进而筛选与生存终点及铂耐药相关的miRNA,构建预后及预测miRNA特征,最后通过功能富集分析及调控网络解析其生物学功能,形成“筛选-验证-功能解析”的完整研究闭环。核心科学问题是明确miRNA表达失调如何影响卵巢癌的临床进程及铂耐药性,技术路线遵循“临床样本高通量分析→多队列验证→临床终点关联→功能机制解析”的逻辑。
3.1 队列样本选择与临床终点定义
实验目的是建立具有明确临床信息的研究队列,定义统一的临床终点用于后续miRNA与临床结局的关联分析。
方法细节:IRE队列纳入60例接受铂类化疗的卵巢癌患者,患者年龄≥18岁,基线ECOG体力状态评分0-1,排除合并第二肿瘤的患者;同时纳入17例年龄匹配的非肿瘤卵巢组织样本作为对照,样本均来自Regina Elena国家癌症研究所生物样本库。TCGA队列纳入563例卵巢癌患者及8例非肿瘤对照样本。临床终点定义为总生存期(OS,从首次化疗开始至任何原因死亡的时间)、无事件生存期(EFS,根据治疗场景分别定义为从首次化疗至疾病进展/复发或死亡的时间)、铂敏感性状态(PSS,末次铂类化疗后6个月内复发为铂耐药,超过6个月为铂敏感)。
结果解读:IRE队列中位随访时间为47.5个月,全队列中位EFS为21.9个月,中位OS为56.5个月;其中31.7%的患者为铂耐药型,65.0%为铂敏感型。不同治疗场景(转移性、新辅助、辅助治疗)的患者EFS、OS及PSS分布存在显著差异,转移性及新辅助治疗患者的铂耐药比例显著高于辅助治疗患者(卡方检验p=0.022),提示队列异质性对临床结局的影响。
产品关联:文献未提及具体实验产品,领域常规使用组织样本保存试剂、临床数据管理系统等。
3.2 miRNA表达谱分析与差异筛选
实验目的是筛选卵巢癌组织与正常组织间差异表达的miRNA,以及与临床终点相关的miRNA。
方法细节:IRE队列采用Agilent miRNA芯片检测miRNA表达水平,数据经Agilent Feature Extraction软件提取后,进行分位数归一化、log2转换,筛选在≥50%样本中表达的miRNA;采用单变量Cox回归分析筛选与EFS、OS相关的miRNA,Wilcoxon检验筛选与铂敏感性状态相关的miRNA;选取3个代表性miRNA,通过实时荧光定量聚合酶链反应(qRT-PCR)在IRE队列的10例肿瘤及10例正常样本中验证表达差异。TCGA队列采用miRNA测序及芯片数据进行差异表达验证。
结果解读:IRE队列中,共筛选出8个与更长EFS相关的miRNA、9个与更短EFS相关的miRNA、2个与更长OS相关的miRNA;15个miRNA与铂敏感性状态相关,其中4个在铂敏感肿瘤中高表达,11个在铂耐药肿瘤中高表达;肿瘤与正常组织间共存在266个差异表达miRNA,其中6个与更短EFS相关的miRNA在肿瘤组织中显著下调(T检验p<0.001)。qRT-PCR验证结果显示,miR-99a-5p、miR-145-5p在肿瘤组织中下调,miR-224-5p在肿瘤组织中上调,与芯片结果一致(Wilcoxon检验p<0.05)。
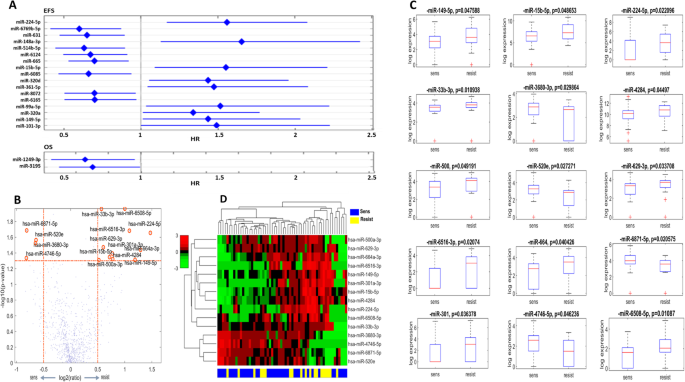
产品关联:文献未提及具体实验产品,领域常规使用miRNA芯片试剂盒、实时荧光定量聚合酶链反应(qRT-PCR)试剂盒等。
3.3 多队列验证与miRNA特征构建
实验目的是验证IRE队列筛选的差异miRNA在TCGA队列中的一致性,构建具有稳定预后及预测价值的miRNA特征。
方法细节:将IRE队列中266个肿瘤/正常差异表达miRNA与TCGA队列的miRNA表达数据进行比对,筛选出54个在两个队列中均一致差异表达的miRNA;在这54个miRNA中,筛选与IRE队列临床终点相关的miRNA,构建预后及预测miRNA特征;采用Kaplan-Meier生存分析及Cox比例风险回归模型验证特征的预后价值。
结果解读:IRE队列中,miR-99a-5p和miR-320a的下调与更短EFS相关,由这两个miRNA组成的特征对EFS的风险比(HR)为1.64(95%CI 1.10-2.44,p=0.014),对OS的HR为1.45(95%CI 0.97-2.18,p=0.07);miR-224-5p的上调与更短EFS及铂耐药相关。TCGA队列中,miR-150、miR-30d、miR-342、miR-424、miR-502的下调与更长EFS及OS相关,由这5个miRNA组成的特征对EFS和OS均有显著预后价值(log-rank检验p<0.05);miR-200a的上调与铂耐药相关。
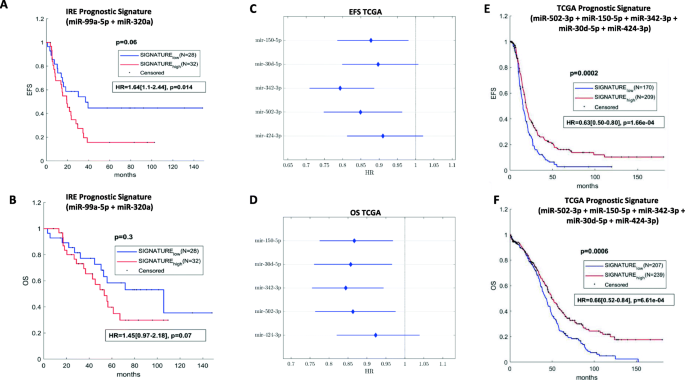
产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析软件(如MATLAB、R语言等)。
3.4 功能富集分析与调控网络构建
实验目的是解析筛选的miRNA特征参与的生物学通路及调控网络,明确其生物学功能。
方法细节:通过miRWalk、miRDB数据库预测miRNA的靶基因,结合TCGA队列的miRNA/mRNA表达数据,筛选与miRNA表达呈负相关的靶基因;采用基因集富集分析(GSEA)分析靶基因富集的生物学通路;通过miRNet构建miRNA-mRNA调控网络,通过STRING数据库构建蛋白-蛋白相互作用网络。
结果解读:7个在肿瘤组织中下调的miRNA(miR-99a-5p、miR-320a、miR-150、miR-30d、miR-342、miR-424、miR-502)的靶基因显著富集于EMT、AKT信号通路、mTOR信号通路、TGF-β信号通路等致癌通路;2个在肿瘤组织中上调的miRNA(miR-224-5p、miR-200a)的靶基因显著富集于细胞周期调控、MAPK/ERK信号通路等抑癌通路。miRNA-mRNA调控网络显示,核心靶基因包括PRKCA(血管生成)、EP300(染色质重塑)、TP53(凋亡调控)、AKT1(细胞生长)等,涉及mTOR、AKT、MAPK、P53、Wnt等卵巢癌发生发展的关键通路。
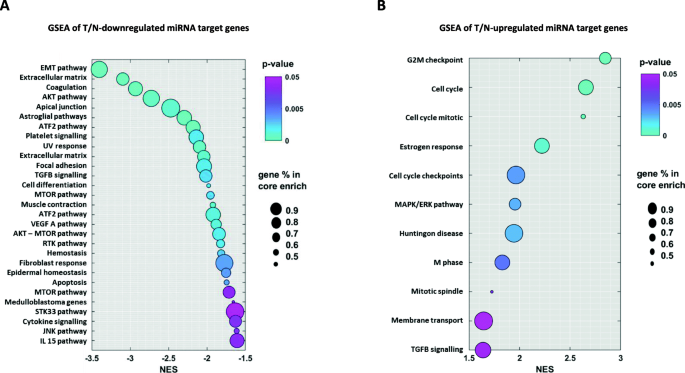
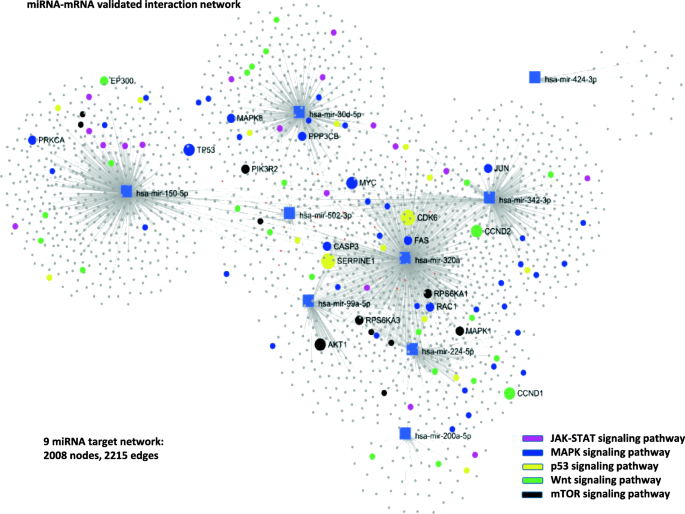
产品关联:文献未提及具体实验产品,领域常规使用生物信息学数据库(如miRWalk、miRDB、miRTarBase、STRING等)。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究涉及的Biomarker为miRNA特征,包括:IRE队列中由miR-99a-5p、miR-320a组成的2-miRNA预后特征,miR-224-5p铂耐药预测miRNA;TCGA队列中由miR-150、miR-30d、miR-342、miR-424、miR-502组成的5-miRNA预后特征,miR-200a铂耐药预测miRNA;以及整合上述9个miRNA的生物学特征。筛选与验证逻辑为:首先通过IRE队列的miRNA芯片筛选肿瘤与正常组织间的差异表达miRNA,然后在TCGA队列中验证差异表达的一致性,接着关联临床终点筛选具有预后或预测价值的miRNA,构建特征后通过生存分析验证其临床价值,最后通过功能富集分析解析其生物学意义,形成完整的“筛选-验证-功能解析”链条。
研究过程详述
Biomarker的来源为卵巢肿瘤组织样本,IRE队列样本来自Regina Elena国家癌症研究所的卵巢癌患者,TCGA队列样本来自公开数据库的卵巢癌患者。验证方法包括:采用miRNA芯片检测IRE队列的miRNA表达谱,实时荧光定量聚合酶链反应(qRT-PCR)验证部分miRNA的表达差异;利用TCGA队列的miRNA测序及芯片数据验证差异表达的一致性;通过Kaplan-Meier生存分析、Cox比例风险回归模型验证miRNA特征的预后及预测价值。特异性与敏感性方面,IRE队列中2-miRNA特征预测EFS的风险比为1.64(95%CI 1.10-2.44,p=0.014),提示其对不良预后具有较好的预测价值;TCGA队列中5-miRNA特征对EFS和OS的预测均具有显著统计学差异(log-rank检验p<0.05);miR-224-5p在IRE队列的铂耐药肿瘤中显著高表达(Wilcoxon检验p<0.05),提示其对铂耐药具有一定的预测价值。
核心成果提炼
本研究的核心成果包括:一是构建了具有稳定预后价值的miRNA特征,IRE队列的2-miRNA特征(miR-99a-5p、miR-320a下调)可作为卵巢癌不良预后的生物标志物,TCGA队列的5-miRNA特征(miR-150、miR-30d、miR-342、miR-424、miR-502下调)可作为卵巢癌良好预后的生物标志物;二是发现了具有铂耐药预测价值的miRNA,miR-224-5p上调可预测卵巢癌患者更短的EFS及铂耐药,miR-200a上调与TCGA队列的铂耐药相关;三是解析了9-miRNA生物学特征参与的关键通路,这些miRNA通过调控EMT、AKT、mTOR、细胞周期等通路影响卵巢癌的发生发展及耐药性,为卵巢癌的分子机制研究提供了新的视角。创新性方面,本研究首次通过单中心队列结合TCGA大样本队列,系统验证了miRNA特征的预后及预测价值,解决了现有研究样本量小、队列单一的问题,同时系统解析了miRNA调控的通路网络,为卵巢癌的精准诊疗提供了新的生物标志物及理论依据。统计学结果方面,IRE队列2-miRNA特征的HR=1.64(95%CI 1.10-2.44,p=0.014),TCGA队列5-miRNA特征的log-rank检验p<0.05,miR-224-5p在铂耐药与铂敏感肿瘤中的表达差异Wilcoxon检验p<0.05,所有结果均具有统计学意义。
