1. 领域背景与文献引入
文献英文标题:A preliminary analysis of interleukin-1 ligands as potential predictive biomarkers of response to cetuximab;发表期刊:Biomarker Research;影响因子:未公开;研究领域:头颈部鳞状细胞癌肿瘤免疫治疗生物标志物研究
头颈部鳞状细胞癌(HNSCC)是全球范围内常见的恶性肿瘤,复发转移型(R/M)患者的临床治疗选择有限。西妥昔单抗联合化疗的EXTREME方案是目前R/M HNSCC的一线标准治疗,虽能提升响应率和疾病控制率,但多数患者仍会出现复发或转移,且缺乏可有效预测治疗响应的生物标志物。领域共识:在非小细胞肺癌和结直肠癌中,EGFR或KRAS突变已成为EGFR抑制剂疗效的成熟预测标志物,但这些突变在HNSCC中发生率极低,无法满足临床需求;已有的潜在标志物如KRAS变体仅覆盖17%的患者,仍存在大量空白。IL-1通路具有双重功能,既被报道与肿瘤侵袭性、不良预后相关,又可激活NK细胞和T细胞的抗肿瘤免疫反应,而西妥昔单抗的疗效部分依赖NK细胞介导的抗体依赖细胞毒性(ADCC)。本研究旨在探讨IL-1α和IL-1β作为西妥昔单抗治疗HNSCC患者生存预后预测生物标志物的潜力,为临床治疗决策提供新的依据。
2. 文献综述解析
作者首先围绕西妥昔单抗的作用机制和现有生物标志物研究进行了系统评述,将现有研究分为三类:一是西妥昔单抗的直接抗肿瘤机制,包括抑制EGFR信号通路和诱导ADCC、激活树突状细胞及CD8+T细胞的免疫调节作用;二是已报道的潜在预测生物标志物,包括EGFR配体表达、EGFR多态性、MET激活等,但均未得到大规模临床验证;三是KRAS变体与更优预后的关联,但仅覆盖少数患者。作者总结了现有研究的局限性:多数标志物缺乏大规模临床验证,无法广泛应用于临床;针对西妥昔单抗疗效的预测标志物仍存在大量空白。同时,作者梳理了IL-1通路的双重功能:传统认知中IL-1信号与肿瘤侵袭性、不良预后相关,但近年研究显示IL-1可激活NK细胞和T细胞的抗肿瘤免疫反应。本研究的创新点在于首次将IL-1配体的表达与西妥昔单抗治疗的HNSCC患者预后关联,挑战了IL-1仅促肿瘤的传统认知,为西妥昔单抗疗效预测提供了新的潜在生物标志物,填补了现有研究的空白。
3. 研究思路总结与详细解析
整体研究目标是验证IL-1α和IL-1β作为西妥昔单抗治疗HNSCC患者生存预后的预测生物标志物,核心科学问题是IL-1配体表达与西妥昔单抗疗效的关联及潜在机制,技术路线为“数据库筛选→临床样本验证→细胞/动物实验机制验证”的闭环,通过多层面证据链支持研究结论。
3.1 TCGA数据库IL-1配体表达与生存分析
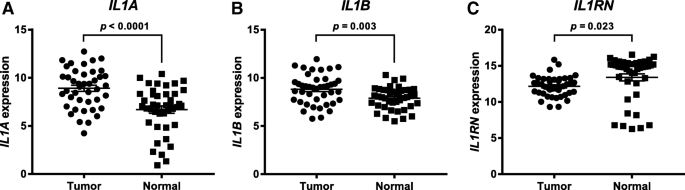
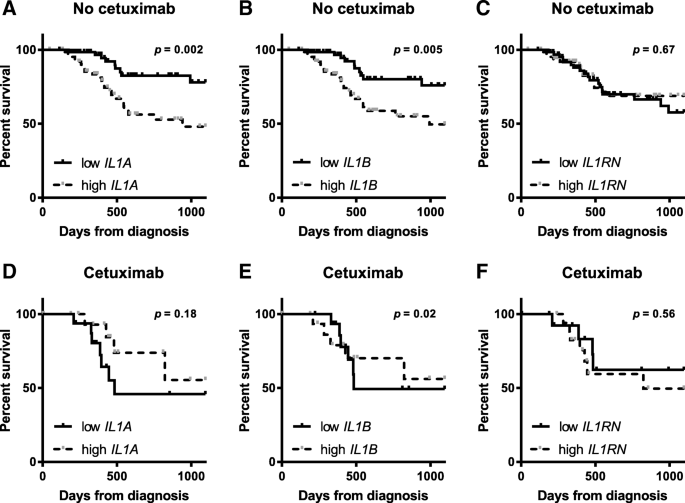
实验目的是明确HNSCC肿瘤组织中IL-1配体的表达特征及其与西妥昔单抗治疗预后的关联。方法是从TCGA数据库下载HNSCC的基因表达和临床数据,纳入164例有治疗信息的患者,分为西妥昔单抗治疗组(n=34)和非西妥昔单抗治疗组(n=130),分析肿瘤组织IL-1α、IL-1β、IL-1RA的表达差异及与总生存期的关联;同时对比42例患者的肿瘤与癌旁正常组织表达。结果显示,HNSCC肿瘤组织中IL-1α(n=42,P<0.0001)和IL-1β(n=42,P=0.003)的基因表达显著高于癌旁正常组织,IL-1RA表达显著降低(n=42,P=0.02);在非西妥昔单抗治疗组中,IL-1α和IL-1β高表达与更差的总生存期相关(P=0.002和P=0.005),而在西妥昔单抗治疗组中,IL-1β高表达与更优的总生存期相关(P=0.02),IL-1α高表达也呈现更优预后的趋势(P=0.18)。产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析工具(如UCSC Xena、GraphPad Prism)进行数据库挖掘和统计分析。
3.2 临床肿瘤样本基因表达与无进展生存关联分析
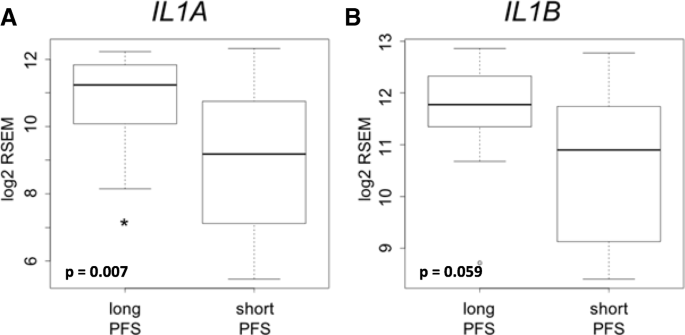
实验目的是验证IL-1配体基因表达与西妥昔单抗联合化疗患者无进展生存期(PFS)的关联。方法是回顾性分析40例接受一线西妥昔单抗联合化疗的R/M HNSCC患者的术前肿瘤活检样本基因表达数据,分为长PFS组(>12个月,n=14)和短PFS组(<5.6个月,n=26),采用LIMMA软件进行差异表达分析。结果显示,长PFS组的IL-1α基因表达显著高于短PFS组(FDR校正P=0.007),IL-1β表达也呈现更高趋势(FDR校正P=0.059)。产品关联:文献未提及具体实验产品,领域常规使用Illumina表达芯片进行基因表达检测,LIMMA软件进行差异分析。
3.3 血清IL-1配体水平与预后分析
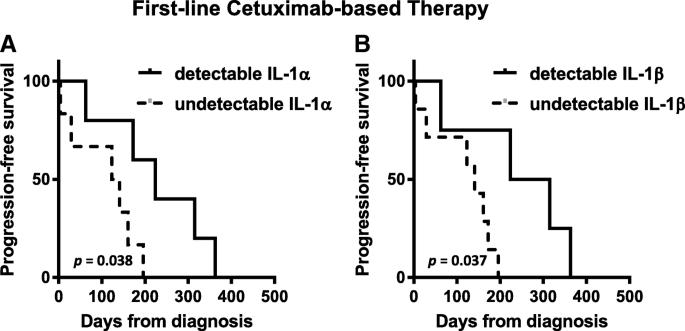
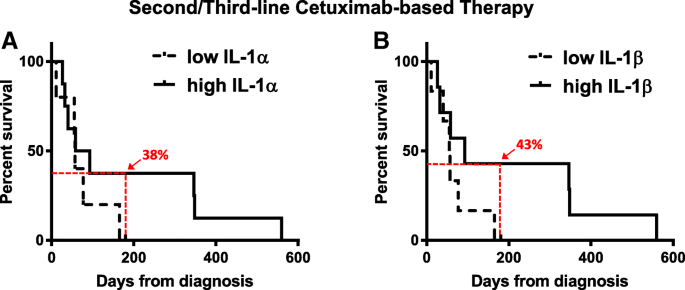
实验目的是探讨循环IL-1配体水平作为非侵入性生物标志物的潜力。方法是收集11例接受西妥昔单抗联合化疗的R/M HNSCC患者的基线血清样本,采用酶联免疫吸附实验(ELISA)检测IL-1α和IL-1β水平,分析其与PFS的关联;同时分析12例西妥昔单抗耐药患者接受西妥昔单抗联合ficlatuzumab治疗的血清样本。结果显示,血清中可检测到IL-1α(n=5)的患者PFS显著长于未检测到的患者(n=6,P=0.038),可检测到IL-1β(n=4)的患者PFS也显著更长(n=7,P=0.037);在西妥昔单抗耐药患者中,高IL-1α和IL-1β水平的患者6个月生存率更高(分别为38% vs 0%、43% vs 0%),生存曲线呈现晚期分离趋势。产品关联:实验所用关键产品:R&D Systems的IL-1α和IL-1β DuoSet ELISA试剂盒。
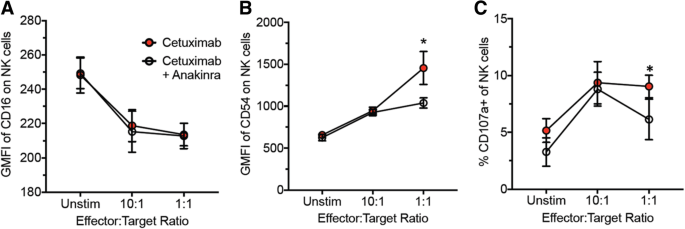
3.4 细胞实验验证IL-1对NK细胞活性的调控
实验目的是明确IL-1通路对西妥昔单抗诱导的NK细胞活性的影响。方法是将人外周血单个核细胞(PBMC)与经西妥昔单抗±IL-1受体拮抗剂(anakinra)处理的SQ20B细胞共培养6小时,采用流式细胞术检测NK细胞(CD3-)的CD16、CD54(激活标志物)和CD107a(脱颗粒标志物)表达。结果显示,anakinra抑制了西妥昔单抗诱导的NK细胞CD54表达和CD107a脱颗粒(P<0.05),但不影响CD16表达,提示IL-1信号对西妥昔单抗诱导的NK细胞激活至关重要。产品关联:实验所用关键产品:BD的抗CD3、CD16、CD54、CD107a流式抗体,FACSCanto流式细胞仪。
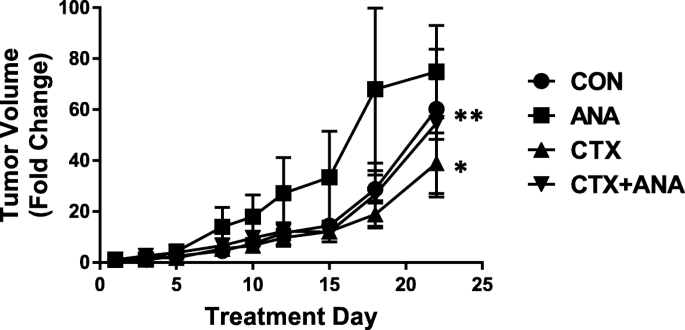
3.5 动物实验验证IL-1通路对西妥昔单抗疗效的影响
实验目的是在体内验证IL-1通路对西妥昔单抗抗肿瘤疗效的调控作用。方法是构建SQ20B细胞的裸鼠异种移植模型,分为对照组、西妥昔单抗组、西妥昔单抗+anakinra组,给药3周后每周三次监测肿瘤体积。结果显示,西妥昔单抗组肿瘤体积显著小于对照组(P<0.05),而西妥昔单抗+anakinra组的肿瘤体积显著大于西妥昔单抗组(P<0.05),提示阻断IL-1通路可部分逆转西妥昔单抗的抗肿瘤疗效。产品关联:文献未提及具体实验产品,领域常规使用免疫缺陷裸鼠构建异种移植模型,采用游标卡尺测量肿瘤体积。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选验证逻辑
本研究中涉及的Biomarker为白细胞介素-1α(IL-1α)和白细胞介素-1β(IL-1β),属于细胞因子类预测性生物标志物,其筛选验证逻辑为“TCGA数据库肿瘤组织表达筛选→临床肿瘤样本基因表达验证→血清样本循环水平验证→细胞/动物实验机制验证”的完整链条,从数据库到临床样本再到机制研究,逐步验证其作为预测标志物的潜力。
研究过程详述
Biomarker的来源包括HNSCC患者的肿瘤组织和外周血清样本,验证方法分别为基于RNA测序的基因表达分析、基于酶联免疫吸附实验(ELISA)的血清蛋白定量检测。在肿瘤组织中,IL-1α和IL-1β的基因表达显著高于癌旁正常组织;在西妥昔单抗治疗患者中,高表达的IL-1β与更优总生存期相关(n=34,P=0.02),高表达的IL-1α与更长PFS相关(n=40,FDR校正P=0.007)。在血清样本中,可检测到IL-1α的患者PFS显著长于未检测到的患者(n=5 vs n=6,P=0.038),可检测到IL-1β的患者PFS也显著更长(n=4 vs n=7,P=0.037);在西妥昔单抗耐药患者中,高IL-1配体水平的患者6个月生存率更高,生存曲线呈现晚期分离趋势。
核心成果提炼
本研究的核心成果包括:1. IL-1β高肿瘤基因表达与西妥昔单抗治疗HNSCC患者的更优总生存期相关(n=34,P=0.02),而在非西妥昔单抗治疗患者中则与不良预后相关,体现了标志物的治疗特异性;2. IL-1α高肿瘤基因表达与更长的PFS相关(n=40,FDR校正P=0.007),提示其可预测长期治疗响应;3. 血清中可检测到IL-1配体的患者PFS显著延长,为非侵入性检测提供了可能;4. 机制上IL-1通路通过调控NK细胞活性影响西妥昔单抗的疗效,为标志物的临床应用提供了理论基础。本研究的创新性在于首次发现IL-1配体在西妥昔单抗治疗中的正向预测作用,打破了IL-1仅与肿瘤不良预后相关的传统认知,为HNSCC患者的西妥昔单抗治疗疗效预测提供了新的潜在生物标志物,同时为血清非侵入性检测提供了可能,值得在更大规模的临床研究中进一步验证。
