1. 领域背景与文献引入
文献英文标题:Mechanically produced schistosomula as a higher-throughput tools for phenotypic pre-screening in drug sensitivity assays: current research and future trends;发表期刊:Biomarker Research;影响因子:未公开;研究领域:热带病学(血吸虫病抗寄生虫药物研发)
全球范围内,血吸虫病是最具破坏性的热带病之一,目前有超过2.07亿人感染,其中85%的感染者集中在撒哈拉以南非洲地区,给发展中国家带来严重的疾病负担与死亡风险。血吸虫病的病理机制主要是宿主对寄生虫虫卵的免疫反应,虫卵在肝脏、肠道、膀胱等组织器官中沉积,引发肝脾肿大、纤维化等慢性病变,甚至导致认知功能损伤。当前血吸虫病的治疗完全依赖单一药物吡喹酮(PZQ),该药物于1970年代被发现,1988年上市,对成虫阶段的血吸虫具有高效杀灭作用,但对幼虫阶段无效,导致感染者需重复治疗;同时,长期单一用药的现状引发了对药物耐药性的广泛担忧,而血吸虫病新药研发管线几乎枯竭,候选药物如甲氟喹、青蒿素类均未达到目标产品要求。
传统的血吸虫病药物筛选依赖成虫模型,需通过哺乳动物宿主(仓鼠、大鼠、小鼠)感染获取成虫,实验周期长达30天以上,通量极低且仅少数具备寄生虫复杂生命周期操作能力的实验室可开展,严重限制了新药研发效率。因此,开发高通量、低成本的体外药物筛选模型成为领域核心需求。本文系统综述了机械转化的新转化血吸虫幼虫(NTS)作为高通量筛选工具的技术体系,涵盖NTS的制备、培养、活力检测全流程,为血吸虫病新药研发提供了全面的技术参考框架。
2. 文献综述解析
作者以“筛选模型类型-幼虫转化方法-活力检测技术”为三维分类维度,对现有血吸虫病药物筛选研究进行系统评述,明确了不同技术路径的优势、局限性及未解决的核心问题。
现有研究中,成虫筛选模型的核心结论是能直接反映成体寄生虫的药物敏感性,优势是贴近临床治疗靶点,技术体系成熟;但该模型必须依赖哺乳动物宿主获取成虫,实验周期长、通量极低,且操作门槛高,仅少数实验室可开展。幼虫筛选模型方面,非机械转化方法(如皮肤穿透法、化学转化法)获得的NTS更贴近体内自然转化过程,但存在宿主材料污染、产量低、转化效率仅34%的问题,难以满足高通量筛选需求;传统的显微镜活力检测是领域金标准,能直接观察寄生虫形态与运动变化,但主观性强、耗时,单实验室每月仅能筛选约640个化合物,结果重复性差。
本文的创新价值在于填补了现有综述对机械转化NTS高通量筛选技术体系总结不足的空白,通过系统对比不同转化方法、培养条件、活力检测技术的性能参数,明确了机械转化NTS作为高通量筛选工具的可行性与优化方向,为领域建立标准化的高通量药物筛选平台提供了关键技术依据。
3. 研究思路总结与详细解析
本文的研究目标是系统构建机械转化NTS用于血吸虫病药物高通量筛选的完整技术体系,核心科学问题是如何优化NTS的制备效率、培养稳定性及活力检测的客观性与通量,技术路线遵循“领域需求→技术体系梳理→方法对比优化→挑战与未来展望”的逻辑闭环。
3.1 血吸虫生活周期与NTS生物学定位
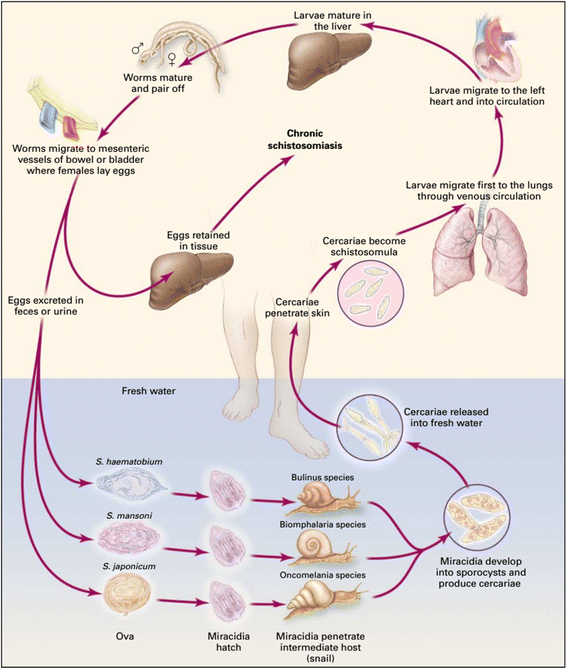
实验目的是明确NTS在血吸虫生活周期中的阶段特征与药物筛选的适用性。方法上通过文献综述梳理血吸虫的完整生活周期,包括虫卵孵化、毛蚴感染钉螺、尾蚴释放、穿透宿主皮肤转化为NTS、发育为成虫产卵的全流程,重点分析NTS阶段的形态与生理变化(如尾蚴丢失、体表膜从三层变为七层、糖萼丢失等)。结果显示,NTS是尾蚴穿透宿主皮肤后立即形成的幼虫阶段,在体内需5-7天进入血液循环,15天以上发育为成虫,该阶段对药物的敏感性与成虫存在差异,且可通过体外大量制备,适合作为高通量药物筛选的模型。
文献未提及具体实验产品,领域常规使用寄生虫培养相关的实验耗材与试剂。
3.2 NTS转化方法优化与对比
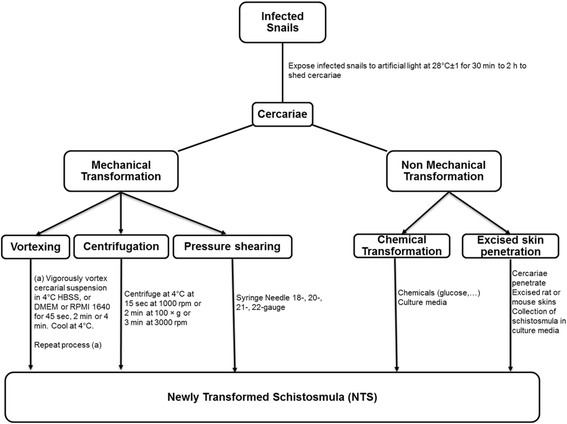
实验目的是对比不同NTS转化方法的效率、纯度与适用性,筛选适合高通量制备的技术。方法上系统综述非机械转化(皮肤穿透法、化学转化法)与机械转化(涡旋法、针头剪切法)的操作流程,包括尾蚴收集、转化处理、纯化步骤(Percoll梯度离心、涡旋纯化、冰浴纯化),并分析不同方法的转化效率与纯化因子。结果显示,机械转化法是目前最适合高通量制备的技术,其中涡旋法的平均转化效率为69%,针头剪切法可实现大量尾蚴的快速转化;纯化方法中Percoll梯度离心的纯化因子最高(24.4±11.4),涡旋法为11.7±3.2,冰浴法仅3±1.7。非机械转化法的转化效率与纯度均低于机械转化法,难以满足高通量需求。
文献未提及具体实验产品,领域常规使用离心机、涡旋振荡器、针头、Percoll等商品化试剂与仪器。
3.3 NTS培养条件优化
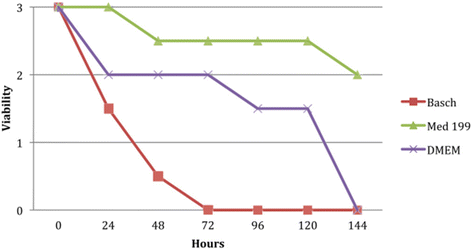
实验目的是筛选适合NTS体外长期培养的培养基,保障药物筛选过程中幼虫的稳定性。方法上对比不同培养基(Medium 199、DMEM、Basch Medium 169等)添加不同浓度灭活胎牛血清(5%-10%)、抗生素(青霉素-链霉素100-300U/ml)、抗真菌试剂(两性霉素B)后的NTS存活时间与形态变化。结果显示,添加5%-10%灭活胎牛血清的Medium 199是最适合NTS培养的培养基,埃及血吸虫NTS在该培养基中可存活120小时,平均活力值为2.5;而Basch Medium 169中NTS仅能存活72小时,DMEM中存活144小时。抗生素与抗真菌试剂可有效降低培养过程中的污染风险。
文献未提及具体实验产品,领域常规使用商品化细胞培养基、血清、抗生素及抗真菌试剂。
3.4 药物筛选中NTS活力检测技术
实验目的是对比不同活力检测方法的客观性、通量与准确性,为高通量筛选提供技术支持。方法上综述传统显微镜观察(形态与运动能力评分,0-3分)、荧光染料法(PI/FDA双染色、刃天青还原法)、代谢标志物法(乳酸检测)、自动化技术(xCELLigence运动监测、高内涵筛选)的原理与应用。结果显示,传统显微镜观察是领域金标准,能直接反映寄生虫表型,但主观性强、通量低;荧光染料法(如PI/FDA双染色)可实现客观定量,通量提升10倍,无需专业形态学培训;乳酸检测可通过代谢水平反映NTS活力,但操作繁琐,通量有限;xCELLigence系统可实时监测运动能力,结果客观,但设备成本高。
文献未提及具体实验产品,领域常规使用荧光显微镜、微孔板读数仪、xCELLigence系统等商品化仪器,以及PI、FDA、刃天青等荧光试剂。
3.5 高通量筛选技术的挑战与未来展望
实验目的是分析当前机械转化NTS用于高通量筛选的瓶颈,提出未来优化方向。方法上总结现有技术的局限性,包括NTS培养稳定性不足、活力检测技术的通量与准确性平衡、自动化技术的成本问题等。结果显示,未来需优化NTS的培养条件以延长存活时间,开发低成本、高准确性的自动化活力检测技术,建立标准化的NTS制备与筛选流程,实现不同实验室结果的可重复性。
文献未提及具体实验产品,领域未来可聚焦自动化检测设备与标准化试剂的开发。
4. Biomarker研究及发现成果
本文围绕NTS活力检测的Biomarker进行系统综述,涵盖形态学、荧光、代谢、运动学四大类Biomarker,明确了不同Biomarker的筛选逻辑、验证方法与应用局限性。
Biomarker定位与筛选逻辑
作者按“传统金标准→客观定量标志物→自动化技术标志物”的逻辑梳理了NTS活力的Biomarker,筛选过程从主观形态观察到客观分子/代谢检测,再到实时运动监测,逐步实现高通量、客观化的活力评估。
研究过程详述
形态学Biomarker(运动能力、形态变化)通过显微镜观察,采用0-3分的活力评分标准(3=运动正常、形态无变化;2=运动减弱、体表轻微损伤;1=运动严重减弱、体表严重损伤;0=死亡);荧光Biomarker包括PI(死虫细胞核染色)、FDA(活虫细胞质染色)、刃天青(被活虫还原为红色荧光产物),通过微孔板读数仪定量检测荧光强度;代谢Biomarker乳酸通过荧光法检测,作为糖酵解的产物,其分泌水平与NTS活力正相关;运动学Biomarker通过xCELLigence系统监测寄生虫与电极接触的电流变化,反映运动能力的实时变化。文献未提供各Biomarker的特异性、敏感性数值(如AUC、敏感性百分比)及统计学结果(P值、样本量)。
核心成果提炼
形态学Biomarker是领域金标准,能直接反映寄生虫表型,但缺乏客观量化数据;荧光Biomarker可实现高通量、客观定量,适合大规模药物筛选;代谢Biomarker能反映寄生虫的生理状态,但操作步骤多,通量有限;运动学Biomarker可实时监测,但设备成本高。未来需开发整合多种Biomarker的检测技术,实现活力评估的准确性与通量的平衡,为高通量药物筛选提供更可靠的技术支持。
