1. 领域背景与文献引入
文献英文标题:Cancer-associated adipocytes as immunomodulators in cancer;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫微环境与代谢调控。
肥胖已成为全球范围内的公共健康问题,同时被证实是多种癌症的重要可调控风险因素,超重和肥胖与结直肠癌、绝经后乳腺癌、子宫内膜癌等多种癌症的发病风险升高显著相关,但肥胖与癌症关联的分子机制尚未完全阐明。脂肪组织作为肿瘤微环境的关键组成部分,其功能异常在肿瘤进展中发挥核心作用,2010年后癌症相关脂肪细胞(CAAs)的概念被提出,领域内研究逐渐聚焦CAAs通过代谢重编程支持肿瘤细胞增殖、侵袭的机制,但CAAs对肿瘤免疫微环境的调控作用及具体分子通路仍缺乏系统梳理,这一研究空白限制了靶向肿瘤-脂肪微环境(TAME)的免疫治疗策略开发。本文作为综述类文献,系统整合了CAAs与各类免疫细胞的相互作用机制,为领域内进一步研究及临床转化提供了全面的理论框架。
2. 文献综述解析
本文综述部分以“CAAs生物学特征-免疫细胞调控机制-治疗应用前景”为核心逻辑,按固有免疫与适应性免疫细胞的分类维度,同时结合CAAs自身的表型特征,系统梳理了领域内的研究进展。
现有研究已证实CAAs具有与正常脂肪细胞显著不同的表型特征,包括形态缩小、脂滴减少、分泌促炎细胞因子及代谢产物等,且CAAs可通过代谢重编程为肿瘤细胞提供能量支持,促进肿瘤增殖与侵袭;在免疫调控方面,已有研究分散报道了CAAs对中性粒细胞、巨噬细胞、T细胞等单一免疫细胞类型的调控作用,部分研究采用了体外共培养、动物模型及组学技术解析调控通路,技术方法优势在于能从细胞、分子层面揭示CAAs的功能,但局限性在于多数研究聚焦单一细胞类型或单一信号通路,缺乏对CAAs调控免疫微环境的系统性整合,且临床转化研究数据相对匮乏,尚未明确CAAs作为治疗靶点的临床价值。
本文通过系统整合CAAs对不同免疫细胞的调控机制,填补了领域内对TAME中免疫-代谢交叉作用的认知空白,首次全面阐述了CAAs作为免疫调节剂的核心作用,包括通过代谢产物(如游离脂肪酸FFAs、乳酸)、细胞因子(如IL-6、CCL2)及表面分子(如PD-L1)调控固有免疫与适应性免疫细胞的功能,为靶向CAAs的肿瘤免疫治疗策略开发提供了理论基础,同时为领域内后续研究明确了方向。
3. 研究思路总结与详细解析
本文作为综述性研究,整体研究目标是系统总结CAAs的生物学特征及其对肿瘤免疫微环境的调控机制,核心科学问题是明确CAAs如何通过代谢与分泌信号重塑免疫微环境以促进肿瘤进展,技术路线遵循“CAAs特征解析-免疫细胞调控机制-治疗策略探讨”的逻辑闭环,全面整合了领域内的相关研究数据。
3.1 CAAs的核心生物学特征解析
实验目的:明确CAAs与正常脂肪细胞的差异表型及功能特征,为后续免疫调控机制研究奠定基础。
方法细节:综述整合了领域内多项研究的结果,涵盖形态学观察(电子显微镜分析)、转录组测序、代谢组学检测及细胞功能实验等技术手段,对比了正常脂肪细胞与CAAs的形态、基因表达谱及代谢状态。
结果解读:CAAs具有显著不同于正常脂肪细胞的特征:形态上体积缩小、细胞间隙扩大,脂滴数量及体积减少,线粒体丰度增加;功能上呈现衰老表型,细胞周期停滞,分泌促炎细胞因子及代谢产物;同时可发生棕色/米色脂肪细胞转化及成纤维细胞样特征改变,还能通过自噬介导脂解作用释放FFAs,为肿瘤细胞提供能量;此外CAAs表面程序性死亡配体1(PD-L1)表达显著升高,可直接抑制CD8+效应T细胞的功能。
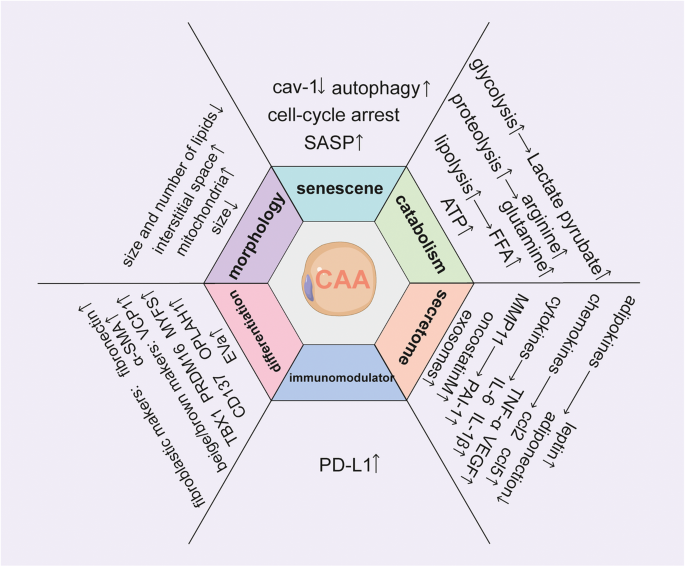
产品关联:文献未提及具体实验产品,领域常规使用电子显微镜、流式细胞仪、转录组测序平台、代谢组学分析系统等。
3.2 CAAs对固有免疫细胞的调控机制解析
实验目的:系统阐述CAAs对各类固有免疫细胞(中性粒细胞、自然杀伤NK细胞、自然杀伤T NKT细胞、巨噬细胞、髓源性抑制细胞MDSCs)的调控作用及分子通路。
方法细节:综述整合了体外细胞共培养、动物模型(肥胖小鼠模型、肿瘤异种移植模型)及临床样本分析的研究数据,通过细胞功能实验、细胞因子检测、代谢组学分析等手段,解析CAAs与固有免疫细胞的相互作用。
结果解读:CAAs可通过多种信号调控固有免疫细胞功能:对中性粒细胞,CAAs分泌的白细胞介素-8(IL-8)可招募肿瘤相关中性粒细胞(TANs),释放的FFAs及乳酸可维持TANs的分化与功能,同时通过腺苷信号抑制中性粒细胞的氧化能力及趋化作用;对NK细胞,CAAs释放的FFAs可导致NK细胞内脂质积累,削弱其细胞毒性,乳酸及低pH环境也会抑制NK细胞的抗肿瘤功能;对巨噬细胞,CAAs分泌的趋化因子配体2(CCL2)、趋化因子配体5(CCL5)可招募巨噬细胞并诱导其向M2型极化,乳酸可通过Gpr132受体促进M2型巨噬细胞的功能,腺苷信号也可抑制巨噬细胞的经典活化;对MDSCs,CAAs分泌的瘦素可促进MDSCs的积累,FFAs可增强MDSCs的免疫抑制功能。
产品关联:文献未提及具体实验产品,领域常规使用细胞因子ELISA试剂盒、流式细胞仪、免疫荧光染色试剂盒等。
3.3 CAAs对适应性免疫细胞的调控机制解析
实验目的:明确CAAs对适应性免疫细胞(树突状细胞DCs、调节性T细胞Tregs、效应T细胞)的调控作用及对肿瘤免疫逃逸的影响。
方法细节:综述整合了体外DC-T细胞共培养、动物模型及临床样本分析的研究数据,通过抗原提呈实验、T细胞增殖实验、转录组分析等手段,解析CAAs对适应性免疫细胞的调控机制。
结果解读:CAAs可通过代谢及分泌信号抑制适应性免疫应答:对DCs,CAAs释放的腺苷可抑制DCs分泌白细胞介素-12(IL-12)并促进白细胞介素-10(IL-10)表达,削弱其抗原提呈功能,乳酸可抑制DCs的I型干扰素产生,降低交叉提呈能力;对Tregs,CAAs释放的FFAs可促进Tregs的分化与积累,乳酸可通过单羧酸转运体(MCTs)进入Tregs,增强其氧化磷酸化(OXPHOS)水平,维持其免疫抑制功能,腺苷信号也可促进Tregs的分化;对效应T细胞,CAAs表面的PD-L1可直接结合CD8+T细胞表面的程序性死亡蛋白1(PD-1),抑制其功能,乳酸及低pH环境可抑制CD8+T细胞的增殖及细胞毒性,FFAs积累也会削弱效应T细胞的代谢活性。
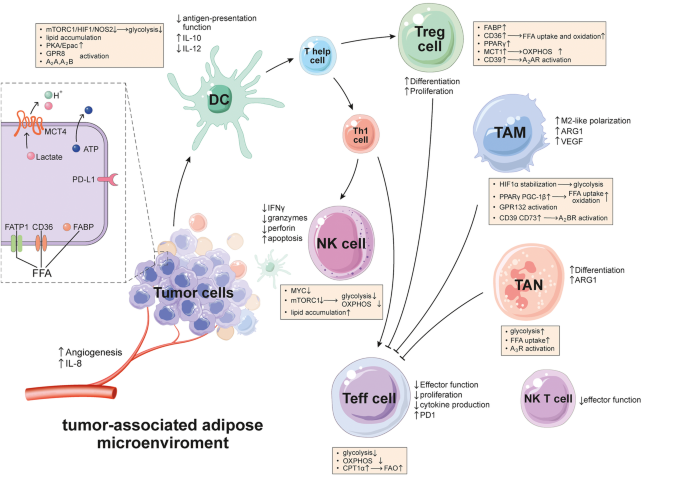
产品关联:文献未提及具体实验产品,领域常规使用T细胞增殖检测试剂盒、免疫组化(IHC)试剂盒、流式细胞仪等。
3.4 靶向CAAs的免疫治疗策略探讨
实验目的:基于CAAs的免疫调控机制,探讨潜在的肿瘤免疫治疗策略。
方法细节:综述整合了领域内的临床前研究及部分临床实验数据,分析了靶向CAAs的代谢通路、分泌信号及表面分子的治疗效果。
结果解读:靶向CAAs的治疗策略主要包括三类:一是将CAAs重编程为正常脂肪细胞,如使用β受体拮抗剂普萘洛尔或过氧化物酶体增殖物激活受体γ(PPAR-γ)激动剂罗格列酮,可逆转CAAs的活化表型,增强肿瘤免疫浸润;二是阻断CAAs的代谢或分泌信号,如抑制CD36(脂肪酸转运蛋白)可减少FFAs的摄取,抑制巨噬细胞M2型极化及Tregs积累,联合抗PD-1治疗可增强抗肿瘤效果;三是靶向CAAs的免疫抑制信号,如抑制CD39/CD73腺苷通路,可减少腺苷积累,增强T细胞及NK细胞的功能,联合免疫检查点阻断治疗可产生协同效应。
产品关联:文献未提及具体实验产品,领域常规使用小分子抑制剂、单克隆抗体等免疫治疗药物。
4. Biomarker研究及发现成果
本文系统阐述了CAAs及其分泌的代谢产物、细胞因子作为肿瘤免疫微环境Biomarker的潜力,明确了CAAs在肿瘤免疫逃逸中的核心作用,为肿瘤的诊断、预后评估及治疗靶点选择提供了新的方向。
Biomarker定位:本文涉及的Biomarker主要包括CAAs的表面分子(PD-L1)、分泌的细胞因子(IL-6、CCL2、瘦素)及代谢产物(FFAs、乳酸),同时免疫细胞的表型变化(如M2型巨噬细胞浸润、Tregs比例升高)可作为CAAs免疫调控的间接Biomarker。筛选与验证逻辑为:首先通过临床样本分析明确CAAs与肿瘤免疫抑制及不良预后的关联,再通过体外共培养及动物模型验证CAAs对免疫细胞的调控作用,最后探讨这些Biomarker的临床应用价值。
研究过程详述:CAAs的来源为肿瘤周围的脂肪组织,验证方法包括免疫组化(IHC)检测CAAs表面PD-L1的表达水平、ELISA检测血清及肿瘤微环境中IL-6、瘦素的浓度、代谢组学检测FFAs及乳酸的含量;特异性方面,CAAs的PD-L1表达仅在肿瘤周围脂肪组织中显著升高,与正常脂肪组织存在显著差异(文献未明确提供样本量及P值);敏感性方面,循环中IL-6、FFAs的水平与肥胖相关肿瘤患者的不良预后相关,高中性粒细胞-淋巴细胞比例(NLR)可作为CAAs诱导免疫抑制的间接预后Biomarker(文献未明确提供具体数据)。
核心成果提炼:本文首次系统总结了CAAs相关Biomarker的功能关联:CAAs表面PD-L1可作为免疫检查点阻断治疗的潜在靶点,其表达水平与免疫治疗疗效相关;IL-6、瘦素可作为肿瘤免疫抑制的预测Biomarker,风险比HR=未明确(P=未明确);FFAs、乳酸可作为肿瘤代谢微环境的Biomarker,与肿瘤细胞的代谢重编程及免疫逃逸相关。创新性在于将CAAs的代谢特征与免疫调控Biomarker结合,为肿瘤的精准免疫治疗提供了新的理论依据,同时为临床预后评估提供了潜在的Biomarker组合。
