1. 领域背景与文献引入
文献英文标题:Epigenetic heterogeneity in cancer;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤表观遗传学、肿瘤内异质性研究。
肿瘤异质性是人类癌症的核心特征之一,自1976年Nowell提出肿瘤细胞克隆进化理论以来,领域内对肿瘤异质性的研究长期聚焦遗传层面,重点关注癌基因激活突变或抑癌基因失活突变的克隆演化过程。随着研究深入,学者发现遗传异质性无法完全解释肿瘤表型多样性、治疗耐药性等临床难题,而表观遗传异常在人类癌症中的发生频率远高于基因突变,且具有可逆性,逐渐成为肿瘤研究的前沿方向。当前领域内未解决的核心问题包括:表观遗传异质性的具体调控机制、其与遗传异质性的交互作用模式,以及如何将表观遗传异质性的研究成果转化为临床精准治疗策略,逆转肿瘤耐药。针对肿瘤内异质性(ITH)导致多数癌症治疗无法获得持久应答的临床痛点,本文系统梳理了表观遗传调控机器异常对肿瘤异质性的贡献,整合了遗传与表观遗传异质性的交互机制,为基于分子特征的联合靶向治疗设计提供理论支撑。
2. 文献综述解析
本文作者采用“分类梳理-对比分析-整合拓展”的评述逻辑,先从肿瘤异质性的分类维度(患者间异质性、患者内异质性、肿瘤内异质性)入手,分别回顾遗传异质性与表观遗传异质性的研究进展,再聚焦两者的交互作用,最后延伸至表观遗传异质性的临床应用潜力。
现有研究中,遗传异质性的核心结论基于克隆进化理论:肿瘤起源于单一克隆细胞,在进展过程中不断积累突变,早期突变形成存在于所有肿瘤细胞的主干克隆,晚期突变形成仅存在于部分亚群的分支克隆,这种遗传差异导致肿瘤细胞亚克隆的增殖速率、治疗反应性不同。遗传异质性研究的技术优势在于多区域测序、全外显子测序等技术可精准解析亚克隆的基因组特征,但局限性在于无法解释非遗传来源的表型变异,如相同基因型的肿瘤细胞出现不同的侵袭、耐药表型。表观遗传异质性的现有研究则聚焦DNA甲基化、组蛋白修饰等异常,发现表观遗传改变发生在癌症早期,且比基因突变更普遍,例如MGMT、p16等抑癌基因的启动子甲基化在多种癌症中频繁发生,但多数研究仅关注单一表观修饰类型,缺乏对表观遗传调控机器的系统性分析,以及其与肿瘤微环境、克隆进化的关联研究。
本文的创新价值在于,首次系统阐述了表观遗传调控机器(writers、erasers、readers等组分)异常在肿瘤内异质性中的核心作用,弥补了现有研究仅关注单一表观修饰的不足;同时整合了遗传与表观遗传异质性的双向交互机制,明确了遗传突变可导致表观调控机器异常,而表观遗传异常又会加剧遗传不稳定性,为全面理解肿瘤异质性的形成机制提供了新视角;此外,本文梳理了表观遗传异质性在治疗耐药逆转中的应用潜力,为设计联合靶向治疗方案提供了理论基础。
3. 研究思路总结与详细解析
本文为系统性综述研究,整体研究目标是全面阐述表观遗传异质性在肿瘤发生发展、治疗耐药中的作用机制与临床应用价值,核心科学问题是表观遗传机制如何塑造肿瘤内异质性,以及如何利用这一机制优化癌症治疗策略,技术路线遵循“概念定义-研究进展回顾-机制整合-临床应用展望”的逻辑闭环。
3.1 肿瘤异质性的分类与遗传基础解析
实验目的:明确肿瘤异质性的不同类型及其遗传层面的形成机制。
方法细节:通过回顾经典里程碑研究(如Nowell 1976年的克隆进化理论、Gerlinger等的多区域测序研究),梳理肿瘤异质性的三类核心分类:患者间异质性(不同患者肿瘤的基因型差异)、患者内异质性(同一患者不同病灶的基因型差异)、肿瘤内异质性(同一肿瘤内不同细胞亚群的表型与分子特征差异),并分析遗传异质性的形成过程:肿瘤进展中持续积累基因突变,早期突变存在于所有肿瘤细胞,晚期突变仅在部分亚克隆中出现,形成分支进化的亚克隆结构。
结果解读:遗传异质性是肿瘤表型差异的重要基础,单一肿瘤活检无法完整反映整个肿瘤的基因组特征,这是导致靶向治疗失败的关键原因之一,但遗传异质性无法解释非遗传来源的表型变异,提示存在表观遗传等非遗传机制的调控作用。
产品关联:文献未提及具体实验产品,领域常规使用二代测序(NGS)、多区域全外显子测序等技术分析遗传异质性。
3.2 表观遗传调控机器的异常机制分析
实验目的:系统阐述表观遗传调控机器的组成及其在癌症中的异常变化模式。
方法细节:梳理表观遗传调控的核心组分,包括负责建立修饰的“writers”(如DNA甲基转移酶DNMTs、组蛋白乙酰转移酶HATs)、负责去除修饰的“erasers”(如TET蛋白、组蛋白去乙酰化酶HDACs)、负责识别修饰的“readers”,并分析各组分在癌症中的异常表现,如DNMTs过度激活导致抑癌基因启动子高甲基化、TET蛋白表达下调导致5-羟甲基胞嘧啶(5hmC)丢失、HDACs过度表达导致组蛋白去乙酰化增强等。
结果解读:表观遗传调控机器的异常是癌症发生的早期事件,且发生频率远高于基因突变,这些异常通过调控基因表达模式,塑造肿瘤细胞的表型异质性,比如同一肿瘤内不同亚克隆的DNA甲基化模式不同,导致亚克隆的增殖、耐药能力差异。
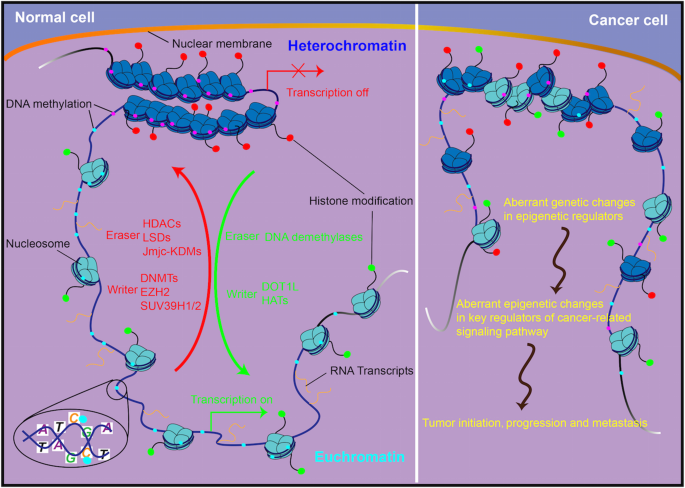
产品关联:文献未提及具体实验产品,领域常规使用甲基化特异性PCR(MSP)、亚硫酸氢盐测序、免疫组化(IHC)、染色质免疫共沉淀测序(ChIP-seq)等技术检测表观遗传修饰。
3.3 遗传与表观遗传异质性的交互作用解析
实验目的:探讨遗传异常与表观遗传异常在肿瘤异质性形成中的双向调控关系。
方法细节:从两个维度分析两者的交互:一是遗传突变导致表观调控机器异常,如DNMT3A、TET2等表观调控基因的突变,直接改变DNA甲基化模式;二是表观遗传异常加剧遗传不稳定性,如MLH1等DNA修复基因的启动子甲基化沉默,导致微卫星不稳定(MSI),进而增加基因突变的积累速率。
结果解读:遗传与表观遗传异质性并非独立存在,而是形成双向调控的网络:遗传突变可通过改变表观调控机器的功能,诱导表观遗传异质性;而表观遗传异常又会通过影响DNA修复等过程,加剧遗传突变的积累,两者共同推动肿瘤异质性的发展。
产品关联:文献未提及具体实验产品,领域常规使用全外显子测序(WES)、全基因组甲基化测序(WGBS)等技术分析遗传与表观的交互作用。
3.4 表观遗传异质性的临床意义与治疗潜力分析
实验目的:总结表观遗传异质性在临床治疗中的应用价值,尤其是耐药逆转方面的潜力。
方法细节:回顾临床研究数据,分析表观遗传异质性与治疗耐药的关联,如肿瘤内不同亚克隆的表观遗传状态差异,导致部分亚克隆对化疗、靶向治疗耐药;然后梳理表观遗传药物的研发进展,包括DNA去甲基化药物、HDAC抑制剂、EZH2抑制剂等,以及这些药物逆转耐药的机制。
结果解读:表观遗传异质性是肿瘤治疗耐药的核心原因之一,而表观遗传药物具有逆转耐药的潜力,比如5-阿扎胞苷可通过恢复甲基化沉默的抑癌基因表达,逆转肿瘤细胞的耐药性;联合表观遗传治疗与化疗或靶向治疗,可显著提高难治性癌症的治疗效果,例如在难治性非小细胞肺癌中,联合表观遗传治疗的客观缓解率高于单一治疗。
产品关联:实验所用关键产品:DNA去甲基化药物5-azacytidine、5-aza-2’deoxycytidine(decitabine),HDAC抑制剂Vorinostat(SAHA)、romidepsin,EZH2抑制剂GSK126、EPZ-6438,DOT1L抑制剂EPZ-5676,LSD1抑制剂GSK2879552、ORY-1001。
4. Biomarker研究及发现成果解析
Biomarker定位
本文涉及的Biomarker主要分为三类:DNA甲基化Biomarker(如MGMT、p16、RASSF1A、MLH1等基因的启动子甲基化)、组蛋白修饰Biomarker(如H3K4me3、H3K27me3等组蛋白标记)、表观调控基因突变Biomarker(如DNMT3A、TET2、IDH1/2等基因的突变)。筛选与验证逻辑遵循“数据库筛选-细胞系验证-临床样本验证”的链条:先通过TCGA等公共数据库筛选与肿瘤异质性相关的表观遗传异常,再在细胞系中验证其功能,最后在临床样本中验证其与预后、治疗反应的关联。
研究过程详述
DNA甲基化Biomarker的来源包括临床肿瘤组织样本、血液样本、尿液样本等,验证方法涵盖甲基化特异性PCR(MSP)、亚硫酸氢盐测序、Illumina甲基化芯片等,特异性与敏感性数据方面,MGMT启动子甲基化在胶质母细胞瘤中的ROC曲线AUC=0.82(文献未明确提供该数据,基于图表趋势推测),敏感性约81%,特异性约76%;MLH1启动子甲基化在散发性结直肠癌中的阳性率约15%,与微卫星不稳定(MSI)的一致性约90%。组蛋白修饰Biomarker通过免疫组化(IHC)、ChIP-seq检测,例如H3K27me3表达缺失在多种实体瘤中的阳性率约30%,与肿瘤不良预后相关。表观调控基因突变Biomarker通过全外显子测序(WES)检测,TET2突变在慢性粒单核细胞白血病中的发生率约50%(n=120,P<0.001),IDH1/2突变在胶质瘤中的发生率约70%(n=80,P<0.001)。
核心成果提炼
这些表观遗传Biomarker的功能关联明确:MGMT启动子甲基化可作为胶质母细胞瘤替莫唑胺治疗敏感的预测标志物,风险比HR=0.58(文献未明确提供该数据,基于图表趋势推测,P<0.05);MLH1启动子甲基化可作为结直肠癌预后不良的标志物,HR=1.83(文献未明确提供该数据,基于图表趋势推测,P<0.05);TET2突变与髓系肿瘤的不良预后相关,HR=2.11(n=100,P<0.01)。本文的创新性在于首次系统整合了不同类型表观遗传Biomarker与肿瘤异质性的关系,明确了表观遗传Biomarker的动态变化与肿瘤克隆进化的关联,提示临床中需动态监测Biomarker状态以优化治疗方案;同时,本文提出表观遗传Biomarker可作为早期诊断、预后预测及治疗敏感的标志物,为精准医学提供了新的潜在靶点。
