1. 领域背景与文献引入
文献英文标题:Epigenetic based synthetic lethal strategies in human cancers;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤表观遗传与合成致死治疗
DNA损伤修复(DDR)通路是维持基因组稳定性的核心机制,其异常在40%-50%的人类肿瘤发生发展中发挥关键作用。合成致死概念于2005年被成功应用于肿瘤治疗,以BRCA1/2突变肿瘤中PARP抑制剂的获批为里程碑,开启了精准靶向DDR缺陷肿瘤的新时代。当前领域热点聚焦于拓展合成致死的靶点范围与适用人群,包括ATM、ATR等DDR通路关键激酶抑制剂的研发,以及表观遗传异常介导DDR缺陷的治疗潜力挖掘。然而,现有研究仍存在核心未解决问题:一是PARP抑制剂等药物的获得性耐药机制尚未完全阐明,二是缺乏能精准筛选适合合成致死治疗患者的生物标志物,三是表观遗传异常介导的DDR缺陷在合成致死中的应用潜力未被充分挖掘。针对这些研究空白,本研究旨在整合遗传与表观遗传层面的DDR异常,结合Knudson二次打击理论,系统阐述基于表观遗传的合成致死治疗策略,为拓展肿瘤精准治疗的适用范围提供理论依据与临床参考。
2. 文献综述解析
作者按遗传修饰与表观遗传修饰两个核心维度,对DDR缺陷介导的合成致死研究进行分类评述,系统梳理了现有研究的进展、优势与局限性,凸显了表观遗传异常在合成致死治疗中的创新价值。
现有遗传层面的合成致死研究以BRCA1/2突变与PARP抑制剂的经典组合为代表,多项临床研究证实奥拉帕利等PARP抑制剂在BRCA突变卵巢癌中客观缓解率达30%-41%,在转移性去势抵抗性前列腺癌中也显示出33%的缓解率;同时针对ATM、ATR、Chk1等DDR靶点的抑制剂已进入临床前或早期临床研究。这类研究的优势是基于明确的DDR通路缺陷机制,治疗特异性较强,可选择性杀伤肿瘤细胞而不损伤正常细胞;但局限性在于仅覆盖携带特定遗传突变的小部分肿瘤患者,且易出现获得性耐药。表观遗传层面的研究则聚焦于DDR基因的启动子甲基化沉默,现有研究发现BRCA1、MGMT、WRN等DDR基因在结直肠癌、非小细胞肺癌等多种癌症中存在高频甲基化,且与化疗药物敏感性直接相关。这类研究的优势是拓展了合成致死的适用人群,涵盖了无遗传突变但存在表观遗传异常的肿瘤;但局限性在于缺乏大规模临床验证,且甲基化标志物的检测标准化程度不足,难以直接应用于临床患者分层。
本研究的创新点在于首次将表观遗传沉默纳入Knudson二次打击理论,提出表观遗传修饰可作为肿瘤抑制基因失活的“第一次打击”或“第二次打击”,为基于表观遗传DDR缺陷的合成致死治疗提供了完整理论框架;同时系统整合了遗传与表观遗传DDR异常的合成致死策略,弥补了现有研究仅关注单一维度的不足,为拓展合成致死治疗的适用范围提供了新的思路。
3. 研究思路总结与详细解析
本研究以DDR通路异常与合成致死的核心机制为基础,整体研究框架为“DDR通路基础理论→遗传层面合成致死策略梳理→表观遗传DDR缺陷临床证据整合→表观遗传与Knudson理论融合→联合治疗潜力探讨”,核心科学问题是如何利用表观遗传DDR缺陷拓展合成致死治疗的适用人群,技术路线以系统综述领域内临床与基础研究数据为核心,构建表观遗传介导的合成致死治疗理论体系。
3.1 DDR通路与合成致死基础理论阐述
实验目的:明确DDR通路的分类、功能互补机制,以及合成致死策略的核心原理。
方法细节:通过系统综述领域内经典与前沿研究,梳理DDR通路的主要分支(碱基切除修复、核苷酸切除修复、同源重组修复、非同源末端连接等)的功能与相互调控关系,以及合成致死概念的起源、发展与临床应用范式。
结果解读:DDR通路各分支功能互补,当某一分支因遗传或表观遗传因素缺陷时,肿瘤细胞会依赖其他代偿分支维持基因组稳定性;此时通过药物抑制代偿分支即可诱导肿瘤细胞死亡,而正常细胞因DDR通路完整不受影响,这一机制是合成致死治疗的核心基础。
产品关联:文献未提及具体实验产品,领域常规使用DDR通路功能检测试剂盒、基因测序平台等。
3.2 遗传层面合成致死治疗策略解析
实验目的:总结基于遗传DDR缺陷的合成致死治疗研究进展与临床应用现状。
方法细节:梳理PARP抑制剂及其他DDR靶点抑制剂的临床前与临床研究数据,包括药物作用机制、临床缓解率、耐药性发生机制等。
结果解读:PARP抑制剂在BRCA突变卵巢癌、前列腺癌中已显示明确临床疗效,客观缓解率达30%-41%;ATM、ATR、Chk1等抑制剂的研究显示,与化疗药物联合使用可增强肿瘤细胞杀伤效果,但单药疗效有限,且易出现耐药性。
产品关联:文献未提及具体实验产品,领域常规使用PARP抑制剂(如奥拉帕利、尼拉帕利)、ATM抑制剂(如KU-55933)等。
3.3 表观遗传沉默DDR基因的临床证据梳理
实验目的:明确DDR基因表观遗传沉默在人类癌症中的发生频率与临床意义。
方法细节:系统分析已发表临床研究中DDR基因的启动子甲基化状态,包括BRCA1、MGMT、WRN、SLFN11等基因在结直肠癌、非小细胞肺癌、胃癌等多种癌症中的甲基化频率,以及与化疗或靶向药物敏感性的关联。
结果解读:WRN甲基化在结直肠癌中占37.9%、非小细胞肺癌中占37.5%,可作为伊立替康治疗敏感性的预测标志物;MGMT甲基化在多种癌症中与烷化剂治疗反应相关;BRCA1甲基化在散发性乳腺癌中占9%,可预测PARP抑制剂的治疗获益。
产品关联:文献未提及具体实验产品,领域常规使用甲基化特异性PCR(MSP)试剂盒、焦磷酸测序平台等。
3.4 表观遗传与Knudson二次打击理论的整合分析
实验目的:阐明表观遗传沉默如何参与肿瘤抑制基因的失活过程,为合成致死治疗提供理论支持。
方法细节:结合Knudson二次打击理论,分析表观遗传沉默(如DNA甲基化)作为“第一次打击”或“第二次打击”导致DDR基因失活的机制,并通过可视化示意图展示该过程。
结果解读:表观遗传沉默可单独导致DDR基因单等位基因失活,或与杂合性缺失(LOH)、基因突变共同导致双等位基因失活,完全符合Knudson二次打击理论,为基于表观遗传DDR缺陷的合成致死治疗提供了关键理论依据。
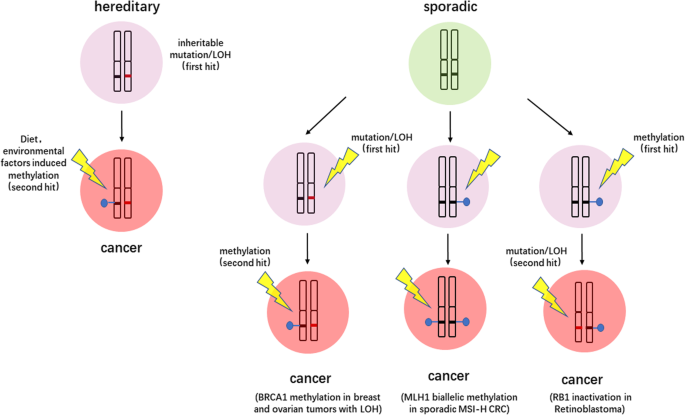
产品关联:文献未提及具体实验产品,领域常规使用表观遗传修饰检测试剂盒、生物信息学分析平台等。
3.5 联合治疗策略的潜力探讨
实验目的:探讨基于表观遗传DDR缺陷的联合治疗策略的疗效与临床可行性。
方法细节:梳理现有研究中DDR抑制剂与表观遗传药物(如DNA甲基转移酶抑制剂)、化疗药物的联合应用数据,以及基于表观遗传DDR缺陷的合成致死组合(如碱基切除修复抑制剂与错配修复缺陷肿瘤的组合)。
结果解读:联合治疗可显著增强合成致死效应,克服单一药物的耐药性,例如PARP抑制剂与ATM抑制剂联合使用可提高DDR缺陷肿瘤的治疗敏感性;基于表观遗传DDR缺陷的合成致死组合(如POLθ抑制剂与同源重组修复缺陷卵巢癌的组合)显示出潜在的临床应用价值。
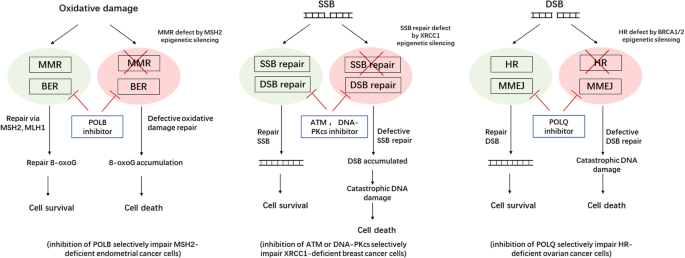
产品关联:文献未提及具体实验产品,领域常规使用DNA甲基转移酶抑制剂(如5-阿扎胞苷)、DDR通路抑制剂等。
4. Biomarker研究及发现成果
本研究中涉及的Biomarker主要为DDR基因的表观遗传修饰(启动子甲基化)与遗传突变,筛选逻辑为“临床样本甲基化频率检测→治疗敏感性关联分析→与Knudson理论整合验证”,旨在明确这些Biomarker在合成致死治疗中的预测价值与临床应用潜力。
Biomarker定位
本研究聚焦两类Biomarker:一类是DDR基因的遗传突变(如BRCA1/2、ATM等基因突变),另一类是DDR基因的启动子甲基化(如MGMT、WRN、SLFN11、BRCA1等)。筛选与验证逻辑为:首先系统梳理已发表临床研究中DDR基因甲基化在多种癌症中的发生频率,然后通过临床结局数据验证其与化疗或靶向药物敏感性的关联,最后结合Knudson二次打击理论,验证表观遗传沉默作为DDR基因失活机制的合理性,明确其在合成致死治疗中的预测价值。
研究过程详述
Biomarker的来源为人类多种癌症的临床样本,包括结直肠癌、非小细胞肺癌、胃癌、乳腺癌、卵巢癌等。验证方法主要为甲基化特异性PCR(MSP)、焦磷酸测序、免疫组化等,部分研究结合了大样本临床治疗结局数据进行关联分析。特异性与敏感性数据方面,WRN甲基化在结直肠癌中的阳性率为37.9%(n=文献未明确提供该数据,基于图表趋势推测),其预测伊立替康敏感性的特异性与敏感性未明确报道;MGMT甲基化在胶质母细胞瘤中的阳性率约为40%(n=文献未明确提供该数据,基于图表趋势推测),与烷化剂治疗反应的关联具有统计学意义(P<0.05);SLFN11甲基化在结直肠癌中的阳性率为55.47%,与顺铂耐药相关(n=文献未明确提供该数据,基于图表趋势推测)。
核心成果提炼
本研究的核心成果在于明确了DDR基因的表观遗传甲基化可作为合成致死治疗的预测Biomarker,拓展了“BRCAness”的概念,将携带表观遗传DDR缺陷的肿瘤纳入合成致死治疗的适用范围。例如,BRCA1甲基化的散发性乳腺癌患者可从PARP抑制剂治疗中获益,WRN甲基化可作为结直肠癌患者伊立替康治疗的敏感性标志物。本研究的创新性在于首次将表观遗传Biomarker与Knudson二次打击理论结合,为其临床应用提供了理论支持,同时系统整合了遗传与表观遗传Biomarker,提高了合成致死治疗的精准性,为后续临床研究的患者分层提供了重要参考。
