1. 领域背景与文献引入
文献英文标题:A phase 1 study of dalpiciclib, a cyclin-dependent kinase 4/6 inhibitor in Chinese patients with advanced breast cancer;发表期刊:Biomark Res;影响因子:未公开;研究领域:肿瘤学-晚期乳腺癌靶向治疗
细胞周期失调是恶性肿瘤的核心特征之一,周期蛋白D(CCND)-周期蛋白依赖性激酶4/6(CDK4/6)轴调控细胞从G1期向S期的转换,在激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)乳腺癌的发生发展中发挥关键作用。2015年帕博西尼作为全球首个CDK4/6抑制剂获批上市,开启了晚期乳腺癌靶向治疗的新时代,随后瑞博西尼、阿贝西尼相继获批,联合内分泌治疗可将HR+/HER2-晚期乳腺癌患者的中位无进展生存期(PFS)从10个月左右延长至20个月以上,成为该领域的标准治疗方案。但现有研究的入组人群以西方患者为主,中国人群的药代动力学及耐受性数据相对匮乏,且经多线治疗后的耐药患者仍缺乏有效治疗选择。达尔西利(SHR6390)是中国自主研发的新型高选择性CDK4/6抑制剂,临床前研究显示其具有良好的抗肿瘤活性及克服内分泌耐药的潜力,因此开展本首次人体I期研究,旨在评估其在中国晚期乳腺癌患者中的耐受性、药代动力学、安全性及初步抗肿瘤活性。
2. 文献综述解析
作者围绕CDK4/6通路的致癌机制、现有CDK4/6抑制剂的临床应用现状、内分泌治疗耐药的核心问题及达尔西利的临床前研究证据展开系统性综述,明确了中国晚期乳腺癌患者对自主研发CDK4/6抑制剂的临床需求。
现有CDK4/6抑制剂的核心研究结论为,联合内分泌治疗可显著延长HR+/HER2-晚期乳腺癌患者的PFS,改善生存质量;技术方法优势在于采用大样本随机对照试验设计,循证医学证据等级高,且不同药物的毒性谱各具特点,可满足不同患者的个体化治疗需求;但局限性在于现有研究的入组人群以西方患者为主,中国人群的药代动力学及耐受性数据不足,针对经多线治疗后的晚期患者,单药CDK4/6抑制剂的疗效数据仍较为有限,且内分泌治疗耐药的机制尚未完全阐明,缺乏针对性的逆转策略。本研究的创新价值在于首次在中国HR+/HER2-晚期乳腺癌患者中开展达尔西利的首次人体试验,填补了中国人群的临床数据空白,同时评估了单药治疗在经多线治疗患者中的初步疗效,为后续联合治疗研究提供了关键依据。
3. 研究思路总结与详细解析
本研究采用开放标签、3+3剂量递增联合剂量扩展的I期临床研究设计,核心目标是确定达尔西利在中国晚期乳腺癌患者中的最大耐受剂量(MTD)、药代动力学特征,同时评估其安全性及初步抗肿瘤活性,研究逻辑遵循“剂量递增探索安全性→剂量扩展验证疗效与药代动力学→综合分析确定II期推荐剂量”的临床研究常规路径。
3.1 研究设计与患者入组
实验目的是筛选符合入组标准的晚期乳腺癌患者,明确基线特征以确保研究人群的代表性;方法细节为2016年4月至2018年12月在中国开展研究,入组标准为18-65岁、组织学确诊的HR+/HER2-晚期乳腺癌、标准治疗失败、美国东部肿瘤协作组(ECOG)体能状态评分0-1、器官功能良好,排除既往接受CDK4/6抑制剂治疗、未控制的脑转移等患者;结果解读为共筛选58例患者,40例符合标准入组,所有患者均为IV期HR+/HER2-乳腺癌,45%接受过至少3线化疗,55%接受过至少2线内分泌治疗,中位随访7.0个月,70%因疾病进展停药,25%仍在治疗,无死亡病例;产品关联:文献未提及具体实验产品,领域常规使用电子病历系统采集患者基线数据,采用免疫组化(IHC)检测激素受体及HER2表达状态。
3.2 剂量递增与扩展方案
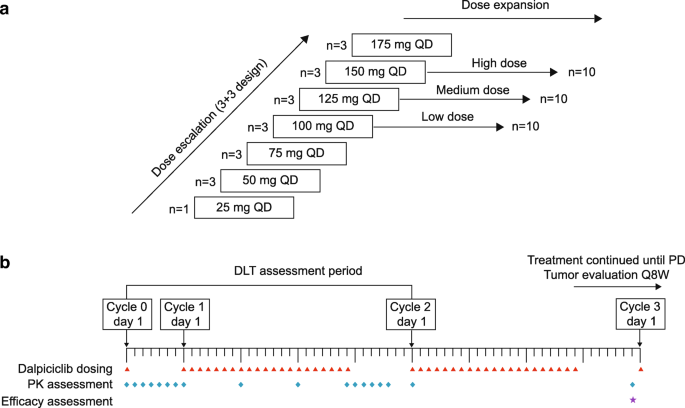
实验目的是探索达尔西利的MTD,确定适合扩展的剂量队列;方法细节采用传统3+3剂量递增设计,起始剂量25mg,以25mg递增至175mg,采用“3周给药、1周停药”的28天周期,先给予单剂量,洗脱≥7天后开始连续给药,剂量限制性毒性(DLT)定义为4级血液学毒性、伴感染/发热的3级中性粒细胞减少等,基于剂量递增阶段的耐受性、药代动力学及疗效数据,选择100mg、125mg、150mg队列各扩展至10例患者;结果解读为所有剂量队列均未观察到DLT,MTD未达到,150mg队列因暴露量更高且疗效更优被优先选择扩展,随后基于安全性考虑扩展125mg和100mg队列,扩展队列同样未观察到DLT;产品关联:文献未提及具体实验产品,领域常规使用临床研究随机化系统进行剂量队列分配,采用电子数据采集系统记录给药及毒性事件。
3.3 安全性与耐受性评估
实验目的是评估达尔西利在中国患者中的安全性及耐受性,明确毒性谱特征;方法细节采用美国国立癌症研究所常见不良反应事件评价标准(CTCAE)4.0版对治疗期间出现的不良反应(TEAE)进行分级,监测从知情同意至末次给药后30天的所有不良事件;结果解读为所有患者均出现至少1例TEAE,55%的患者出现3/4级TEAE,主要为中性粒细胞减少(52.5%)、白细胞减少(35.0%),无严重不良事件或因不良反应停药的病例,非血液学毒性主要为天门冬氨酸氨基转移酶(AST)升高(40.0%)、丙氨酸氨基转移酶(ALT)升高(32.5%),多为1级,仅3例为2级,QT间期延长发生率为12.5%,均未超过500ms;产品关联:文献未提及具体实验产品,领域常规采用全自动血液分析仪检测血常规指标,采用生化分析仪检测肝肾功能,采用心电图监测QT间期。
3.4 药代动力学分析
实验目的是明确达尔西利在中国患者中的药代动力学特征,为给药方案提供依据;方法细节在单剂量阶段(第1天)和多剂量阶段(第1周期第1、8、15、21天等时间点)采集血样,采用高效液相色谱-串联质谱法(LC-MS/MS)检测血浆达尔西利浓度,采用非房室模型分析药代动力学参数;结果解读为50-175mg剂量范围内,稳态药时曲线下面积(AUCss)和峰浓度(Cmax)随剂量增加呈近似线性增长,达峰时间(Tmax)为2.5-4.0h,终末半衰期(t1/2)为40.3-51.4h,多剂量给药后第8天达到稳态,蓄积比为1.9-3.4,提示药物分布广泛,支持每日一次给药方案;产品关联:文献未提及具体实验产品,领域常规使用LC-MS/MS系统进行血浆药物浓度检测,采用WinNonlin软件进行药代动力学参数分析。
3.5 初步抗肿瘤疗效评估
实验目的是评估达尔西利单药治疗在中国晚期乳腺癌患者中的初步抗肿瘤活性;方法细节采用实体瘤疗效评价标准(RECIST)1.1版,每2个周期(8周)通过计算机断层扫描(CT)或磁共振成像(MRI)评估肿瘤疗效,计算疾病控制率(DCR)、客观缓解率(ORR)及无进展生存期(PFS);结果解读为所有40例患者均可评估疗效,ORR为5%(2例部分缓解),缓解持续时间分别为169天和356+天,DCR为62.5%(95%CI:45.8-77.3),中位PFS为4.0个月(95%CI:2.4-9.1),其中150mg队列的DCR最高(80.0%,95%CI:44.4-97.5),中位PFS最长(8.4个月,95%CI:2.1-未达到);产品关联:文献未提及具体实验产品,领域常规采用CT/MRI设备进行肿瘤影像学评估,采用Kaplan-Meier法分析PFS数据。
4. Biomarker研究及发现成果解析
本研究未开展专门的Biomarker筛选与验证,但基于临床前研究及现有CDK4/6抑制剂的研究证据,明确了达尔西利的作用依赖于功能性视网膜母细胞瘤蛋白(Rb),并间接评估了其在HR+/HER2-患者中的疗效,为后续Biomarker研究提供了方向。
Biomarker定位为功能性Rb蛋白,筛选逻辑基于CDK4/6抑制剂的核心作用机制——通过抑制CDK4/6-Rb通路阻滞细胞周期,临床前研究显示达尔西利的抗肿瘤活性严格依赖于Rb的表达;研究过程详述为入组患者均为HR+/HER2-乳腺癌,该亚型通常保留功能性Rb,本研究未直接采用免疫组化(IHC)检测Rb表达,但通过疗效数据间接验证了Rb通路的作用,150mg队列的更高疗效提示足够的药物暴露可更好地抑制Rb通路;核心成果提炼为达尔西利在HR+/HER2-晚期乳腺癌患者中显示出初步抗肿瘤活性,尤其是在150mg剂量下,DCR达80.0%,中位PFS达8.4个月(n=10,95%CI:2.1-未达到),创新性在于首次在中国人群中证实了自主研发CDK4/6抑制剂针对Rb通路的抗肿瘤活性,为后续开展Rb表达与疗效相关性的Biomarker研究提供了临床依据;由于本研究未直接检测Rb表达,因此未获得特异性与敏感性数据,推测:Rb阳性的HR+/HER2-晚期乳腺癌患者可能从达尔西利治疗中获得更大获益,需在后续研究中通过免疫组化检测Rb表达进行验证。
