1. 领域背景与文献引入
文献英文标题:Selective isolation of extracellular vesicles from minimally processed human plasma as a translational strategy for liquid biopsies;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤液体活检、细胞外囊泡分离与生物标志物研究。
细胞外囊泡(EVs)作为介导细胞间通讯的载体,能携带反映细胞病理生理状态的核酸、蛋白等生物分子,在近15年成为液体活检领域的研究热点。领域共识:传统细胞外囊泡分离方法如超速离心、尺寸排阻色谱依赖物理特性(密度、尺寸),在细胞培养上清等简单样本中可获得大量细胞外囊泡,但在血浆等复杂生物样本中,由于非囊泡颗粒(如脂蛋白、蛋白聚集体)的干扰,会引入大量污染物,且这类方法无法富集特定功能的细胞外囊泡亚群,难以适配临床常规检测流程。当前研究热点聚焦于细胞外囊泡亚群的选择性分离,因为细胞外囊泡异质性极高,不同亚群携带的生物标志物具有不同的临床价值,但现有亲和分离方法普遍存在特异性不足、未充分考虑血浆基质对分离效率的影响等问题,核心研究空白是缺乏可临床转化的、高特异性的细胞外囊泡亚群分离策略,尤其是针对早期癌症检测的液体活检需求,亟需建立能在复杂血浆基质中高效分离特定细胞外囊泡亚群的方法,并验证其临床应用价值。本文针对这一空白,系统优化了基于纳米磁珠的细胞外囊泡免疫亲和分离体系,探索了不同细胞外囊泡亚群在早期非小细胞肺癌(NSCLC)液体活检中的临床潜力。
2. 文献综述解析
作者对领域内现有研究的分类维度为分离方法的原理,分为依赖物理特性的分离方法和基于亲和捕获的分离方法两类,重点对比不同方法在复杂样本中的性能及临床转化可行性。现有研究中,物理分离方法(超速离心、尺寸排阻色谱)的优势是能从简单样本中获得大量细胞外囊泡,可用于细胞外囊泡的无偏性表征,但在血浆等复杂样本中,由于非囊泡颗粒与细胞外囊泡的物理特性(尺寸、密度)存在重叠,分离产物纯度低,且无法靶向特定细胞外囊泡亚群;亲和分离方法如芯片、磁珠捕获能通过表面标志物靶向特定细胞外囊泡亚群,但其局限性在于多数研究未充分验证分离的特异性,也未考虑血浆基质成分对亲和反应的干扰,缺乏标准化的性能评估体系,导致方法的可重复性和临床转化可行性不足。本文的创新价值在于,首次系统对比了共价偶联抗体磁珠与链霉亲和素包被磁珠的细胞外囊泡分离性能,明确了共价偶联磁珠在复杂血浆基质中的特异性优势;建立了基于荧光标记细胞外囊泡spike-in模型的分离效率定量评估体系,揭示了细胞外囊泡表面表型和血浆基质异质性对分离效率的影响;首次在临床样本中证明血小板来源细胞外囊泡亚群(CD61+)携带的mRNA能有效区分健康人和早期NSCLC患者,为早期癌症液体活检提供了新的生物标志物来源,弥补了现有研究在临床转化验证方面的不足。
3. 研究思路总结与详细解析
本研究的整体框架为:以优化高特异性的细胞外囊泡亚群免疫亲和分离方法为核心,通过模型实验验证方法性能,解析分离效率的影响因素,建立细胞外囊泡表面标志物检测体系,最终在临床样本中验证不同细胞外囊泡亚群的液体活检价值。核心科学问题包括如何在复杂血浆基质中实现细胞外囊泡亚群的高效、特异性分离,以及不同细胞外囊泡亚群携带的生物标志物在早期NSCLC检测中的差异价值。技术路线遵循“方法优化→性能验证→影响因素分析→临床应用”的闭环逻辑,通过多组实验逐步验证研究假设。
3.1 磁珠分离体系优化与性能验证
实验目的:对比共价偶联抗体磁珠(MACS)与链霉亲和素包被磁珠(MACS-STV)在细胞外囊泡免疫沉淀中的特异性和回收率,筛选适用于复杂血浆基质的分离工具。
方法细节:采用CFSE标记HEK293细胞来源的细胞外囊泡作为可追踪的spike-in模型,分别在PBS-BSA(简单基质)和健康人血浆(复杂基质)中进行免疫沉淀反应;通过荧光读数直接检测磁珠上的细胞外囊泡回收率,或通过检测上清中剩余荧光信号间接计算回收率;采用ddPCR检测HEK293细胞特异性标记CA9的mRNA,验证回收产物的特异性;通过冷冻透射电镜(Cryo-TEM)观察磁珠-细胞外囊泡复合物的结构。
结果解读:在简单基质中,MACS磁珠的特异性达89%,能回收100%的CD9+细胞外囊泡亚群(n=3,P<0.001),而MACS-STV的特异性仅44%;在血浆基质中,MACS磁珠的特异性达78%,ddPCR检测到CA9 mRNA的表达,验证了回收产物为spike-in的HEK293细胞外囊泡(n=3,P<0.01);Cryo-TEM图像显示细胞外囊泡结构完整,磁珠可结合在细胞外囊泡表面。
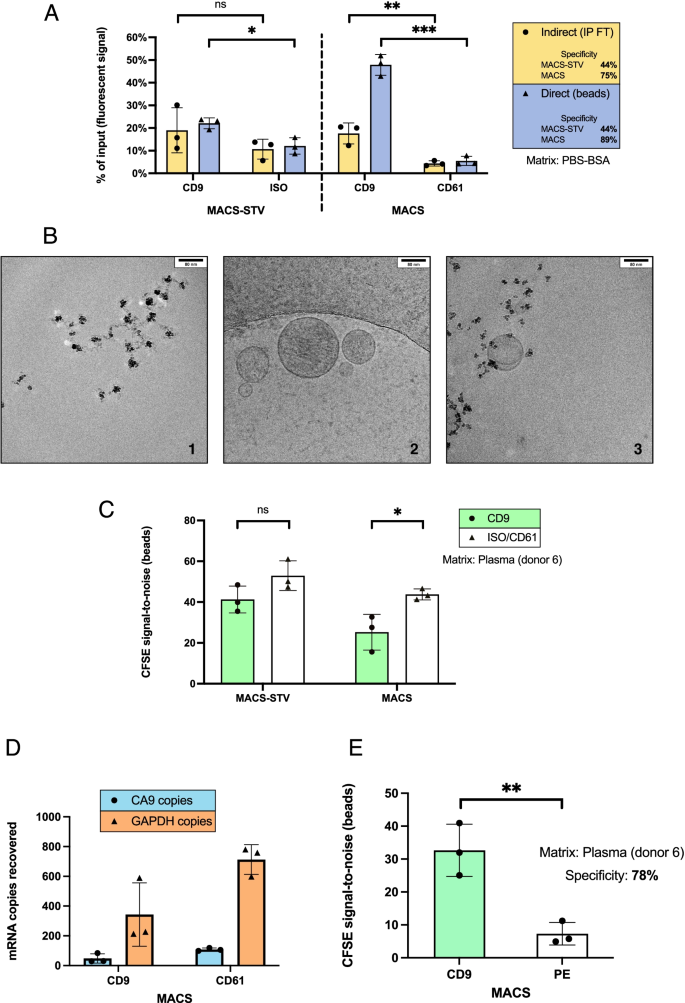
实验所用关键产品:Miltenyi Biotec的MACS磁珠、Thermo Fisher Scientific的CellTrace™ CFSE染色剂、Bio-Rad的ddPCR试剂盒、nanoFCM Inc.的纳米流式细胞仪。
3.2 细胞外囊泡分离效率影响因素分析
实验目的:探究细胞外囊泡表面表型和血浆基质异质性对分离效率的影响,明确分离体系的适用条件。
方法细节:分别用NIR标记22RV1细胞来源细胞外囊泡、CFSE标记HT29/HEK293/A549细胞来源细胞外囊泡作为spike-in模型,在3例不同健康人血浆样本中进行免疫沉淀,检测不同细胞来源细胞外囊泡的回收率;优化孵育时间(10min、25min、60min)、血浆稀释度(1:2至1:20)等实验条件,评估对分离效率的影响。
结果解读:不同细胞来源的细胞外囊泡回收率存在显著差异,HT29细胞外囊泡在不同血浆样本中的回收率差异达3倍(n=3,P<0.05),HEK293细胞外囊泡在部分血浆样本中的回收率高于简单基质,表明细胞外囊泡表面表型和血浆基质组成共同影响分离效率;孵育60min时回收率最高,血浆稀释对回收率无显著影响(n=2,P>0.05)。
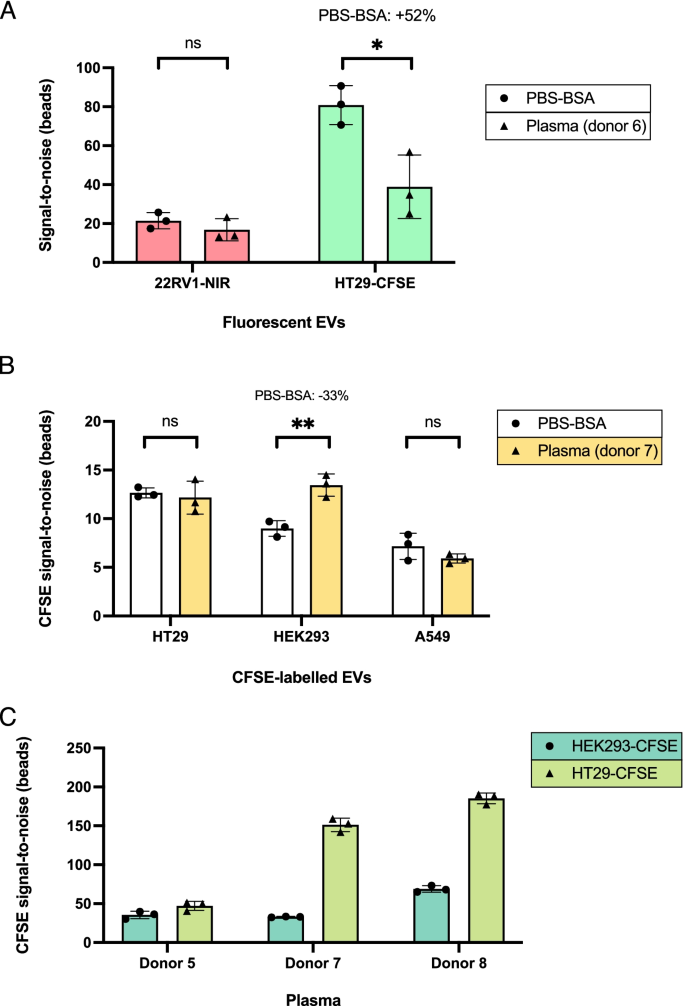
实验所用关键产品:Thermo Fisher Scientific的NIR荧光探针、Izon Science的尺寸排阻色谱柱。
3.3 细胞外囊泡表面标志物检测方法建立
实验目的:建立基于磁珠的细胞外囊泡表面标志物直接检测方法,验证方法的特异性和多标记检测能力。
方法细节:用MACS磁珠分离血浆中的细胞外囊泡后,直接在磁珠上进行荧光抗体染色(如CD41-PE、CD9-AF488),通过酶标仪检测荧光信号;采用凝血酶处理或56℃加热处理血浆,分离血小板来源细胞外囊泡后检测标志物表达变化,验证检测的特异性;同时进行双标记染色,评估多标志物检测的可行性。
结果解读:CD41-PE在血小板来源细胞外囊泡上的荧光信号显著高于同型对照抗体(n=3,P<0.01),证明检测方法的特异性;双标记染色(CD41-PE+CD9-AF488)的荧光信号与单标记染色相当,表明多标志物检测不影响信号强度;血浆处理后,CD41的荧光信号显著下降(n=3,P<0.05),验证了检测信号来源于血小板来源细胞外囊泡。
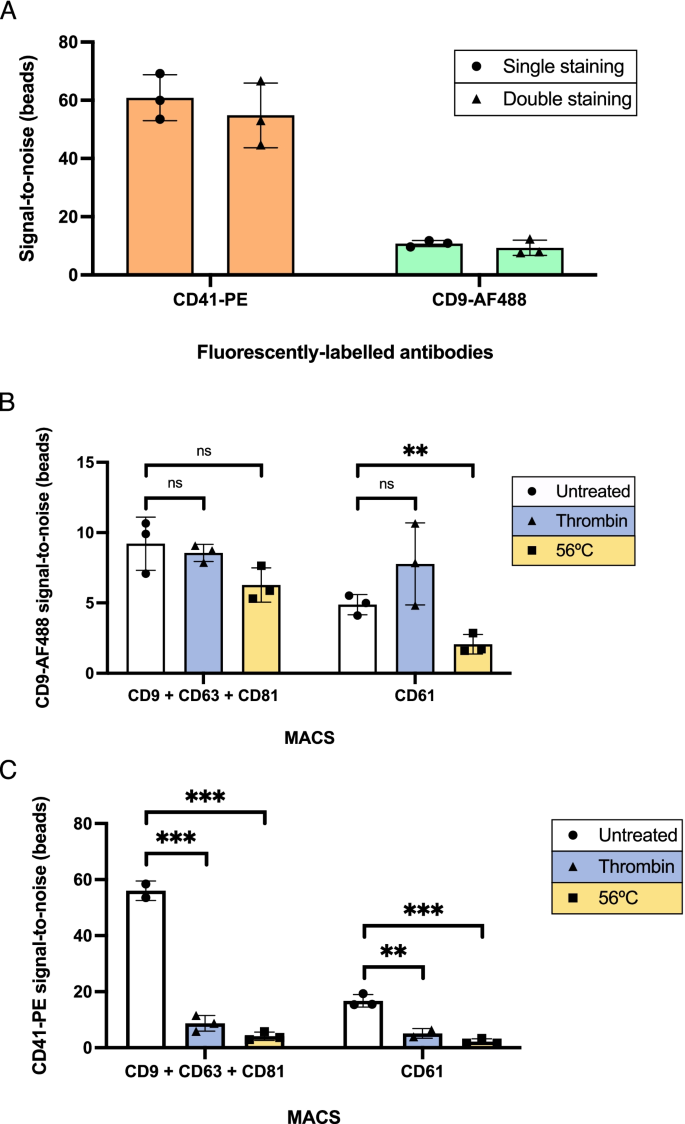
实验所用关键产品:Exbio Praha的荧光标记抗体、PerkinElmer的黑色不透明96孔板、BMG Labtech的CLARIOstar Plus酶标仪。
3.4 临床样本细胞外囊泡亚群mRNA测序分析
实验目的:对比不同细胞外囊泡亚群(CD9/CD63/CD81+ vs CD61+)的mRNA表达谱,验证其在早期NSCLC液体活检中的临床价值。
方法细节:从14例健康人和14例早期NSCLC患者的血浆中,分别分离CD9/CD63/CD81+细胞外囊泡亚群和CD61+细胞外囊泡亚群;采用NanoString nCounter平台对594个免疫相关基因的mRNA表达进行检测,通过生物信息学流程(质量控制、低表达基因过滤、标准化、差异表达分析)分析两组样本的基因表达差异。
结果解读:在健康人样本中,CD61+细胞外囊泡的mRNA计数显著高于CD9/CD63/CD81+细胞外囊泡(p=0.00053,Wilcoxon检验),且存在4个差异表达基因;在临床样本中,CD61+细胞外囊泡的mRNA谱能有效区分健康人和早期NSCLC患者,共鉴定出47个差异表达基因(调整P<0.05,log2 fold change>2),而CD9/CD63/CD81+细胞外囊泡亚群未检测到显著差异表达基因。
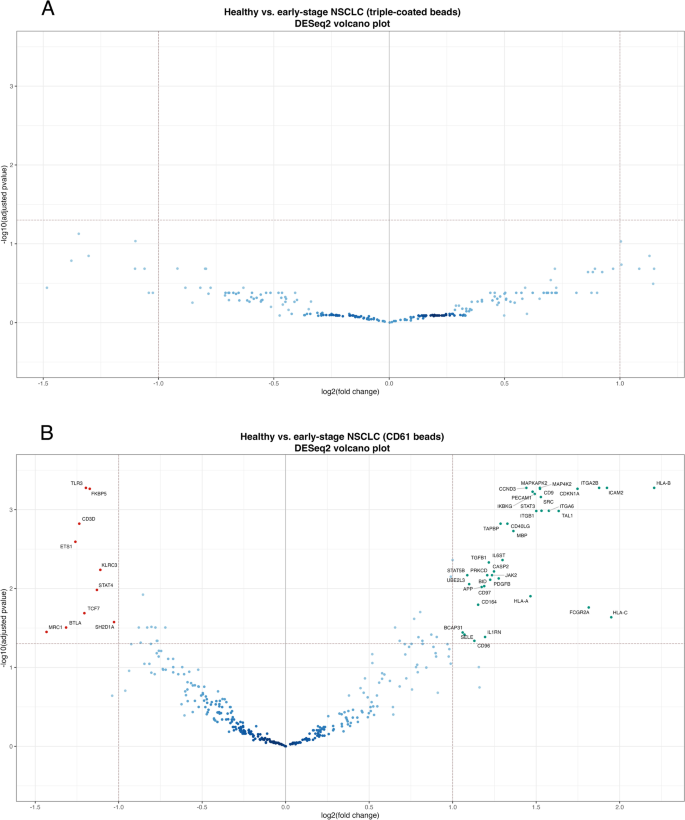
实验所用关键产品:NanoString Technologies的nCounter Human Immunology v2 Panel、DESeq2生物信息学分析工具。
4. Biomarker研究及发现成果解析
Biomarker定位:本文涉及的生物标志物为血小板来源细胞外囊泡亚群(CD61+)及其携带的mRNA标志物,筛选与验证逻辑为:首先通过优化的免疫亲和分离方法富集特定细胞外囊泡亚群,在健康人样本中验证亚群的特异性,随后在临床样本中对比健康人与早期NSCLC患者的mRNA表达谱,筛选差异表达基因作为潜在生物标志物。
研究过程详述:该生物标志物的来源为健康人和早期NSCLC患者的血浆样本,验证方法包括:采用免疫亲和磁珠分离CD61+细胞外囊泡亚群,通过NanoString nCounter平台进行mRNA表达谱检测;特异性方面,CD61+细胞外囊泡的mRNA谱在健康人与早期NSCLC患者间存在显著差异,共鉴定出47个差异表达基因(调整P<0.05,log2 fold change>2),敏感性与特异性数据未通过ROC曲线直接给出,但临床样本的分组对比证明该亚群能有效区分两组人群(n=14/组)。
核心成果提炼:该生物标志物的功能关联为,血小板来源细胞外囊泡亚群携带的mRNA可作为早期NSCLC的液体活检生物标志物,风险比等生存分析数据未在本文中提供;创新性在于首次在临床样本中证明血小板来源细胞外囊泡亚群在早期NSCLC检测中的价值,明确了细胞外囊泡亚群分离的临床意义,为早期癌症液体活检提供了新的生物标志物来源;统计学结果显示,差异表达基因的调整P值均小于0.05,样本量为每组14例,具有统计学显著性。
