1. 领域背景与文献引入
文献英文标题:Evidence for the biogenesis of more than 1,000 novel human microRNAs;发表期刊:Genome Biology;影响因子:10.433(2014年);研究领域:非编码RNA(微小核糖核酸)研究
微小核糖核酸(miRNA)是调控基因表达的关键非编码RNA,2001年被系统发现后成为发育生物学、肿瘤学等领域的研究热点。领域发展关键节点包括:2001年首次在动物中系统发现miRNA;2008年高通量小RNA测序技术普及,推动miRNA大规模发现;到2014年miRBase数据库已收录约2000个人类miRNA基因。当前研究热点集中在miRNA调控网络解析、疾病标志物开发及靶向治疗,但未解决的核心问题是,人类基因组中miRNA的实际总量尚未被系统评估,低丰度、组织特异性miRNA因检测技术限制被大量遗漏。
针对这一研究空白,本研究采用创新计算方法结合大规模合并的小RNA测序数据,系统发现并验证了大量新型人类miRNA,为扩展人类miRNA库、解析复杂基因调控网络提供了重要基础,填补了领域内对人类miRNA组规模认知的空白。
2. 文献综述解析
作者对现有miRNA研究的分类维度主要包括技术方法(Sanger测序、高通量小RNA测序)、研究内容(miRNA发现、功能验证、靶标鉴定)及进化特征(保守miRNA、物种特异性miRNA)。
现有研究中,早期miRNA发现依赖Sanger测序,仅能检测高丰度的保守miRNA;高通量小RNA测序技术出现后,miRNA发现效率大幅提升,但单个数据集测序深度不足,难以检测低丰度、组织特异性miRNA;已有的功能研究局限于已知miRNA,明确了其经典生物发生途径及在疾病中的作用,但未系统挖掘人类基因组中潜在的新型miRNA,导致对人类miRNA总量的认知严重不足。
与现有研究相比,本研究首次采用94个公共小RNA测序数据集的合并分析,突破了单个数据集的深度限制,结合CLIP-seq、CLASH等技术,从生物发生、蛋白结合、靶标调控多个层面验证新型miRNA,最终确认1098个新型人类miRNA,证明人类miRNA总量远大于已知数量,为领域提供了全新的miRNA资源库,推动了对人类基因调控网络复杂性的认知。
3. 研究思路总结与详细解析
本研究的整体目标是系统发现并验证人类新型微小核糖核酸,核心科学问题是人类基因组中微小核糖核酸的实际总量远大于已注释的约2000个,技术路线遵循“数据合并预测→细胞水平验证→分子互作验证→功能关联分析”的闭环逻辑,通过多组学技术交叉验证,确保新型miRNA的可靠性。
3.1 合并小RNA测序数据集的新型miRNA预测
本环节的核心目标是从大规模公共测序数据中挖掘未被注释的新型微小核糖核酸候选。实验方法上,研究团队收集了94个来自人类组织和细胞系的小RNA测序数据集,合并后使用bowtie工具将测序读段比对到人类基因组hg19版本,过滤掉重复序列、已知微小核糖核酸、转运RNA(tRNA)、核糖体RNA(rRNA)等非目标序列;随后用MiPred工具预测剩余序列的RNA发夹结构,筛选符合微小核糖核酸前体特征的序列;最后用miRDeep2工具验证读段的Dicer加工特征,确保候选序列符合经典微小核糖核酸生物发生规律。结果显示,该流程共得到2469个新型微小核糖核酸候选,其中420个候选可检测到形成双链的证据,其读段分布完全符合Dicer加工的特征,说明这些候选序列具有典型的微小核糖核酸结构与加工特征。
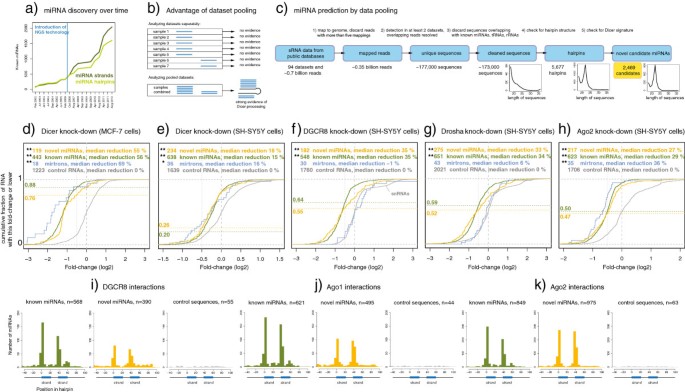
产品关联:文献未提及具体实验产品,领域常规使用bowtie、miRDeep2等生物信息学工具,MiPred用于RNA二级结构预测。
3.2 神经元细胞系中miRNA生物发生途径验证
本环节旨在验证新型微小核糖核酸候选依赖经典的微小核糖核酸生物发生途径。实验方法上,研究团队在分化的SH-SY5Y神经母细胞瘤细胞中,采用RNA干扰技术分别沉默Dicer、Drosha、DGCR8、Ago2这四个核心生物发生因子,其中DGCR8和Drosha采用两次转染的方式提升沉默效率,Dicer和Ago2采用单次转染;转染72小时后提取总RNA,构建小RNA测序文库并测序。结果显示,295个新型微小核糖核酸候选在沉默生物发生因子后表达显著下调,下调幅度为18%-35%(P<0.001),与已知微小核糖核酸的下调幅度(15%-35%)相当,说明这些新型微小核糖核酸的表达依赖经典的生物发生途径。
产品关联:实验所用关键产品:Dharmacon的靶向DGCR8、Drosha、Dicer、Ago2的小干扰RNA(siRNA),Qiagen的miRNeasy Mini试剂盒用于总RNA提取,Illumina的TruSeq Small RNA Sample Preparation试剂盒用于构建测序文库。
3.3 交联免疫沉淀测序验证与关键蛋白的相互作用
本环节的核心目标是验证新型微小核糖核酸候选与微小核糖核酸生物发生关键蛋白的直接结合。实验方法上,研究团队重分析了已发表的HEK293细胞中DGCR8、Ago1、Ago2的交联免疫沉淀测序(CLIP-seq)数据,将新型微小核糖核酸候选的序列与CLIP-seq的标签序列进行比对,分析结合位置的特征。结果显示,390-975个新型微小核糖核酸候选与这些蛋白存在直接结合,结合位置集中在微小核糖核酸前体的成熟链区域,其中796个新型微小核糖核酸的成熟链序列与Ago蛋白的CLIP-seq标签完全匹配,说明这些新型微小核糖核酸可被招募到RNA诱导沉默复合物(RISC)中。
产品关联:文献未提及具体实验产品,领域常规使用交联免疫沉淀结合高通量测序(CLIP-seq)技术,常用抗体包括抗DGCR8、抗Ago2等。
3.4 交联连接与测序技术验证miRNA-mRNA靶标相互作用
本环节旨在鉴定新型微小核糖核酸的靶标mRNA,明确其调控功能。实验方法上,研究团队重分析了HEK293细胞的交联连接与测序(CLASH)数据,通过识别微小核糖核酸与mRNA的嵌合序列,鉴定直接的靶标相互作用;随后用UNAFold工具分析结合能,验证结合的特异性。结果显示,87个新型微小核糖核酸候选与245个mRNA存在直接相互作用,其结合能与已知微小核糖核酸相当(P<0.001),且80%以上的相互作用存在经典的5"种子区配对;靶标mRNA富集在蛋白质生物合成、RNA结合、泛素化修饰等功能通路,部分靶标为疾病相关基因如ABL1、TP53等。
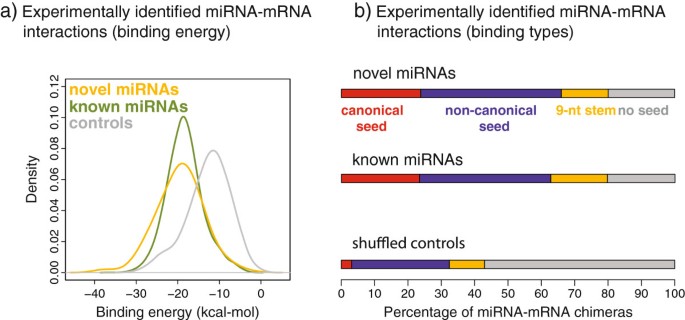
例如候选2375靶向Dicer的mRNA,形成微小核糖核酸生物发生的负调控环路;候选153来自EIF2B3的内含子,靶向蛋白质折叠相关基因;候选1331靶向核糖体60S亚基的两个基因,参与蛋白质合成通路的调控。
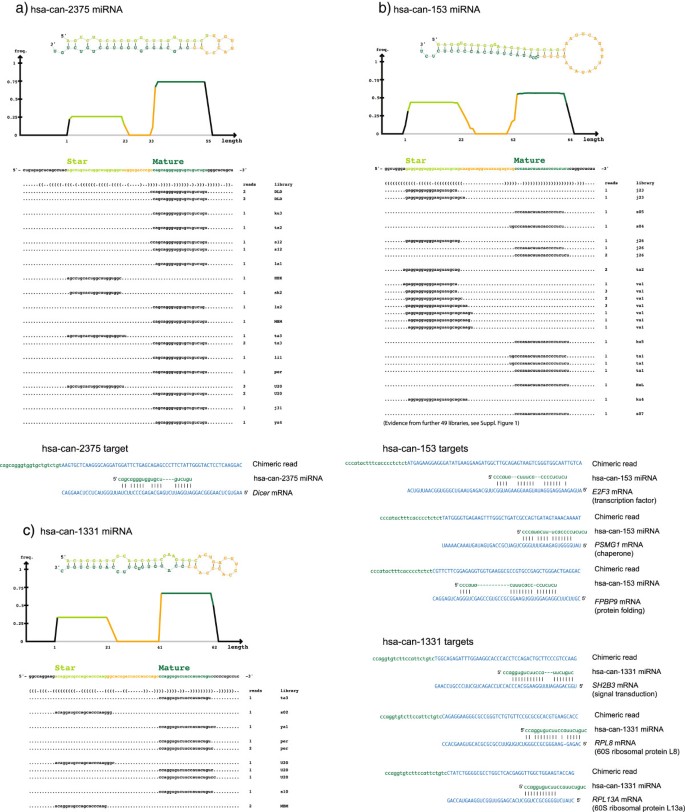
产品关联:文献未提及具体实验产品,领域常规使用CLASH技术鉴定微小核糖核酸-靶标mRNA相互作用,UNAFold用于RNA结合能分析。
3.5 定制微小核糖核酸捕获系统的开发与分化过程表达分析
本环节旨在开发低丰度微小核糖核酸的富集检测方法,并分析新型微小核糖核酸在细胞分化中的表达变化。实验方法上,研究团队与Agilent合作开发了SureSelect定制捕获系统,针对新型微小核糖核酸候选设计生物素化的捕获探针,在SH-SY5Y细胞分化前后,提取总RNA并构建小RNA测序文库,随后用捕获系统富集目标微小核糖核酸,再进行高通量测序。结果显示,该捕获系统可将新型微小核糖核酸的测序深度从平均5 reads提升至176 reads,对新型微小核糖核酸的检测灵敏度达91%,且定量准确性高(与无捕获的测序结果Pearson相关系数为0.85);在细胞分化过程中,44%的新型微小核糖核酸候选表达发生显著变化,与已知微小核糖核酸的变化比例一致,说明这些新型微小核糖核酸参与细胞分化的调控。
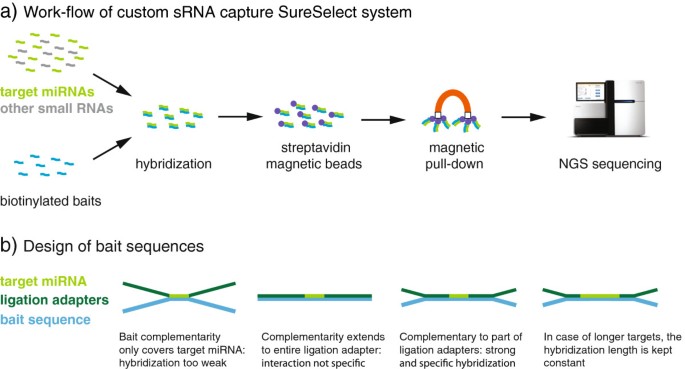
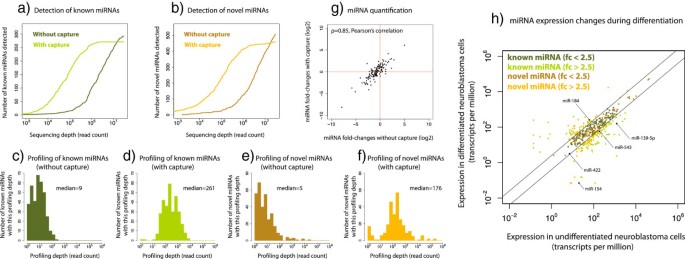
产品关联:实验所用关键产品:Agilent的SureSelect定制微小核糖核酸捕获系统,Illumina的TruSeq Small RNA Sample Preparation试剂盒用于构建测序文库。
4. Biomarker研究及发现成果解析
本研究发现的1098个新型人类微小核糖核酸可作为潜在的基因调控分子及疾病生物标志物,其筛选与验证逻辑遵循“数据预测→生物发生验证→蛋白互作验证→靶标调控验证”的完整链条,确保了候选分子的可靠性。
Biomarker定位与验证逻辑
本研究中的生物标志物为1098个新型人类微小核糖核酸,属于非编码RNA类生物标志物,筛选逻辑分为五个置信水平,其中最高水平的候选同时具备双链检测证据、生物发生因子沉默后下调、与Ago/DGCR8结合、靶标相互作用验证多个层面的证据;验证逻辑从分子(生物发生途径)、细胞(蛋白结合)、功能(靶标调控)三个维度展开,确保候选分子的真实性与功能性。
研究过程详述
这些新型微小核糖核酸主要来自人类大脑等组织,通过小RNA测序、CLIP-seq、免疫沉淀等方法验证其存在与生物发生;其中281个候选在生物发生因子沉默后表达下调30%以上,87个候选的靶标相互作用被CLASH技术证实;部分候选在神经元分化过程中表达显著变化,如候选2375在分化中表达上调,靶向Dicer mRNA参与负调控。特异性方面,新型微小核糖核酸大多为组织特异性表达,仅在2-3个数据集中被检测到,丰度较低(中位数0.5转录本/百万reads),但进化上年轻,34%的候选起源于旧世界猴祖先,在人类大脑中富集。
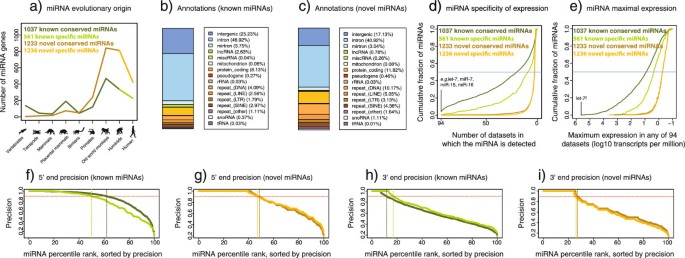
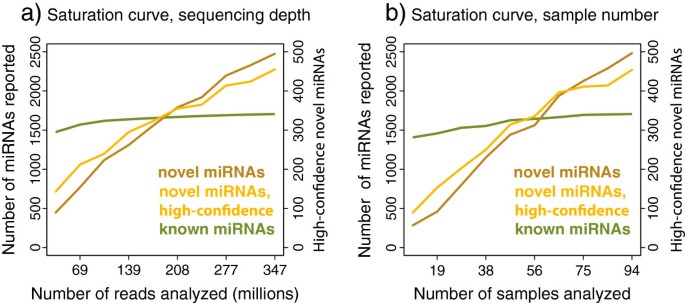
核心成果提炼
这些新型微小核糖核酸的核心功能是参与基因表达的精细调控,部分候选形成复杂的调控网络,如靶向Dicer的候选2375参与微小核糖核酸生物发生的负反馈调控,候选153、1331参与蛋白质合成通路的调控;创新性在于首次系统发现并验证了超过1000个新型人类微小核糖核酸,证明人类微小核糖核酸组的规模远大于已知数量,为后续的基因调控网络研究及疾病标志物开发提供了新的资源。统计学结果显示,1098个新型微小核糖核酸得到多层面验证,其中281个在生物发生因子沉默后下调30%以上(P<0.001),87个候选的靶标相互作用被CLASH证实(P<0.001),44%的候选在细胞分化中表达变化(文献未明确样本量,基于图表趋势推测)。此外,饱和曲线分析显示,随着测序数据量的增加,新型微小核糖核酸的发现数量呈线性增长,说明人类微小核糖核酸组尚未被完全挖掘,未来仍有大量新型微小核糖核酸待发现。