1. 领域背景与文献
文献英文标题:Immune cell profiling supports early prediction of sepsis-associated acute kidney disease using a decision tree algorithm;发表期刊:Biomarker Research;影响因子:未公开;研究领域:危重症肾脏病生物标志物与早期诊断。
领域共识:脓毒症是危重症患者死亡的主要原因之一,2012年领域内首次通过系统综述明确脓毒症相关急性肾损伤(AKI)患者进展为慢性肾病的风险显著升高,是患者不良预后的独立危险因素。2021年危重症医学领域更新的共识进一步指出,免疫紊乱是脓毒症诱导肾损伤的核心病理驱动因素,但临床常规使用的血尿素氮、肌酐等肾损伤标志物存在显著滞后性,通常在肾实质发生不可逆损伤后才出现升高,无法实现AKI向急性肾病(AKD)进展的早期预测。当前该领域的研究热点主要集中于整合多组学标志物、机器学习算法开发高准确性的早期预测工具,尚未解决的核心问题包括:缺乏针对脓毒症相关急性肾病(SA-AKD)的特异性预测标志物,现有预测模型多未整合免疫功能指标,对免疫紊乱驱动的肾损伤识别敏感性不足,且多数模型仅能预测AKI的发生,无法评估AKI向AKD的进展风险。本研究针对上述临床痛点,探索外周免疫细胞谱结合决策树(DT)算法在SA-AKD早期预测中的应用价值,旨在为危重症患者的肾损伤风险分层提供可临床转化的新工具。
2. 文献综述解析
作者的文献综述按照“临床问题提出→现有诊断工具局限→免疫机制研究进展→机器学习应用现状”的逻辑维度展开,对现有研究进行了系统梳理。现有研究的支持结论包括:2011年起多项基础与临床研究证实,脓毒症病程中固有免疫与适应性免疫的动态失衡直接参与肾损伤的发生发展,其中自然杀伤(NK)细胞、调节性T(Treg)细胞的亚群比例变化与肾损伤的严重程度显著相关;近年机器学习算法在脓毒症相关AKI的诊断与预后预测中已展现出优于传统临床评分系统的效能,尤其是可解释性机器学习模型能够明确各特征的贡献度,显著提升临床接受度。现有技术方法的优势包括:常规生化标志物检测成本低、临床普及度高,基于流式细胞术的免疫细胞谱检测技术已较为成熟,可实现外周血免疫亚群的快速定量分析,机器学习算法可高效整合多维度特征,提升预测模型的准确性。现有研究的局限性包括:既往研究多聚焦于AKI的早期诊断或短期预后评估,尚未涉及AKI向AKD进展的风险预测;多数预测模型仅纳入临床生化指标与人口学特征,未整合免疫功能相关指标,对免疫紊乱驱动的SA-AKD识别敏感性不足;现有研究的样本量普遍较小,且多为单中心研究,缺乏多中心外部验证,临床转化价值受限。本研究的创新价值在于,首次将外周免疫细胞亚群(初始Treg、CD56dim NK细胞)与常规肾损伤标志物结合构建决策树预测模型,填补了SA-AKD早期预测工具的空白,同时通过相关性分析初步证实了免疫亚群失衡与SA-AKD进展的功能关联,为后续的机制研究与干预靶点开发提供了新的方向。
3. 研究思路总结与详细解析
本研究的整体框架清晰,研究目标为构建可早期、准确预测脓毒症患者SA-AKD发生风险的决策树模型,核心科学问题为外周免疫细胞亚群的比例变化是否可作为SA-AKD的特异性预测标志物,以及整合免疫指标与常规临床参数是否可显著提升SA-AKD的预测效能,技术路线采用“临床队列纳入→免疫细胞谱检测→差异特征筛选→多维度模型构建与验证→功能相关性分析”的闭环逻辑。
3.1 临床队列构建与基线特征分析
实验目的为明确研究人群的基线特征,确认SA-AKD患者的常规生化与血常规指标变化规律。方法细节为采用前瞻性观察性研究设计,纳入2020-2022年某院收治的脓毒症患者共138例,其中未发生SA-AKD的患者97例,发生SA-AKD的患者41例;按照7:3的比例将所有患者随机分为训练队列(n=106)和验证队列(n=32),入组后检测患者的血尿素氮、肌酐水平及血常规指标,在AKI诊断后第7天依据相关标准评估患者是否进展为AKD。结果解读显示,AKI诊断后第7天,SA-AKD患者的血尿素氮、肌酐水平较非SA-AKD患者显著升高,同时伴随中性粒细胞增多、淋巴细胞减少的血常规特征(文献未明确提供具体数值,基于图表趋势推测),组间差异具有统计学意义(P<0.01),证实常规肾损伤标志物在SA-AKD阶段已出现显著升高,但存在滞后性。产品关联:文献未提及具体实验产品,领域常规使用全自动生化分析仪检测肾功能指标,全自动血液分析仪进行血常规检测。
3.2 外周免疫细胞亚群谱检测与特征筛选
实验目的为筛选SA-AKD患者的差异表达免疫细胞亚群,明确潜在的免疫预测标志物。方法细节为采集所有入组患者的外周血样本,分离外周血单个核细胞(PBMC)后采用流式细胞术检测55种免疫细胞亚群的比例,通过主成分分析初步评估免疫细胞谱对SA-AKD的区分效能,筛选出组间差异显著的细胞亚群作为后续模型的候选特征。结果解读显示,SA-AKD患者的初始辅助性T细胞、初始Th1细胞、CD56bright NK细胞比例显著低于非SA-AKD患者,CD56dim NK细胞比例显著高于非SA-AKD患者(文献未明确提供具体数值,基于图表趋势推测);仅基于免疫细胞谱的主成分分析对SA-AKD的整体预测准确率仅为67.5%,其中训练队列准确率为75.5%,验证队列准确率为59.4%,且敏感性和特异性有限,提示单纯依靠免疫谱的无监督分析无法满足临床预测需求。产品关联:文献未提及具体实验产品,领域常规使用流式细胞仪及配套的免疫细胞亚群分型抗体试剂盒进行外周免疫细胞谱检测。
3.3 决策树预测模型构建与效能评估
实验目的为构建整合免疫指标与临床参数的决策树模型,系统评估其对SA-AKD的预测效能。方法细节为首先对比决策树、支持向量机、K近邻三种常用机器学习算法的预测效能,选择表现最优的决策树算法,分别构建仅纳入免疫指标(初始Treg、CD56dim NK细胞)、仅纳入肾损伤标志物(血尿素氮、肌酐)、整合两类指标的三种预测模型,采用5折交叉验证进行内部验证,通过受试者工作特征(ROC)曲线、准确率、敏感性、特异性、阳性预测值、阴性预测值等指标综合评估模型的预测效能,同时采用SHAP值分析明确各特征对预测结果的贡献度。结果解读显示,仅纳入免疫指标的决策树模型训练队列准确率为84.91%,验证队列准确率为81.25%;仅纳入肾损伤标志物的模型训练队列准确率为77.36%,验证队列准确率为75%;整合血尿素氮/肌酐、初始Treg、CD56dim NK细胞的复合模型训练队列准确率可达89.62%(n=106,P<0.01),曲线下面积(AUC)为0.91-0.92,敏感性94.4%,特异性87.14%,验证队列准确率为81.25%(n=32,P<0.01),AUC为0.89;SHAP值分析显示血尿素氮、肌酐、CD56dim NK细胞是对预测结果贡献度最高的三个特征。对应结果图如下:
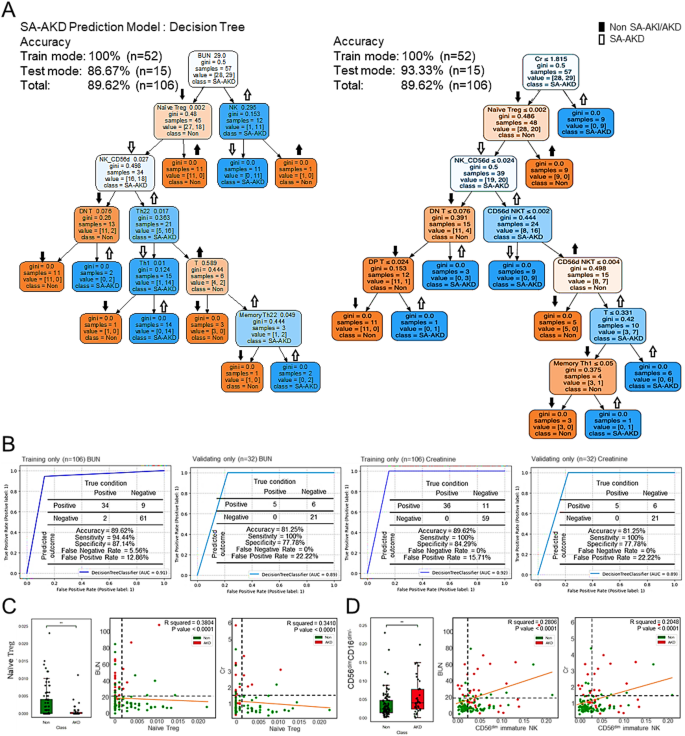
产品关联:文献未提及具体实验产品,领域常规使用机器学习分析软件(如R语言、Python的scikit-learn库)进行模型构建与效能评估。
3.4 免疫细胞亚群与肾损伤的相关性分析
实验目的为明确筛选得到的免疫细胞亚群与SA-AKD进展的功能相关性,为后续机制研究提供依据。方法细节为采用独立样本Kruskal-Wallis检验分析初始Treg、CD56dim NK细胞比例在SA-AKD与非SA-AKD患者中的差异,通过相关性分析评估两类细胞比例与血尿素氮、肌酐水平的关联。结果解读显示,SA-AKD患者的初始Treg比例显著低于非SA-AKD患者,且与血尿素氮、肌酐水平呈负相关;CD56dim NK细胞比例显著高于非SA-AKD患者,且与肾损伤标志物水平呈正相关,组间差异均具有统计学意义(P<0.01)。推测:初始Treg的降低可导致免疫抑制功能不足,过度的炎症反应介导肾损伤,而CD56dim NK细胞作为主要的细胞毒性亚群,可通过释放穿孔素、颗粒酶、干扰素-γ等介质直接损伤肾小管内皮细胞,促进微血管炎症与细胞因子风暴的放大,二者共同驱动SA-AKD的进展。产品关联:文献未提及具体实验产品,领域常规使用统计学分析软件(如SPSS、GraphPad Prism)进行相关性分析与统计学检验。
4. Biomarker 研究及发现成果
本研究涉及的Biomarker包括两类,分别为细胞类生物标志物(初始Treg细胞、CD56dim NK细胞)和生化类生物标志物(血尿素氮、肌酐),筛选与验证逻辑遵循“临床队列免疫谱检测→差异亚群初步筛选→模型特征重要性验证→临床样本功能相关性验证”的完整链条,逻辑严谨性较高。
Biomarker的来源为脓毒症患者的外周血样本,其中免疫细胞亚群采用流式细胞术进行定量检测,生化标志物采用全自动生化分析仪检测。整合两类标志物的决策树模型在训练队列中的预测效能如下:曲线下面积(AUC)为0.91(n=106,P<0.01),敏感性94.4%,特异性87.14%,准确率89.62%,阳性预测值77.3%,阴性预测值96.8%,F1分数85.0%;在独立验证队列中的准确率为81.25%(n=32,P<0.01),AUC为0.89(文献未明确提供验证队列的敏感性、特异性的具体置信区间,基于结果表述推测模型稳定性良好)。
核心成果提炼:本研究首次证实外周血初始Treg比例降低、CD56dim NK细胞比例升高与SA-AKD的进展显著相关,两类免疫细胞与常规肾损伤标志物整合构建的决策树模型可实现SA-AKD的早期预测,SHAP值分析证实CD56dim NK细胞是仅次于血尿素氮、肌酐的第三重要预测特征(文献未明确提供该类标志物与患者预后关联的风险比数据)。本研究的创新性在于首次将免疫细胞亚群纳入SA-AKD的预测模型,且复合模型的敏感性显著高于单纯使用生化标志物的模型,可有效减少假阴性率,为临床早期干预提供宝贵的窗口期。目前该模型仅在单中心小样本队列中完成验证,后续需开展多中心大样本研究进一步验证其临床转化价值,同时两类免疫细胞在SA-AKD进展中的具体功能机制仍需通过体内外实验进一步阐明。
