1. 领域背景与文献
文献英文标题:Reprogramming myeloid cells and restoring T cell fitness in checkpoint inhibitor resistant melanoma patients;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫治疗(黑色素瘤免疫检查点抑制剂耐药方向)。
领域共识:免疫检查点抑制剂(immune checkpoint inhibitor,ICI)的出现是晚期黑色素瘤治疗的里程碑,单药治疗晚期皮肤黑色素瘤的5年生存率约为35%,联合抗细胞毒性T淋巴细胞相关抗原4(cytotoxic T-lymphocyte-associated protein 4,CTLA-4)抑制剂可提升至49%,但仍有超过50%的患者会出现原发性或继发性耐药,同时联合治疗会显著提升免疫相关不良反应发生率。当前肿瘤免疫治疗领域的研究热点聚焦于通过重编程肿瘤微环境(tumor microenvironment,TME)克服免疫检查点抑制剂耐药,包括溶瘤病毒、免疫刺激基因疗法、先天性免疫通路激动剂等方向,未解决的核心问题是缺乏针对免疫检查点抑制剂难治性患者的低毒、高效临床方案,且多数候选疗法的作用机制缺乏临床多组学证据支持。
本研究针对免疫检查点抑制剂耐药黑色素瘤患者缺乏有效治疗策略的临床空白,验证表达三聚体跨膜CD40配体(trimerized membrane-bound CD40 ligand,TMZ-CD40L)和4-1BB配体(4-1BB ligand,4-1BBL)的腺病毒载体LOAd703联合抗程序性死亡配体1(programmed death ligand 1,PD-L1)单抗阿替利珠单抗的免疫重编程效应,明确该方案能否诱导免疫检查点抑制剂应答相关的免疫特征,为克服免疫检查点抑制剂耐药提供新的联合治疗范式和生物标志物参考。
2. 文献综述解析
作者的文献综述按“耐药机制现状-现有干预策略局限性-候选疗法临床前证据”的逻辑维度展开论述。现有研究的核心支持结论包括:免疫检查点抑制剂耐药可分为肿瘤固有机制(如抗原提呈通路缺陷、MHC分子表达下调)和肿瘤微环境介导的外源性机制(如免疫抑制细胞浸润、趋化因子表达沉默);CD40通路激活能有效促进树突状细胞(dendritic cell,DC)成熟、上调共刺激分子表达,4-1BB通路激活能增强CD8+T细胞和自然杀伤(natural killer,NK)细胞的增殖与效应功能,二者联用在临床前黑色素瘤模型中可显著增强免疫检查点抑制剂的抗肿瘤活性;瘤内注射溶瘤病毒介导的免疫刺激基因递送可规避全身给药的毒性问题,同时诱导局部抗肿瘤免疫应答和远端抗肿瘤效应。现有技术的优势包括:CD40激动剂联合抗程序性死亡蛋白1(programmed death 1,PD-1)单抗在免疫检查点抑制剂耐药黑色素瘤中已显示出初步临床活性,溶瘤病毒瘤内给药可降低循环中和抗体对载体的清除作用,提升局部转染效率。现有研究的局限性包括:全身给予CD40激动剂的免疫相关不良反应发生率较高,限制了临床应用;多数重编程肿瘤微环境的策略仅在临床前模型中验证了活性,缺乏免疫检查点抑制剂难治性患者的临床生物标志物数据;现有研究未明确治疗诱导的免疫特征与患者预后的关联,无法指导优势人群筛选。
本研究的创新价值在于首次在免疫检查点抑制剂难治性黑色素瘤患者中开展LOAd703联合阿替利珠单抗的多组学生物标志物分析,从肿瘤微环境转录组、血浆蛋白组、外周免疫细胞表型三个维度系统解析治疗的免疫调控效应,证实该联合方案可诱导与既往报道的免疫检查点抑制剂应答高度一致的免疫特征,为该方案的后续临床开发提供了扎实的机制证据,填补了免疫检查点抑制剂耐药人群免疫重编程疗法的临床证据空白。
3. 研究思路总结与详细解析
本研究的整体目标是明确LOAd703联合阿替利珠单抗对免疫检查点抑制剂耐药黑色素瘤患者的免疫重编程作用,核心科学问题为该联合方案能否通过调控髓系细胞和T细胞功能恢复免疫检查点抑制剂敏感性,技术路线遵循“假设提出-临床研究-多组学检测-数据分析-结论验证”的闭环逻辑:首先基于临床前研究提出“LOAd703瘤内注射可重编程肿瘤微环境,恢复免疫检查点抑制剂应答”的核心假设,随后通过LOKON003 I/II期临床试验入组免疫检查点抑制剂耐药的晚期黑色素瘤患者,给予瘤内注射LOAd703联合静脉输注阿替利珠单抗,采集治疗前后多时间点的肿瘤活检、血浆、外周血单个核细胞(peripheral blood mononuclear cell,PBMC)样本,分别开展NanoString转录组检测、Olink蛋白组检测、流式细胞术免疫分型,通过差异分析、生存关联分析、通路富集分析解析治疗诱导的免疫变化及预后意义,最终得出联合方案可诱导免疫检查点抑制剂应答相关免疫特征的结论。
3.1 临床研究设计与样本采集
本环节的核心目标是入组符合免疫检查点抑制剂耐药标准的晚期黑色素瘤患者,按方案采集多时间点样本用于后续免疫分析。实验采用多中心、单臂I/II期LOKON003临床试验(ClinicalTrials.gov注册号:NCT04123470),入组24例经抗PD-1抑制剂治疗进展的IV期皮肤黑色素瘤(23例)和黏膜黑色素瘤(1例)患者,所有患者均接受过至少1种抗PD-1抑制剂治疗,部分患者合并接受过抗CTLA-4抑制剂或其他试验性免疫治疗。给药方案为:LOAd703以1×10^11或5×10^11病毒颗粒的剂量超声引导下瘤内注射,阿替利珠单抗1200mg静脉输注,每3周1次,最多完成12次联合治疗周期,后续可接受最多7次阿替利珠单抗单药治疗。分别在治疗前、治疗后9周(采集外周血单个核细胞、血浆、肿瘤活检)、18周(采集血浆)、27周(采集肿瘤活检)收集临床样本。
结果显示共完成24例患者入组,所有样本均按方案采集,其中5例外周血单个核细胞样本因细胞质量差未纳入流式分析,1例患者因蛋白检测质量差被排除出蛋白组分析,最终15例配对肿瘤活检样本、17例配对血浆样本、14例配对外周血单个核细胞样本纳入最终分析。实验所用关键产品:纳斯特林(NanoString)的nCounter®泛癌免疫分析Panel、欧林克(Olink)的Target 96免疫肿瘤/肿瘤学II蛋白组Panel、碧迪(BD)的BD Canto II流式细胞仪、凯杰(QIAGEN)的RNeasy Mini试剂盒;其余试剂未明确提及,领域常规使用腺病毒载体制剂、抗PD-L1单抗类药物。
3.2 肿瘤微环境免疫相关基因表达分析
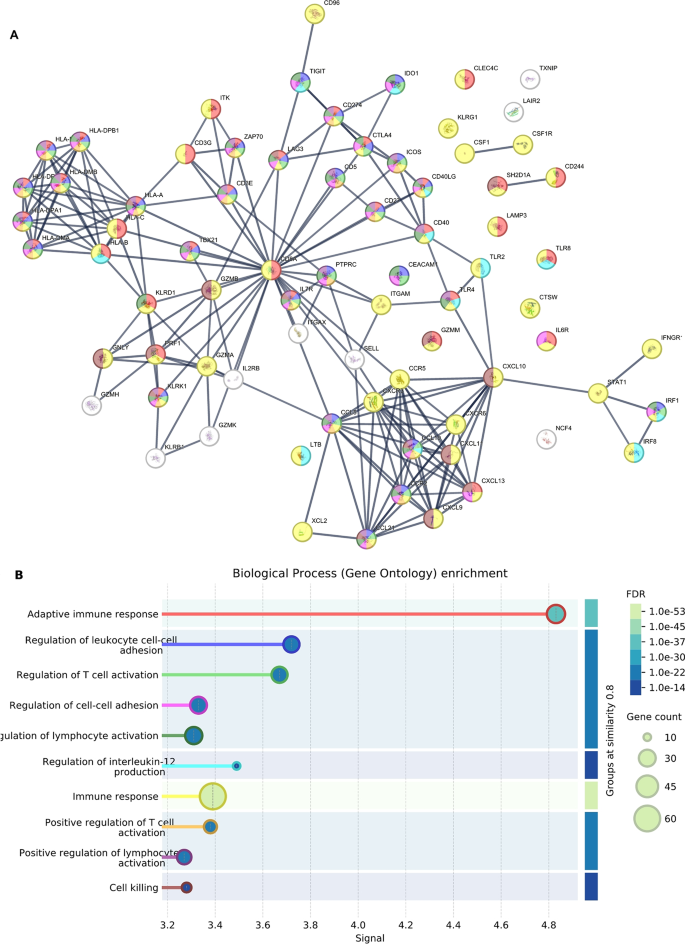
本环节的核心目标是明确联合治疗对肿瘤微环境免疫基因表达的调控效应。实验采用纳斯特林(NanoString)技术检测治疗前、治疗后9周、27周肿瘤活检样本中770个免疫和肿瘤相关基因的表达,提取156个免疫细胞相关基因进行差异分析,采用Benjamini Hochberg法校正多重检验,计算调和平均P值(harmonic mean p-value,HMP)评估基因集的整体变化,同时开展通路富集分析和K-means聚类分析。
结果显示,治疗后9周和27周,肿瘤微环境中树突状细胞相关基因集(调和平均P值分别为0.00025、0.0015,n=15,P<0.001)、抗原提呈相关基因集(调和平均P值分别为0.00031、0.0025,n=15,P<0.001)、三级淋巴结构(tertiary lymphoid structure,TLS)相关基因集(调和平均P值分别为0.0023、0.0024,n=15,P<0.01)、T细胞募集/记忆/效应相关基因集、自然杀伤细胞相关基因集均显著上调;同时肿瘤相关巨噬细胞(tumor-associated macrophage,TAM)和髓系来源抑制细胞(myeloid-derived suppressor cell,MDSC)相关基因集也显著上调(调和平均P值分别为0.00027、0.0012,n=15,P<0.001);K-means聚类显示调节性T细胞(regulatory T cell,Treg)相关基因上调幅度低的患者总生存期(overall survival,OS)更长(P<0.05,Log-rank检验)。对应结果图为转录组差异基因热图、火山图、生存曲线:
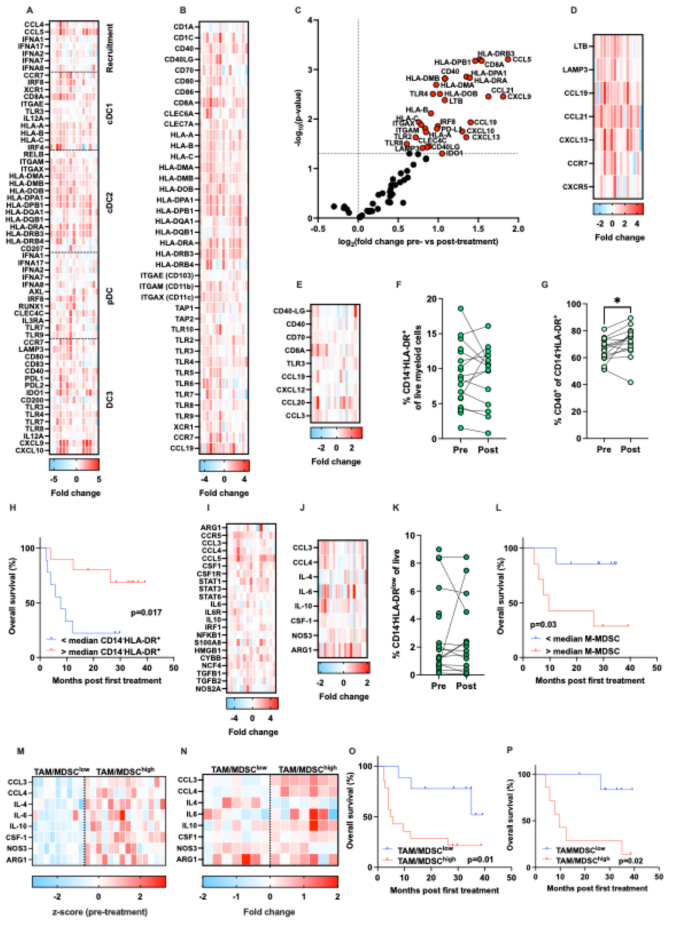
实验所用关键产品:纳斯特林(NanoString)的nCounter®泛癌免疫分析Panel、凯杰(QIAGEN)的RNeasy Mini试剂盒;文献未提及其他具体产品,领域常规使用转录组数据分析相关软件(R、Jamovi等)。
3.3 血浆免疫相关蛋白表达分析
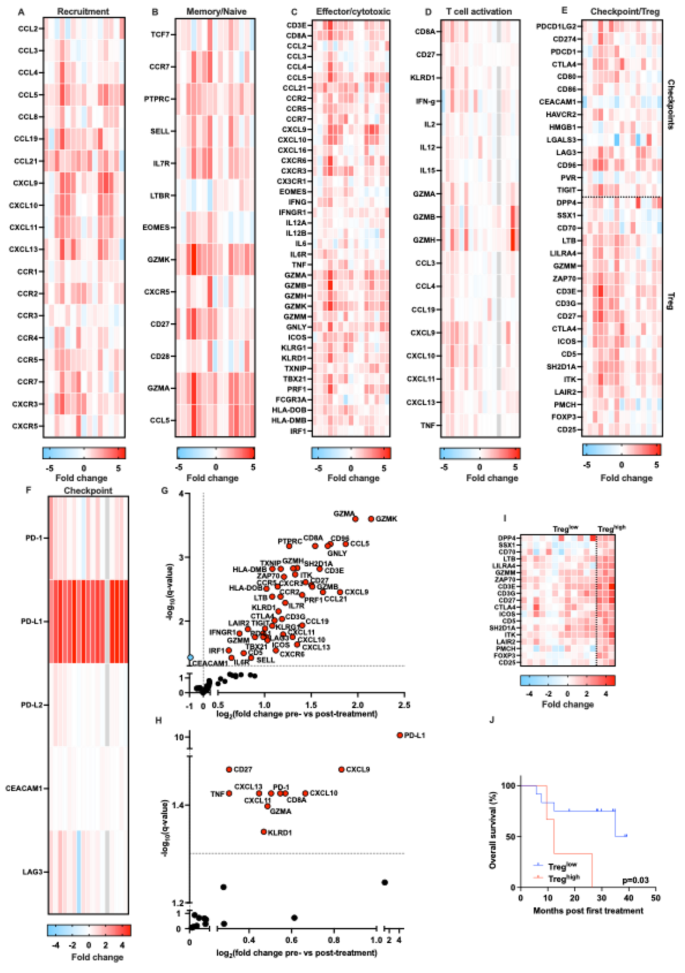
本环节的核心目标是明确联合治疗对血浆免疫相关蛋白的调控效应,探索系统性免疫变化的体液标志物。实验采用欧林克(Olink)的Target 96免疫肿瘤和肿瘤学II蛋白组Panel,检测治疗前、治疗后9周、18周血浆样本中172个免疫和肿瘤相关蛋白的表达,数据以log2标准化蛋白表达(normalized protein expression,NPX)表示,采用Benjamini Hochberg法校正多重检验,错误发现率(false discovery rate,FDR)<5%定义为显著差异。
结果显示,治疗后9周,血浆中T细胞相关蛋白、自然杀伤细胞相关蛋白、PD-1/PD-L1等免疫检查点蛋白显著上调(调和平均P值分别为0.016、9.2×10^-13,n=17,P<0.05),树突状细胞相关蛋白无显著变化,精氨酸酶1(ARG1,髓系来源抑制细胞相关蛋白)显著上调(q=0.047,n=16,P<0.05),18周时精氨酸酶1水平恢复至基线;K-means聚类显示基线肿瘤相关巨噬细胞/髓系来源抑制细胞相关蛋白水平低的患者总生存期更长(P<0.05,Log-rank检验)。
实验所用关键产品:欧林克(Olink)的Target 96免疫肿瘤/肿瘤学II蛋白组Panel;文献未提及其他具体产品,领域常规使用血浆蛋白提取和检测相关试剂。
3.4 外周血免疫细胞表型分析
本环节的核心目标是明确联合治疗对外周免疫细胞亚群的调控效应,探索系统性免疫变化的细胞标志物。实验采用流式细胞术检测治疗前、治疗后9周外周血单个核细胞样本的免疫细胞表型,使用5个荧光抗体染色组合,通过碧迪(BD)的BD Canto II流式细胞仪采集数据,采用FlowJo软件分析,分别用传统设门和Phenograph无监督聚类分析免疫细胞亚群的频率变化,采用Wilcoxon配对检验比较治疗前后的差异,Log-rank检验分析亚群频率与总生存期的关联。
结果显示,治疗后外周血中常规CD4+T细胞、调节性T细胞频率显著降低,CD8+T细胞频率显著升高,CD8+/CD4+T细胞比值、CD8+/调节性T细胞比值显著升高(P<0.05,n=14);CD8+T细胞中,初始亚群频率降低,效应记忆(effector memory,EM)亚群频率升高,PD-1表达上调(P<0.05,n=14);外周树突状细胞样细胞(CD14-HLA-DR+)的CD40表达显著升高(P<0.05,n=14);自然杀伤细胞亚群频率无显著变化,但基线CD56brightCD16-自然杀伤细胞频率高于中位数的患者总生存期更长(P<0.05,Log-rank检验);治疗后9周循环单核系髓系来源抑制细胞(CD14+HLA-DRlow)频率高于中位数的患者总生存期更短(P<0.05,Log-rank检验)。对应结果图为流式tSNE图、细胞频率变化散点图、生存曲线:
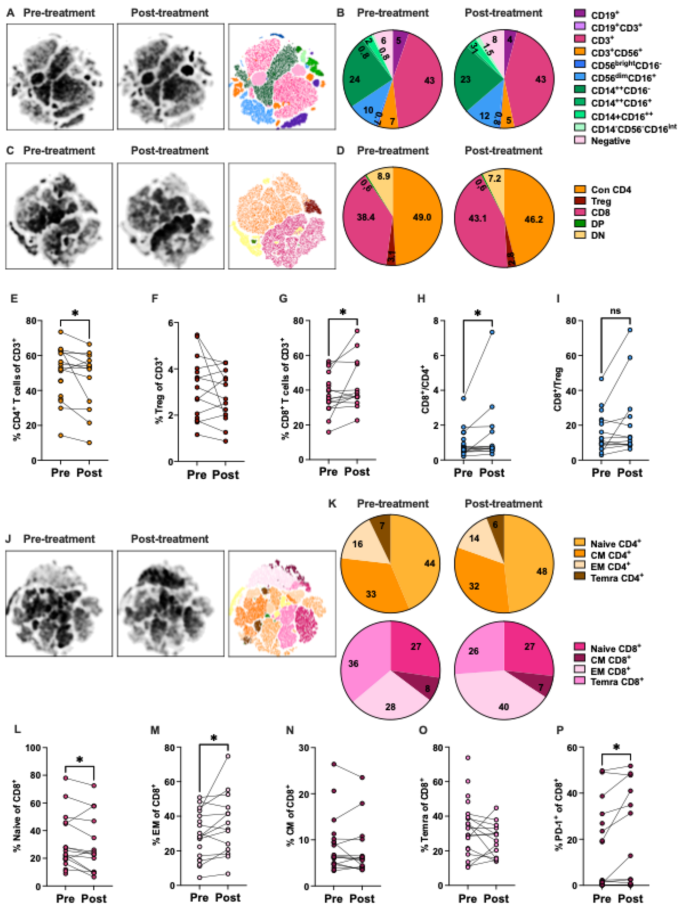
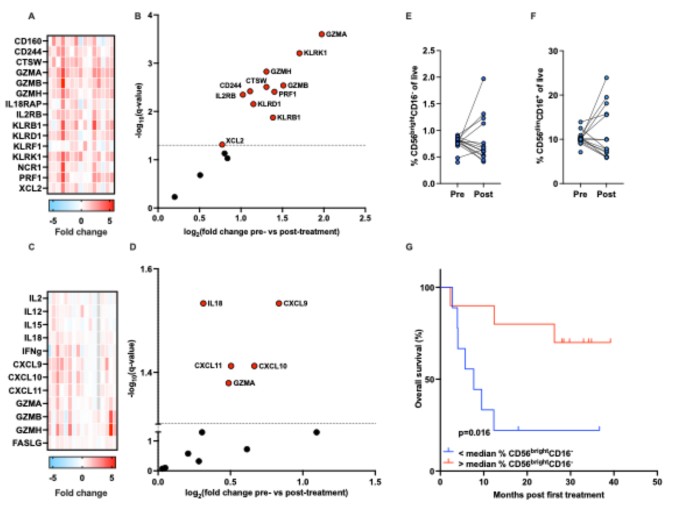
实验所用关键产品:生物传奇(Biolegend)的Live Dead Zombie Near IR染色试剂、碧迪(BD)的BD Canto II流式细胞仪;文献未提及具体抗体货号,领域常规使用流式细胞术相关抗体和试剂。
3.5 免疫特征的生存关联与通路分析
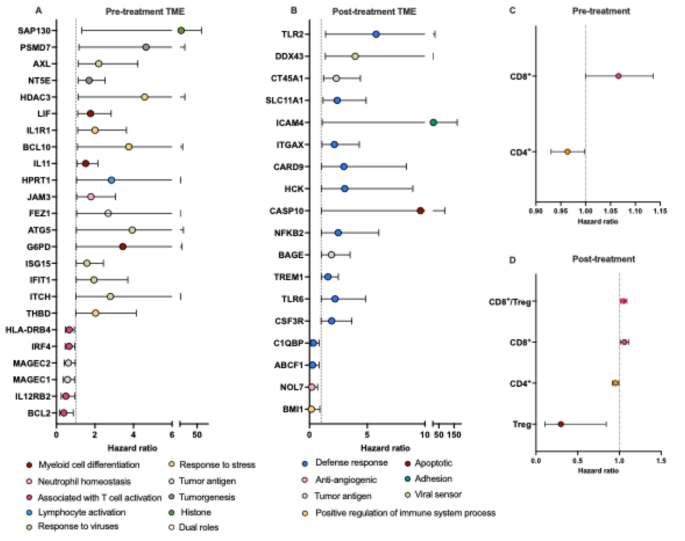
本环节的核心目标是明确治疗诱导的免疫特征与患者预后的关联,解析核心调控通路。实验采用单变量Cox回归分析肿瘤微环境基因表达、外周免疫细胞频率与总生存期的关联,采用STRING数据库进行基因本体(gene ontology,GO)富集分析和通路互作分析。
结果显示,通路分析显示CD8A是治疗诱导的免疫基因网络的核心节点,与MHC分子、细胞因子/趋化因子、T细胞活化和杀伤相关基因高度相关;基线肿瘤微环境中黑色素瘤抗原MAGE-C1/2、T细胞活化相关基因IRF4、HLA-DRB4高表达的患者总生存期更长,治疗后T细胞适应度相关基因BMI1、C1QBP高表达的患者总生存期更长;而抗病毒防御相关基因高表达的患者总生存期更短;外周血中基线CD4+T细胞、调节性T细胞频率高的患者总生存期更长,而CD8+T细胞频率高的患者总生存期更短,推测:该现象与CD8+T细胞向肿瘤微环境浸润导致外周消耗有关。对应结果图为通路互作网络、森林图:
文献未提及具体实验产品,领域常规使用生存分析软件(R、SPSS等)、通路富集分析数据库(STRING等)。
4. Biomarker 研究及发现成果
本研究涉及的生物标志物(Biomarker)分为三类,分别为肿瘤微环境转录组生物标志物、血浆蛋白生物标志物、外周免疫细胞生物标志物,筛选验证逻辑为:基于临床前研究明确的CD40/4-1BB通路免疫调控效应,从临床样本的多组学检测中筛选治疗前后差异表达的分子或细胞亚群,通过生存分析验证其预后价值,最终明确与免疫检查点抑制剂应答相关的特征性生物标志物。
生物标志物的来源覆盖三类样本:肿瘤活检组织(转录组生物标志物)、血浆(蛋白生物标志物)、外周血单个核细胞(细胞亚群生物标志物)。验证方法包括:纳斯特林(NanoString)转录组定量、欧林克(Olink)蛋白定量、流式细胞术免疫表型检测。研究未单独报告单个生物标志物的诊断敏感性和特异性,基因集层面的差异分析采用多重检验校正,错误发现率<5%;细胞亚群的组间比较采用Wilcoxon检验,P<0.05为显著差异。
核心成果提炼如下:第一,治疗诱导的树突状细胞/抗原提呈/T细胞相关基因集上调是免疫重编程的核心特征,与既往报道的免疫检查点抑制剂应答特征高度一致,证实该联合方案可有效重塑肿瘤微环境的免疫抑制状态;第二,不良预后生物标志物包括:基线肿瘤相关巨噬细胞/髓系来源抑制细胞相关蛋白水平高(风险比HR>1,P<0.05,Log-rank检验)、治疗后循环髓系来源抑制细胞频率高于中位数(HR>1,P<0.05,Log-rank检验),可用于筛选治疗不获益人群;第三,良好预后生物标志物包括:基线CD56brightCD16-自然杀伤细胞频率高于中位数(HR<1,P<0.05,Log-rank检验)、基线肿瘤MAGE-C1/2高表达(HR<1,P<0.05,Log-rank检验),可用于指导优势人群筛选;第四,治疗后调节性T细胞相关基因上调幅度低的患者总生存期更长(HR<1,P<0.05,Log-rank检验),提示调节性T细胞的抑制效应是影响治疗获益的重要因素。所有统计结果均来自14-17例配对样本的差异检验和生存分析,单个生物标志物的95%置信区间文献未明确提供,仅Cox回归分析显示上述指标与总生存期存在显著关联。
