1. 领域背景与文献
文献英文标题:Outcomes in patients with refractory/relapsed CNS lymphoma treated in complete remission: autologous transplantation vs. CAR-T therapy;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:肿瘤免疫治疗(血液肿瘤/中枢神经系统淋巴瘤方向)。
领域共识显示,复发/难治性中枢神经系统淋巴瘤(R/R CNSL)患者预后极差,未经有效巩固治疗的患者总生存期仅4-10个月。该领域的关键发展节点包括:2010年前后,大剂量化疗联合自体造血干细胞移植(ASCT)被确立为化疗敏感复发/难治性中枢神经系统淋巴瘤患者的标准巩固方案,可显著延长患者生存;2017年起,嵌合抗原受体T细胞(CAR-T)疗法逐步在B细胞来源血液肿瘤中获批应用,后续多项研究证实其对复发/难治性中枢神经系统淋巴瘤具有明确抗肿瘤活性,为无法接受自体造血干细胞移植的患者提供了新的治疗选择。当前领域研究热点聚焦于复发/难治性中枢神经系统淋巴瘤巩固治疗方案的优化、中枢浸润性肿瘤的免疫治疗耐药机制解析等,尚未解决的核心问题是:对于经挽救治疗达到完全缓解(CR)的复发/难治性中枢神经系统淋巴瘤患者,自体造血干细胞移植与嵌合抗原受体T细胞疗法作为巩固治疗的长期获益差异尚不明确,缺乏头对头比较的临床证据。本研究针对这一研究空白开展回顾性分析,旨在明确两类巩固方案的疗效差异,为临床治疗决策提供直接依据,具有重要的临床指导价值。
2. 文献综述解析
作者在文献综述部分按照治疗方案的分类维度,系统梳理了自体造血干细胞移植、嵌合抗原受体T细胞疗法两类巩固治疗的现有研究证据,明确了现有研究的优势与局限性,凸显了本研究的创新价值。
现有研究中,支持自体造血干细胞移植作为巩固治疗的证据显示,化疗敏感的复发/难治性中枢神经系统淋巴瘤患者经挽救治疗达到完全缓解后接受自体造血干细胞移植,中位无进展生存期(PFS)可达82个月,2年无病生存率最高可达93%,该方案的核心优势是清髓性预处理可深度清除中枢神经系统内的残留肿瘤细胞,长期生存获益明确;其局限性在于适用人群受限,老年、合并严重基础疾病、无法采集到足够数量造血干细胞的患者无法接受该治疗,临床中约30%-40%的完全缓解期患者因上述原因无法选择自体造血干细胞移植。针对嵌合抗原受体T细胞疗法的现有研究显示,该方案对复发/难治性中枢神经系统淋巴瘤的完全缓解率可达44%-50%,优势是无需清髓性预处理、适用人群更广,即使是老年、身体状况较差的患者也可耐受;其局限性在于缺乏完全缓解后巩固治疗的长期生存数据,且受中枢神经系统免疫微环境抑制、CAR-T细胞存续时间较短等因素影响,长期复发风险尚不明确。通过对比现有研究的未解决问题可以发现,目前尚无研究头对头比较完全缓解期复发/难治性中枢神经系统淋巴瘤患者接受两类巩固治疗的疗效差异,本研究首次填补了这一研究空白,为该人群的治疗选择提供了最高等级的真实世界证据。
3. 研究思路总结与详细解析
本研究的核心目标是对比完全缓解期复发/难治性中枢神经系统淋巴瘤患者接受自体造血干细胞移植或嵌合抗原受体T细胞疗法作为巩固治疗的疗效差异,核心科学问题是两类巩固方案对患者无进展生存期、总生存期(OS)及复发风险的影响是否存在统计学差异,技术路线采用“回顾性队列构建→基线特征均衡性评估→生存结局比较→亚组分析验证→多因素校正混杂→安全性与动力学评估”的闭环逻辑,研究结果可靠性较高。
3.1 研究队列构建与基线评估
该环节的核心实验目的是筛选符合入组标准的完全缓解期复发/难治性中枢神经系统淋巴瘤患者,确保两组患者的基线特征均衡可比,排除混杂因素对疗效结果的干扰。方法细节:研究纳入2021-2024年于北京高博医院淋巴瘤科接受治疗的患者,入组标准包括经病理确诊为复发/难治性中枢神经系统淋巴瘤,经至少2线二线挽救治疗后达到完全缓解,完全缓解状态经治疗前14天内的磁共振成像(MRI)或正电子发射计算机断层显像(PET/CT)确认,符合国际原发性中枢神经系统淋巴瘤协作组反应标准及Lugano标准;嵌合抗原受体T细胞治疗组排除既往接受过自体造血干细胞移植的患者,所有患者均未接受桥接治疗,巩固治疗前均处于持续完全缓解状态;基线特征统计采用描述性分析,分类变量采用卡方检验或Fisher精确检验比较组间差异,连续变量采用Wilcoxon秩和检验比较组间差异。结果解读:本研究共纳入60例患者,其中42例为原发性中枢神经系统淋巴瘤,18例为继发中枢受累的弥漫大B细胞淋巴瘤;33例患者接受自体造血干细胞移植,27例患者接受嵌合抗原受体T细胞治疗;基线数据显示,自体造血干细胞移植组中位年龄为53岁,嵌合抗原受体T细胞组中位年龄为65岁(n=60,P=0.001),其余基线特征包括性别比例、病理类型分布、高危患者占比、中枢神经系统受累部位、难治性患者占比、既往治疗线数、基线基因突变特征(Tp53、MYD88/CD79b突变率)均无统计学差异,两组具有可比性。对应入组流程图如下:
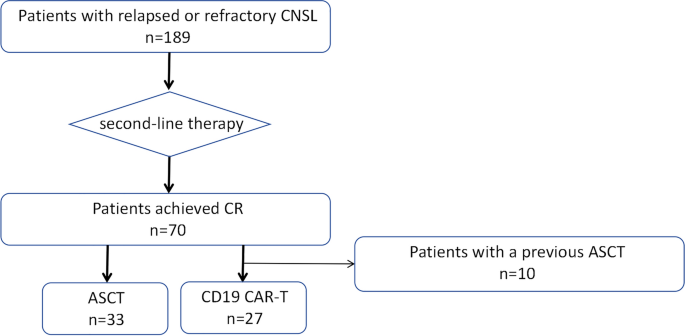
实验所用关键产品:文献未提及具体实验产品,领域常规使用造血干细胞采集试剂、基因突变检测试剂盒、影像学对比剂等相关试剂与仪器。
3.2 治疗方案实施
该环节的核心实验目的是规范实施两类巩固治疗方案,确保干预措施的一致性,避免治疗操作差异影响疗效结果。方法细节:自体造血干细胞移植组采用标准自体移植流程,化疗敏感患者接受粒细胞集落刺激因子动员自体造血干细胞,采集后冷冻保存,预处理方案以TEAM、BEAM方案为主,若患者既往治疗阶段存在预处理相关药物耐药,由临床医生根据患者情况个体化调整预处理方案;嵌合抗原受体T细胞治疗组患者均入组“靶向B细胞不同抗原的CAR-T细胞治疗复发/难治性中枢神经系统淋巴瘤(ChiCTR2200058972)”临床试验,清淋预处理采用环磷酰胺300mg/m²联合氟达拉滨30mg/m²,清淋结束后回输靶向B细胞抗原的嵌合抗原受体T细胞,输注中位剂量为1.75×10⁶细胞/kg(范围0.16×10⁶-10×10⁶细胞/kg)。结果解读:两组患者均顺利完成既定巩固治疗方案,未出现治疗相关的早期死亡事件,治疗操作的一致性符合研究设计要求。实验所用关键产品:文献未提及具体实验产品,领域常规使用粒细胞集落刺激因子、清淋化疗药物、靶向CD19的嵌合抗原受体T细胞制剂等相关药品。
3.3 生存结局与复发风险分析
该环节的核心实验目的是对比两组患者的无进展生存期、总生存期及复发累积发生率差异,明确两类巩固治疗的疗效优劣。方法细节:患者治疗后定期随访,前3个月每月随访1次,之后每3个月随访1次,随访内容包括磁共振成像、正电子发射计算机断层显像、脑脊液微小残留病检测等;采用Kaplan-Meier法绘制生存曲线,log-rank检验比较组间生存差异;采用竞争风险模型计算复发累积发生率,Gray’s检验比较组间复发风险差异,中位随访时间为12.1个月(范围1.28-59.9个月)。结果解读:总人群的3年无进展生存期率为71.5%(95%CI 51.8-82.2),3年总生存期率为87.5%(95%CI 65.2-92.5);自体造血干细胞移植组3年无进展生存期率为80.0%(95%CI 48.4-93.4),显著优于嵌合抗原受体T细胞组的64.8%(95%CI 38.9-81.9,n=60,P=0.026);自体造血干细胞移植组3年总生存期率为93.3%(95%CI 61.3-99.0),高于嵌合抗原受体T细胞组的80.1%(95%CI 49.4-93.3),但差异无统计学意义(n=60,P=0.115);自体造血干细胞移植组3年复发累积发生率为20%(95%CI 4.1-44.4),显著低于嵌合抗原受体T细胞组的30.2%(95%CI 11.0-52.2,n=60,P=0.038)。对应总人群及组间生存曲线图如下:
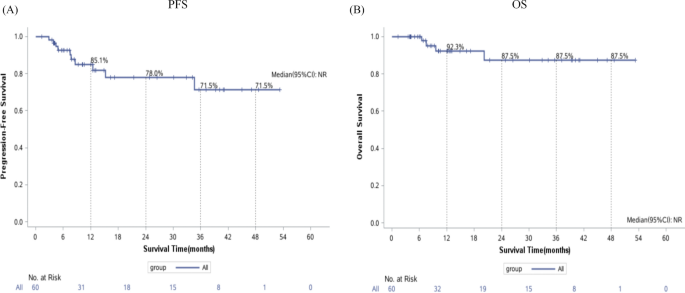
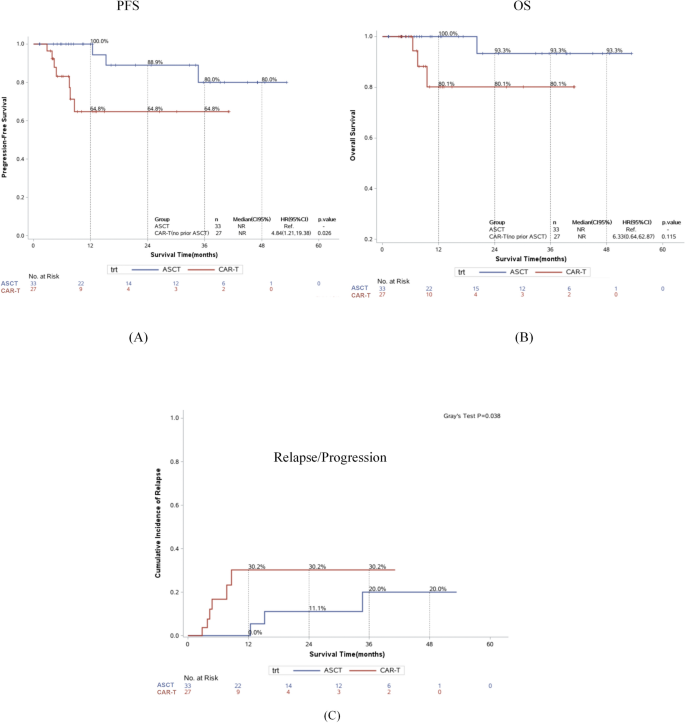
实验所用关键产品:文献未提及具体实验产品,领域常规使用生存分析统计软件、脑脊液微小残留病检测试剂等相关产品。
3.4 亚组分析与多因素校正
该环节的核心实验目的是验证不同病理亚型患者的治疗获益差异,排除混杂因素对疗效结果的影响,明确疗效差异的独立性。方法细节:按照病理类型将患者分为原发性中枢神经系统淋巴瘤亚组和继发性中枢神经系统淋巴瘤亚组,分别在亚组内进行生存分析比较;采用单因素Cox比例风险回归模型筛选无进展生存期和总生存期的潜在影响因素,将单因素分析中P<0.15的变量及临床相关变量纳入多因素Cox回归模型,校正混杂因素的影响。结果解读:原发性中枢神经系统淋巴瘤亚组共纳入42例患者,其中26例接受自体造血干细胞移植,16例接受嵌合抗原受体T细胞治疗;自体造血干细胞移植组2年无进展生存期率为92.9%(95%CI 59.1-99.9),显著优于嵌合抗原受体T细胞组的65.7%(95%CI 31.0-86.0,n=42,P=0.026);两组2年总生存期率分别为91.7%和74.1%,差异无统计学意义(n=42,P=0.101)。继发性中枢神经系统淋巴瘤亚组共纳入18例患者,其中7例接受自体造血干细胞移植,11例接受嵌合抗原受体T细胞治疗;自体造血干细胞移植组2年无进展生存期率为75%(95%CI 12.8-96.1),高于嵌合抗原受体T细胞组的64.9%(95%CI 24.9-87.4),2年总生存期率分别为100%和87.5%,但因样本量较小,差异均无统计学意义。多因素Cox回归分析显示,与自体造血干细胞移植相比,完全缓解期接受嵌合抗原受体T细胞治疗是无进展生存期不良的独立危险因素(风险比HR=5.74,95%CI 1.10-30.11,P=0.039),两类治疗方案对总生存期的影响无统计学差异(P=0.2356)。对应亚组生存曲线图如下:
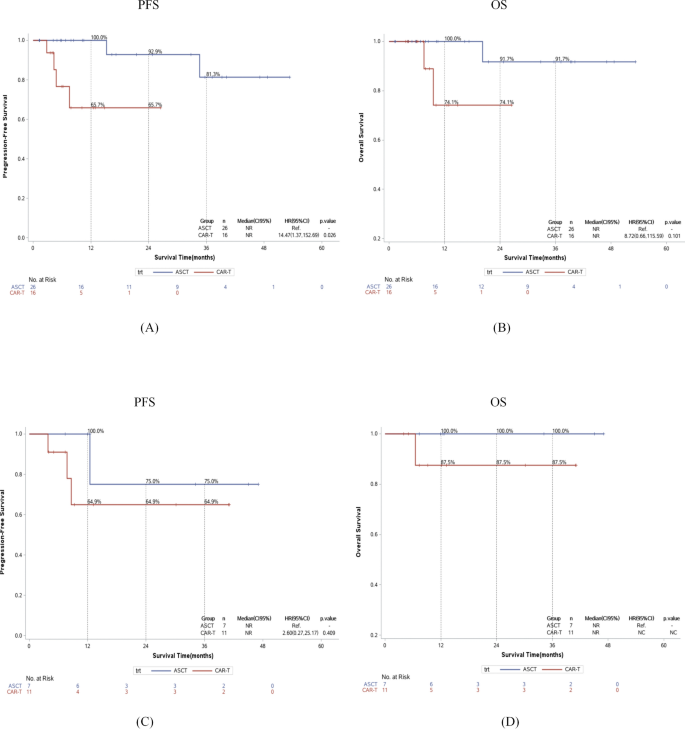
实验所用关键产品:文献未提及具体实验产品,领域常规使用统计学分析软件。
3.5 嵌合抗原受体T细胞动力学与安全性评估
该环节的核心实验目的是评估嵌合抗原受体T细胞在患者体内的扩增、中枢神经系统迁移能力,以及两类巩固治疗的安全性特征。方法细节:采用实时定量聚合酶链反应(qRT-PCR)定期检测患者外周血及脑脊液中嵌合抗原受体T细胞的慢病毒拷贝数,分析其体内动力学特征;按照国际通用标准评估细胞因子释放综合征、免疫效应细胞相关神经毒性综合征等不良反应的发生率与严重程度,记录随访期间的死亡事件及死亡原因。结果解读:36/37例可评估患者的外周血中检测到嵌合抗原受体T细胞扩增,中位峰值为7465慢病毒拷贝/μg DNA,中位达峰时间为10天(范围6-28天);10例接受脑脊液检测的患者中,4例检测到嵌合抗原受体T细胞,中位峰值为2415慢病毒拷贝/μg DNA,证实嵌合抗原受体T细胞可穿透血脑屏障进入中枢神经系统。安全性方面,所有患者中最常见的不良反应为中性粒细胞减少(发生率95%),其次为感染(发生率56.7%)、低丙种球蛋白血症(发生率46.7%);嵌合抗原受体T细胞组中6例(22.3%)发生1级细胞因子释放综合征,3例(11.1%)发生1-2级免疫效应细胞相关神经毒性综合征,经糖皮质激素、司妥昔单抗等治疗后均完全缓解,未出现严重不良反应导致的死亡。随访期间,自体造血干细胞移植组死亡率为3%(1/33),嵌合抗原受体T细胞组死亡率为18.5%(5/27),最主要的死亡原因为疾病进展(占总死亡病例的66.7%),其次为感染(占总死亡病例的33.3%)。对应嵌合抗原受体T细胞动力学图如下:
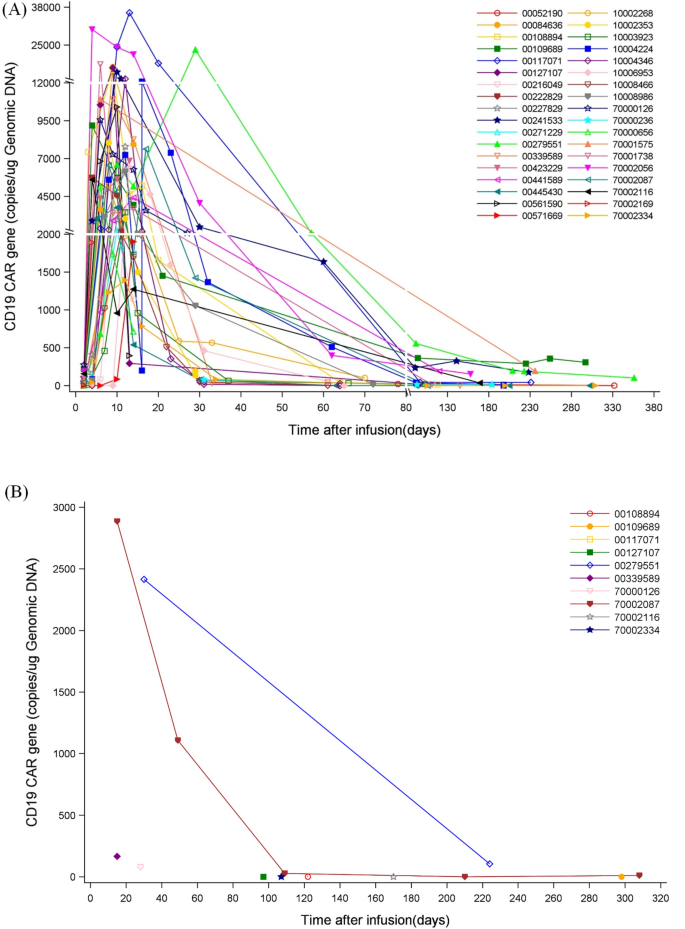
实验所用关键产品:文献未提及具体实验产品,领域常规使用实时定量聚合酶链反应检测试剂盒、细胞因子释放综合征及神经毒性评估量表、不良反应治疗药物等相关产品。
4. Biomarker 研究及发现成果
本研究未发现新的复发/难治性中枢神经系统淋巴瘤特异性生物标志物,主要探索了基线体细胞突变特征与两类巩固治疗疗效的关联,同时验证了巩固治疗方案类型对无进展生存期的独立预测价值。
本研究涉及的生物标志物为Tp53基因突变、MYD88/CD79b基因突变,属于肿瘤体细胞突变类生物标志物,筛选验证逻辑为:入组患者基线时采集肿瘤组织或外周血样本,采用下一代测序(NGS)检测体细胞突变谱,后续关联患者的治疗结局数据,分析突变特征与治疗获益的相关性。生物标志物的检测样本来源于患者基线肿瘤组织或外周血,验证方法为下一代测序技术;共35例患者完成基因突变检测,其中自体造血干细胞移植组11例,嵌合抗原受体T细胞组24例;自体造血干细胞移植组的中位突变数为7个(范围1-21),Tp53突变率为27.3%(3/11),MYD88/CD79b突变率为90.9%(10/11);嵌合抗原受体T细胞组的中位突变数为7个(范围1-38),Tp53突变率为20.8%(5/24),MYD88/CD79b突变率为66.7%(16/24)。核心成果方面,自体造血干细胞移植组中所有携带Tp53或MYD88/CD79b突变的患者均存活,仅1例Tp53突变患者、1例MYD88/CD79b突变患者出现疾病进展;嵌合抗原受体T细胞组中5例Tp53突变患者均存活,仅1例出现疾病进展,16例MYD88/CD79b突变患者中1例因疾病进展死亡、2例带瘤生存、13例维持完全缓解;因样本量较小,未发现上述基因突变与两类治疗疗效的统计学关联(文献未明确提供该数据,基于图表趋势推测)。此外,多因素分析显示,巩固治疗方案类型(自体造血干细胞移植/嵌合抗原受体T细胞疗法)是完全缓解期患者无进展生存期的独立预测因素,风险比为5.74(95%CI 1.10-30.11,P=0.039),可作为临床治疗选择的参考指标。推测:Tp53、MYD88/CD79b突变可能对两类巩固治疗的获益影响较小,后续需扩大样本量进一步验证突变特征与疗效的关联。
