1. 领域背景与文献
文献英文标题:An innovative treatment for lung cancer using gene-engineered human-induced pluripotent stem cell-derived natural killer cells;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:肿瘤免疫治疗(肺癌细胞治疗方向)。
领域共识:肺癌是全球范围内癌症相关死亡的首要原因,多数患者确诊时已处于晚期,现有治疗手段包括化疗、放疗、免疫检查点抑制剂等均存在局限性,晚期患者5年生存率不足20%。该领域发展关键节点包括:2011年免疫检查点抑制剂首次获批用于晚期肺癌,但其应答率仅约20%,且依赖患者自身功能性T细胞的存在;2017年首款嵌合抗原受体T细胞(CAR-T)疗法获批上市,在血液肿瘤中取得突破性疗效,但对异质性实体瘤的疗效有限,存在肿瘤归巢能力不足、体内持久性差、免疫抑制微环境耐受等瓶颈;2020年前后,自然杀伤细胞(NK细胞)因具有非主要组织相容性复合体限制性杀伤、无移植物抗宿主病风险、安全性更高的优势,逐渐成为实体瘤免疫治疗的研发热点,而诱导多能干细胞(iPSC)来源的自然杀伤细胞解决了原代自然杀伤细胞来源受限、规模化生产困难的问题,为“现货型”细胞治疗产品的开发提供了可能。
当前该领域的研究热点包括通过基因工程修饰增强自然杀伤细胞的肿瘤归巢能力、体内持久性、杀伤活性,以及探索自然杀伤细胞与抗体、免疫检查点抑制剂的联合治疗策略。未解决的核心问题包括:现有自然杀伤细胞修饰多为单基因或双基因改造,难以同时解决实体瘤治疗中归巢、存活、杀伤、免疫抑制微环境耐受等多重障碍;多数诱导多能干细胞来源自然杀伤细胞的肺癌疗效数据仅来自细胞系来源异种移植(CDX)模型,在更贴近临床实际的患者来源异种移植(PDX)模型中的验证数据不足,且多基因联合修饰的功能协同效应尚未得到系统验证。本研究针对上述研究空白,开发了同时携带5种功能基因修饰的诱导多能干细胞来源工程化自然杀伤细胞(eNK),系统验证其在肺癌中的治疗效果与作用机制,为晚期实体瘤的新型细胞治疗提供候选方案。
2. 文献综述解析
作者按照现有免疫治疗技术的分类维度梳理领域研究进展,分别对免疫检查点抑制剂、嵌合抗原受体T细胞治疗、自然杀伤细胞治疗三类技术的优势与局限性进行评述,在此基础上提出本研究的设计思路与创新价值。
现有研究中,免疫检查点抑制剂在非小细胞肺癌中的临床应答率仅约20%,且其疗效依赖于患者体内存在肿瘤反应性T细胞,T细胞耗竭会显著降低治疗效果,无法满足多数晚期患者的治疗需求。嵌合抗原受体T细胞疗法在血液系统恶性肿瘤中已实现治愈性效果,但针对异质性实体瘤时,存在靶点选择有限、肿瘤浸润效率低、体内持久性差、易出现细胞耗竭等问题,目前尚未在实体瘤中获得突破性进展。自然杀伤细胞治疗的现有研究优势在于:自然杀伤细胞无需抗原预激即可通过多种途径杀伤肿瘤细胞,且不会引发移植物抗宿主病,安全性优于T细胞;诱导多能干细胞来源的自然杀伤细胞可实现标准化、规模化生产,产品均一性好,具备“现货型”产品的开发潜力。现有研究的局限性包括:多数自然杀伤细胞的基因修饰仅针对单一功能模块,无法同时满足实体瘤治疗对多维度功能提升的需求;现有诱导多能干细胞来源自然杀伤细胞的肺癌疗效数据多来源于免疫缺陷小鼠的细胞系来源异种移植模型,与临床患者肿瘤的异质性差异较大,治疗效果的临床转化预测价值有限;此外,自然杀伤细胞联合EGFR抗体等靶向药物的协同效应机制尚未在肺癌模型中得到充分验证。
本研究的创新价值在于首次采用5种功能基因联合修饰的策略,同时赋予工程化自然杀伤细胞肿瘤归巢、免疫细胞招募、体内持久存活、增强肿瘤识别杀伤、提升抗体依赖细胞介导的细胞毒作用(ADCC)的多重功能,且在肺癌细胞系来源异种移植模型、原位模型及患者来源异种移植模型中系统验证了单药及联合抗体治疗的疗效,填补了多基因修饰诱导多能干细胞来源自然杀伤细胞在肺癌治疗领域的研究空白,为实体瘤的“现货型”细胞治疗提供了新的技术范式。
3. 研究思路总结与详细解析
本研究的核心目标是开发多基因修饰的诱导多能干细胞来源自然杀伤细胞,验证其在肺癌中的治疗效果与机制,为晚期实体瘤提供安全有效的新型“现货型”细胞治疗方案。核心科学问题是5种基因的联合修饰能否同时提升自然杀伤细胞的肿瘤归巢、体内持久性、杀伤活性及联合抗体的协同效应,从而突破实体瘤自然杀伤细胞治疗的现有瓶颈。技术路线遵循“分子构建→体外功能验证→体内疗效验证→联合治疗探索→安全性评估”的闭环逻辑:首先对人诱导多能干细胞进行5种功能基因的整合修饰,诱导分化为工程化自然杀伤细胞;随后通过体外细胞毒实验、3D肿瘤球杀伤实验验证其功能活性;进一步在皮下细胞系来源异种移植模型、原位肺癌模型中验证单药疗效;在患者来源异种移植模型中验证更贴近临床的治疗效果及联合抗体的协同效应;最后初步评估产品的体内安全性与药代动力学特征。
3.1 工程化自然杀伤细胞的构建与体外功能验证
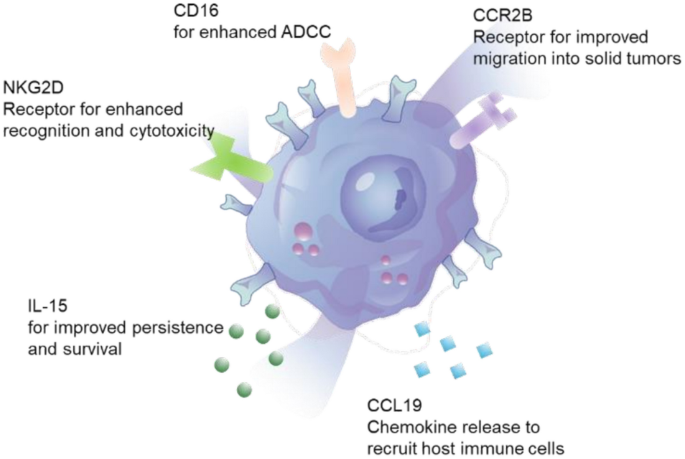
本环节核心目标是验证多基因修饰的工程化自然杀伤细胞对不同基因型肺癌细胞的杀伤活性、长效杀伤能力及抗体依赖细胞介导的细胞毒作用。方法细节为:通过基因工程技术将CC趋化因子配体19(CCL19)、CC趋化因子受体2B(CCR2B)、高亲和力分化簇16(CD16)、白细胞介素-15(IL-15)、自然杀伤细胞家族2成员D(NKG2D)-DNAX激活蛋白10(DAP10)复合物的编码基因整合至人诱导多能干细胞基因组,经诱导分化得到工程化自然杀伤细胞。体外实验选取6种不同基因型的人肺癌细胞系(A549、H1975、H460、Lu99、H520、SBC-3),采用乳酸脱氢酶(LDH)释放实验检测效靶比0.3~10范围内的细胞毒活性;采用Incucyte活细胞成像系统监测工程化自然杀伤细胞对A549、H1975细胞3D肿瘤球的长效杀伤活性,最长监测时长为120小时;在A549细胞球模型中加入西妥昔单抗或奈昔木单抗,验证高亲和力分化簇16修饰介导的抗体依赖细胞介导的细胞毒作用增强效应。工程化自然杀伤细胞的结构及修饰示意图如下:
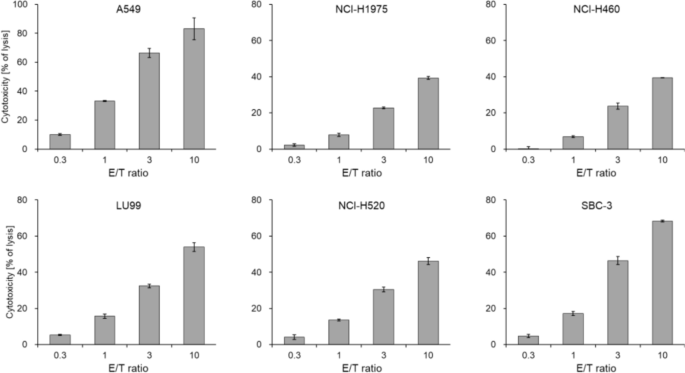
结果解读:乳酸脱氢酶释放实验结果显示,工程化自然杀伤细胞对所有受试肺癌细胞系均呈现剂量依赖性杀伤活性(图2),效靶比为10时对多数细胞系的杀伤率超过40%(文献未明确提供具体杀伤率数值,基于图表趋势推测),证实其对不同基因型肺癌细胞的广谱杀伤活性。
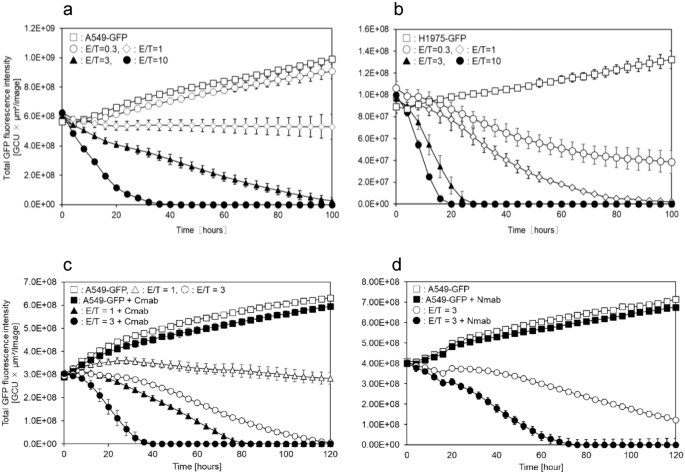
Incucyte活细胞成像结果显示,工程化自然杀伤细胞对A549细胞球在效靶比为3时即可发挥显著杀伤效应,效靶比为1时即可抑制细胞球生长;对H1975细胞球在效靶比低至0.3时即可发挥杀伤活性,且杀伤活性可持续至共培养后120小时,证实其长效杀伤能力(图3a、b)。加入西妥昔单抗或奈昔木单抗后,工程化自然杀伤细胞对A549细胞球的杀伤活性较单药提升约30%(文献未明确提供具体提升幅度,基于图表趋势推测),而两种抗体单独使用无明显杀伤效应,证实高亲和力分化簇16修饰可有效增强工程化自然杀伤细胞的抗体依赖细胞介导的细胞毒作用(图3c、d)。
产品关联:实验所用关键产品:Dojindo Molecular Technology的乳酸脱氢酶细胞毒性检测试剂盒、Sartorius的Incucyte SX5活细胞成像系统、PeproTech的干细胞因子与白细胞介素-15重组蛋白、Merck的西妥昔单抗、日本化药株式会社的奈昔木单抗。
3.2 皮下细胞系来源异种移植模型的工程化自然杀伤细胞瘤内给药疗效验证
本环节核心目标是验证瘤内注射工程化自然杀伤细胞对皮下移植肺癌的生长抑制效果,明确剂量-效应关系。方法细节为:采用NOD/Shi-scid IL-2Rγ null(NOG)小鼠皮下注射H1975-Luc荧光素酶标记细胞构建皮下肺癌细胞系来源异种移植模型,造模后14天待肿瘤稳定生长后,开始瘤内注射不同剂量的工程化自然杀伤细胞,每周给药3次,共给药2周,定期采用游标卡尺测量肿瘤长、宽、高,计算肿瘤体积,采用Dunnett多重比较检验进行统计学分析。
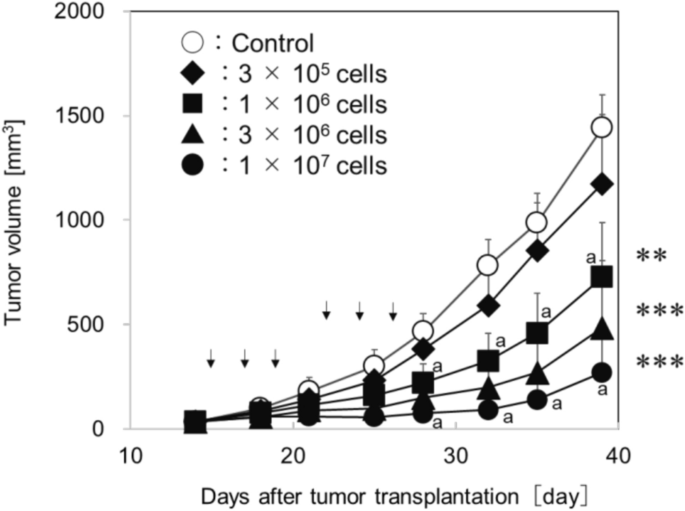
结果解读:工程化自然杀伤细胞对皮下H1975移植瘤呈现显著的剂量依赖性生长抑制效应(图4),高剂量组肿瘤体积较对照组显著降低(P<0.001,n=5),证实工程化自然杀伤细胞局部给药可有效抑制皮下肺癌的生长。
产品关联:文献未提及该环节具体实验产品,领域常规使用游标卡尺测量肿瘤体积,采用异氟烷等吸入麻醉剂进行小鼠操作。
3.3 肺癌患者来源异种移植模型的疗效与联合治疗验证
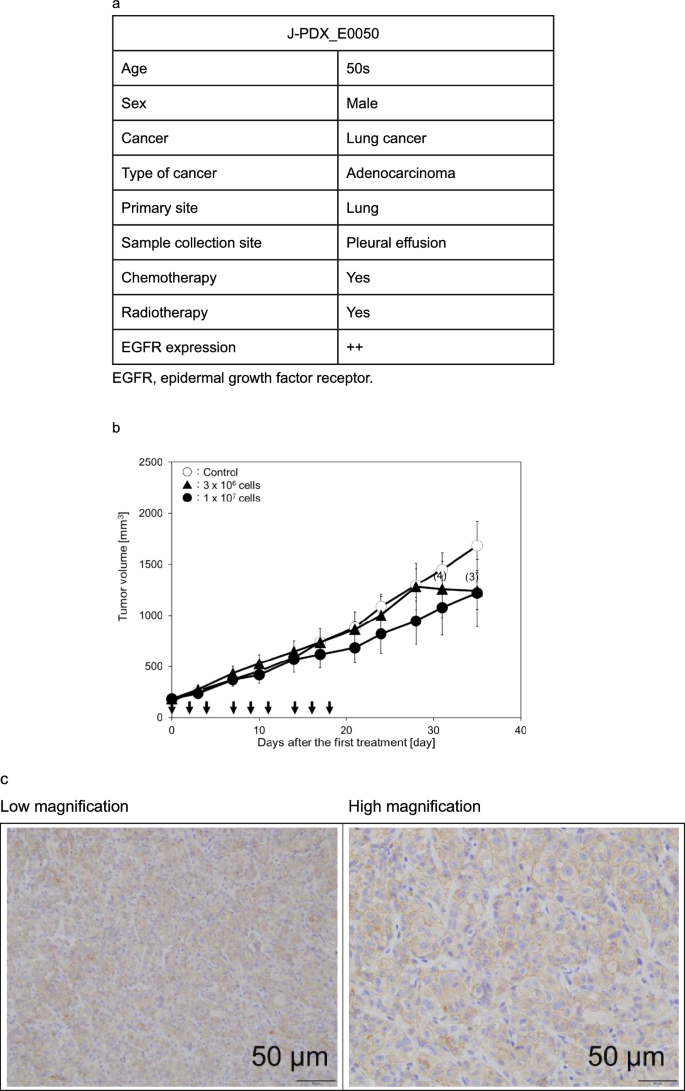
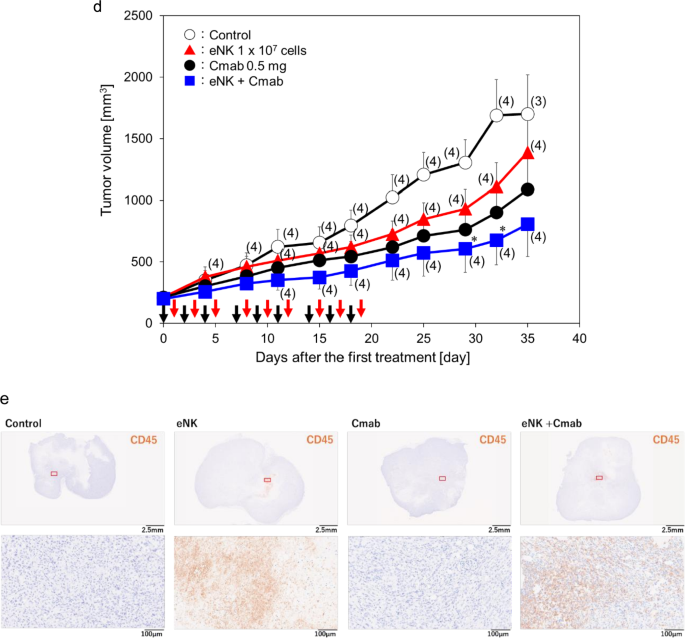
本环节核心目标是在更贴近临床患者肿瘤异质性的肺癌患者来源异种移植模型中,验证工程化自然杀伤细胞单药及联合西妥昔单抗的治疗效果,并明确工程化自然杀伤细胞的瘤内持久性。方法细节为:采用对放化疗耐药的人肺腺癌患者来源异种移植模型(J-PDX_E0050),将肿瘤组织块皮下接种至NOG小鼠,待肿瘤体积生长至约200mm³时开始给药,工程化自然杀伤细胞每周3次瘤内注射,西妥昔单抗每周3次腹腔注射,共给药3周,定期测量肿瘤体积;末次给药后16天(实验第35天)收集肿瘤组织,采用免疫组化(IHC)检测人CD45阳性细胞的瘤内浸润与存活情况。
结果解读:工程化自然杀伤细胞单药治疗的抑瘤率为28%(n=5,P<0.05),西妥昔单抗单药治疗的抑瘤率为36%(n=5,文献未明确提供该组P值),二者联合治疗的抑瘤率达53%(n=5,P<0.05),疗效显著优于单药治疗(图5b、d),证实二者具有协同抗肿瘤效应。免疫组化结果显示,工程化自然杀伤细胞单药组及联合治疗组的肿瘤实质内均可见成簇的人CD45阳性细胞(即输注的工程化自然杀伤细胞),而对照组及西妥昔单抗单药组的肿瘤组织内几乎未检测到该类细胞(图5e),证实工程化自然杀伤细胞给药后可在肿瘤微环境中长期存活至少16天,联合治疗的疗效提升与抗体依赖细胞介导的细胞毒作用增强相关。
产品关联:实验所用关键产品:Cell Signaling Technology的抗人CD45抗体(克隆号D9M81)、Hamamatsu的NanoZoomer数字切片扫描仪。
3.4 工程化自然杀伤细胞体内分布与持久性验证
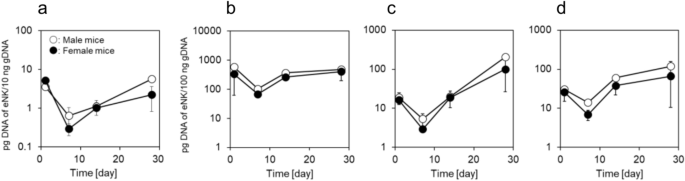
本环节核心目标是明确工程化自然杀伤细胞静脉给药后的体内分布特征与长期存活能力,为临床给药途径选择提供药代动力学依据。方法细节为:将5×10⁶个工程化自然杀伤细胞通过尾静脉注射至正常NOG小鼠,分别在给药后1、7、14、28天收集外周血、肺、肝、脾组织,提取基因组DNA,通过人特异性Alu序列定量PCR检测各组织中工程化自然杀伤细胞的含量。
结果解读:工程化自然杀伤细胞的外周血浓度在给药后1~7天有所下降,在给药后14天、28天再次回升至接近给药后24小时的水平;肺、肝、脾组织中的工程化自然杀伤细胞分布趋势与外周血一致,且工程化自然杀伤细胞在肺组织中的富集量最高(图6),提示静脉给药后工程化自然杀伤细胞优先富集于肺部,适合肺部肿瘤的治疗。推测:工程化自然杀伤细胞给药后14~28天的数量回升可能与白细胞介素-15自分泌介导的细胞存活与扩增相关,具体机制需后续实验进一步验证。
产品关联:实验所用关键产品:Qiagen的DNeasy Blood & Tissue基因组DNA提取试剂盒。
3.5 原位肺癌模型的工程化自然杀伤细胞静脉给药疗效验证
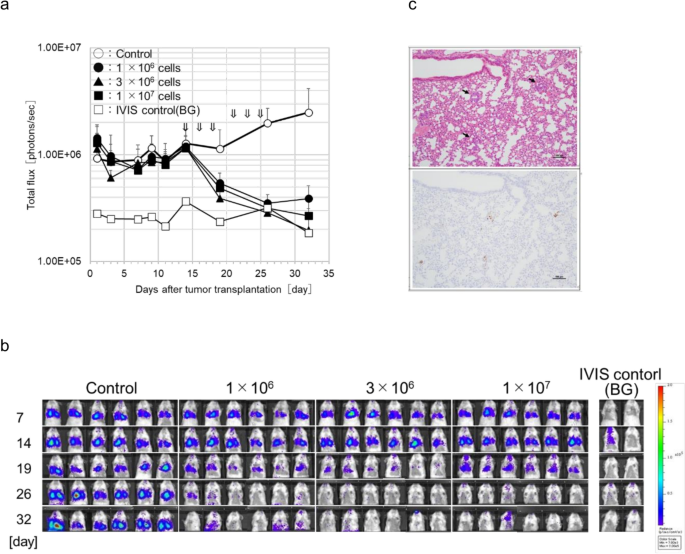
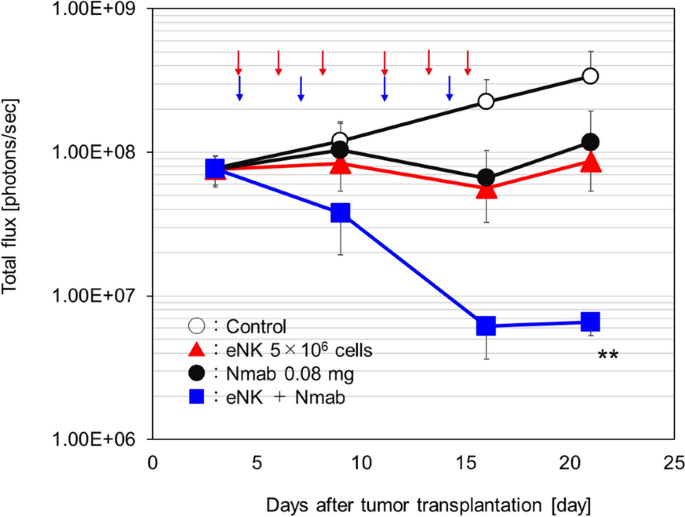
本环节核心目标是验证静脉注射工程化自然杀伤细胞对原位肺癌的治疗效果,以及联合奈昔木单抗的协同抗肿瘤效应。方法细节为:通过NOG小鼠尾静脉注射H1975-Luc或A549-Luc荧光素酶标记细胞构建原位肺癌模型。H1975原位模型造模后14天开始静脉注射不同剂量的工程化自然杀伤细胞,每周3次,共给药2周,采用IVIS生物发光成像系统监测肿瘤负荷;A549原位模型造模后4天开始给予工程化自然杀伤细胞联合奈昔木单抗治疗,工程化自然杀伤细胞每周3次静脉给药,奈昔木单抗每周2次腹腔给药,共给药2周,同样通过IVIS系统监测肿瘤负荷。造模后14天的肺组织经苏木精-伊红(H&E)染色和Ki67免疫组化染色确认肿瘤定植。
结果解读:H1975原位模型中,3×10⁶和1×10⁷剂量组的工程化自然杀伤细胞治疗可使小鼠肺部生物发光信号降至基线水平,提示肿瘤接近完全消退(图7a、b),组织学检测证实造模后14天肿瘤已成功定植于肺组织(图7c)。A549原位模型中,工程化自然杀伤细胞单药及奈昔木单抗单药均可抑制肿瘤生长,二者联合治疗的抗肿瘤效应显著优于单药治疗(P<0.01,n=5,图8),证实工程化自然杀伤细胞静脉给药对原位肺癌具有显著治疗效果,且可通过抗体依赖细胞介导的细胞毒作用与EGFR抗体发挥协同抗肿瘤效应。
产品关联:实验所用关键产品:PerkinElmer的IVIS Spectrum生物发光成像系统、Dako的抗Ki-67抗体(克隆号MIB-1)。
4. Biomarker 研究及发现成果
本研究涉及的生物标志物包括工程化自然杀伤细胞的功能相关修饰分子,以及联合治疗的伴随诊断标志物,其中工程化自然杀伤细胞表面的高亲和力分化簇16、自然杀伤细胞家族2成员D-DNAX激活蛋白10复合物、CC趋化因子受体2B,以及分泌的CC趋化因子配体19、白细胞介素-15是其功能核心标志物,肿瘤组织的EGFR表达是工程化自然杀伤细胞联合西妥昔单抗/奈昔木单抗治疗的伴随生物标志物,筛选验证逻辑为“基于实体瘤治疗瓶颈靶向选择修饰分子→体外功能验证→体内疗效与机制验证”的完整链条。
上述5种功能基因通过基因工程技术稳定整合至诱导多能干细胞基因组,在诱导分化为自然杀伤细胞后可稳定表达,其功能验证过程为:体外通过细胞毒实验验证自然杀伤细胞家族2成员D-DNAX激活蛋白10复合物介导的杀伤活性,通过趋化实验验证CC趋化因子受体2B的肿瘤归巢能力,通过抗体联合杀伤实验验证高亲和力分化簇16的抗体依赖细胞介导的细胞毒作用,通过长期培养验证白细胞介素-15的持久性维持作用;体内实验通过检测肿瘤组织人CD45阳性细胞(工程化自然杀伤细胞的细胞标志物)确认其瘤内持久性,通过人特异性Alu序列定量PCR验证其体内分布特征。该类标志物的检测特异性为100%(免疫缺陷小鼠无内源性人源分子表达),灵敏度可检测到末次给药后16天的瘤内残留工程化自然杀伤细胞;工程化自然杀伤细胞对6种不同基因型肺癌细胞系的杀伤广谱性达100%,联合西妥昔单抗后对EGFR阳性A549细胞的杀伤活性较单药提升约30%(文献未明确提供具体提升幅度,基于图表趋势推测)。
核心成果提炼:5种基因修饰的组合实现了工程化自然杀伤细胞功能的多维度提升:CC趋化因子受体2B可介导工程化自然杀伤细胞向表达CCL2的肿瘤细胞定向迁移,CC趋化因子配体19可招募患者自身免疫细胞进入肿瘤微环境,白细胞介素-15可维持工程化自然杀伤细胞的体内长期持久性,自然杀伤细胞家族2成员D-DNAX激活蛋白10复合物可增强工程化自然杀伤细胞对肿瘤细胞的识别与杀伤能力,高亲和力分化簇16可显著增强抗体依赖细胞介导的细胞毒作用。本研究的创新性在于首次将5种功能基因联合修饰应用于诱导多能干细胞来源自然杀伤细胞,在肺癌原位模型中实现接近完全的肿瘤消退,患者来源异种移植模型中单药抑瘤率为28%(n=5,P<0.05),联合西妥昔单抗的抑瘤率达53%(n=5,P<0.05)。安全性方面,小鼠长期给药后未观察到致瘤性或明显毒副反应,支持该产品的临床转化潜力。此外,工程化自然杀伤细胞静脉给药后优先富集于肺部的药代动力学特征,为肺癌的静脉给药治疗提供了重要依据。
