1. 领域背景与文献引入
文献英文标题:Metabolic reprogramming in macrophage responses;发表期刊:Biomarker Research;影响因子:未公开;研究领域:巨噬细胞代谢重编程与免疫响应。
巨噬细胞是固有免疫系统的核心效应细胞,广泛分布于组织中,通过吞噬作用、细胞因子分泌及抗原呈递参与病原体清除、炎症调控与组织修复。传统观点将巨噬细胞分为经典激活型(M1,促炎)与替代激活型(M2,抗炎),并认为其功能差异源于代谢重编程:M1依赖糖酵解(效率低但快速供能),M2依赖线粒体氧化磷酸化(OXPHOS,高效供能)。然而,近年研究揭示巨噬细胞代谢重编程的复杂性——不同来源(胚胎源性vs循环单核细胞源性)、刺激类型(TLR2 vs TLR4配体)及物种(小鼠vs人类)的巨噬细胞代谢特征存在显著差异,且代谢物(如琥珀酸、衣康酸)的非能量功能(如调控炎症信号、翻译后修饰)逐渐受到关注。
当前研究热点集中于:① 代谢通路(精氨酸、糖酵解、TCA循环、脂肪酸、谷氨酰胺)如何调控巨噬细胞表型与功能;② 肿瘤相关巨噬细胞(TAMs)的代谢异常及其促肿瘤机制;③ 代谢靶向癌症治疗的可行性。未解决的核心问题包括:不同来源/刺激的巨噬细胞代谢差异的分子机制、代谢物翻译后修饰(如琥珀酰化)的功能、TAMs代谢异质性的调控因素,以及代谢靶向治疗的特异性与毒性平衡。
本文作为综述,旨在系统总结巨噬细胞代谢重编程的最新进展,重点阐述不同表型巨噬细胞的代谢特征、TAMs的代谢异常及治疗意义,同时探讨当前研究的挑战与未来方向,为深入理解巨噬细胞“代谢-功能”关联及开发新型癌症疗法提供理论框架。
2. 文献综述解析
作者对现有研究的分类维度主要为:代谢通路(精氨酸、糖酵解、PPP、TCA、脂肪酸、谷氨酰胺)→巨噬细胞表型(M1/M2)→疾病场景(肿瘤相关巨噬细胞)。
现有研究的关键结论
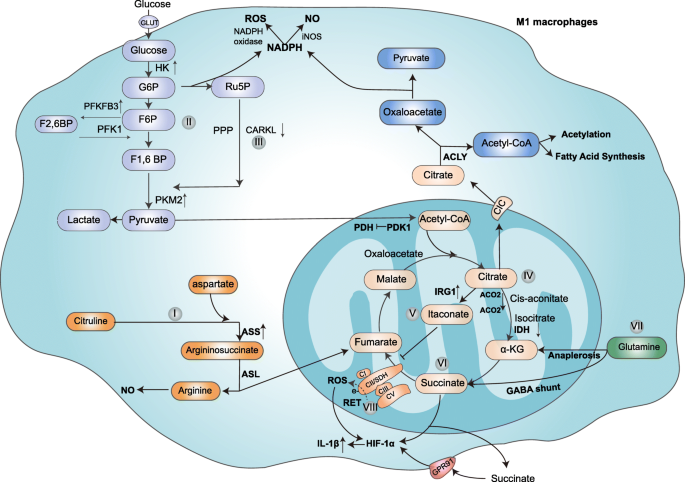
- M1型巨噬细胞:通过iNOS代谢精氨酸产生NO(促炎),糖酵解增强(HK1、PFKFB3、PKM2激活),PPP途径提供NADPH用于ROS/NO生成,TCA循环中断(柠檬酸、琥珀酸、衣康酸积累),促进IL-1β、IL-6等促炎细胞因子分泌;
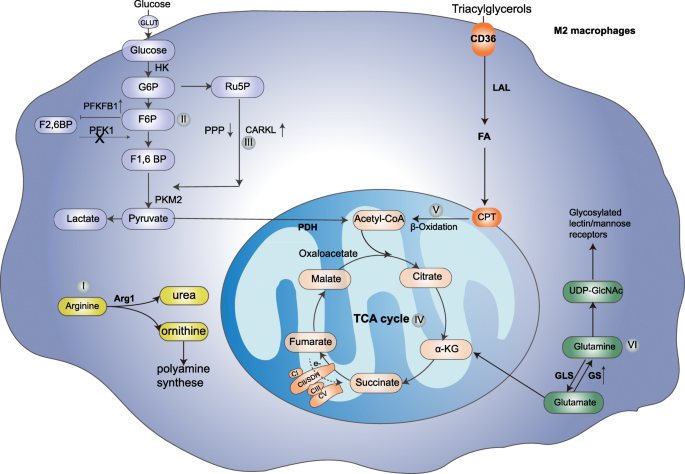
- M2型巨噬细胞:通过Arg1代谢精氨酸产生鸟氨酸(支持组织修复),依赖OXPHOS,脂肪酸氧化(CPT1A介导)与谷氨酰胺代谢增强;
- TAMs:代谢异常(糖酵解增强、脂肪酸积累),通过分泌VEGF、Arg1等促进肿瘤生长、血管生成及免疫抑制。
现有研究的优势与局限性
优势:揭示了代谢通路与巨噬细胞功能的因果关系(如糖酵解抑制剂2-DG抑制M1炎症反应);局限性:部分研究使用的代谢抑制剂(如2-DG、依托莫司)存在脱靶效应,需遗传工具(如基因敲除)验证;人类与小鼠巨噬细胞的代谢差异(如人类巨噬细胞NO生成能力弱)未明确;代谢物翻译后修饰功能(如琥珀酰化对酶活性的调控)研究不足;TAMs代谢的体内机制仍需深入探讨。
本文的创新价值
- 强调巨噬细胞代谢重编程的复杂性(来源、刺激、物种差异),而非传统的M1/M2二元分类;
- 系统整合代谢通路与巨噬细胞功能的最新研究(如衣康酸激活Nrf2的抗炎作用、琥珀酸稳定HIF-1α的促炎作用);
- 聚焦TAMs的代谢特征及治疗意义,为癌症免疫治疗提供新靶点;
- 提出当前研究的挑战(如抑制剂脱靶、代谢异质性)及未来方向(如遗传验证、代谢物修饰功能)。
3. 研究思路总结与详细解析
本文作为综述,研究思路为“概述巨噬细胞表型→分代谢通路阐述调控机制→探讨TAMs代谢→总结治疗策略→讨论挑战与未来”,具体解析如下:
3.1 巨噬细胞表型与代谢通路概述
实验目的:明确巨噬细胞表型分类及代谢重编程的核心框架。
方法细节:综合现有研究,将巨噬细胞分为M1(促炎,LPS/IFN-γ诱导)和M2(抗炎,IL-4/IL-10诱导),总结其代谢特征(M1依赖糖酵解,M2依赖OXPHOS)。
结果解读:传统代谢框架能解释部分巨噬细胞功能,但近年发现不同来源(如骨髓源性BMDMs vs腹膜巨噬细胞pMACs)、刺激(如TLR2 vs TLR4)的巨噬细胞代谢存在差异,需更细致的分类。
产品关联:文献未提及具体实验产品,领域常规使用细胞系(RAW264.7、BMDMs)、细胞因子(LPS、IFN-γ、IL-4)、代谢抑制剂(2-DG、依托莫司)等。
3.2 精氨酸代谢调控
实验目的:解析精氨酸代谢对巨噬细胞表型的影响。
方法细节:通过细胞实验(LPS/IFN-γ刺激BMDMs)、动物模型(自身免疫性脑炎小鼠)验证iNOS(M1)和Arg1(M2)的功能。
结果解读:M1通过iNOS将精氨酸转化为NO和瓜氨酸,NO抑制线粒体ETC(电子传递链),促进促炎反应;M2通过Arg1将精氨酸转化为鸟氨酸,用于多胺合成,支持组织修复。iNOS抑制剂(如氨基胍)可减轻炎症,Arg1抑制剂(如CB-1158)可阻断TAMs的免疫抑制。
产品关联:文献提到iNOS抑制剂GW274150、Arg1抑制剂CB-1158,领域常规使用iNOS抗体(检测表达)、Arg1活性试剂盒。
3.3 糖酵解与戊糖磷酸途径(PPP)
实验目的:探讨糖酵解对巨噬细胞功能的调控。
方法细节:通过细胞实验(LPS刺激RAW264.7、BMDMs)、代谢组学分析糖酵解酶(HK1、PFKFB3、PKM2)的作用。
结果解读:M1的糖酵解增强,HK1激活促进NLRP3炎症小体,PFKFB3促进糖酵解通量,PKM2与HIF-1α结合促进IL-1β分泌;糖酵解抑制剂2-DG可抑制M1的炎症反应,但高浓度(>10 mM)有脱靶效应(如抑制OXPHOS)。
产品关联:文献提到糖酵解抑制剂2-DG、PFKFB3抑制剂3PO,领域常规使用GLUT1抗体(检测葡萄糖摄取)、糖酵解通量试剂盒。
3.4 三羧酸(TCA)循环及其代谢物
实验目的:解析TCA循环中断对M1巨噬细胞的影响。
方法细节:通过代谢组学(13C标记葡萄糖/谷氨酰胺)、细胞实验(LPS刺激BMDMs)分析TCA代谢物(柠檬酸、琥珀酸、衣康酸)的功能。
结果解读:M1的TCA循环中断,柠檬酸积累促进脂肪酸合成和蛋白乙酰化,琥珀酸稳定HIF-1α促进IL-1β分泌,衣康酸激活Nrf2发挥抗炎作用(图1)。这些代谢物通过调控NF-κB、Nrf2等信号通路影响巨噬细胞功能。
产品关联:文献提到衣康酸衍生物DI、4-OI,领域常规使用TCA代谢物检测试剂盒、Nrf2抗体。
3.5 脂肪酸代谢
实验目的:探讨脂肪酸代谢对巨噬细胞极化的作用。
方法细节:通过细胞实验(IL-4刺激BMDMs)、基因敲除(Cpt1a-/-小鼠)验证脂肪酸氧化(FAO)对M2的影响。
结果解读:M2依赖FAO(CPT1A介导),抑制剂依托莫司可抑制M2极化;M1的脂肪酸合成增强(FASN激活),促进NLRP3炎症小体;TAMs通过CD36摄取脂肪酸,FAO增强促进肿瘤生长(图2)。
产品关联:文献提到FAO抑制剂依托莫司、脂肪酸合成抑制剂C646,领域常规使用CPT1A抗体、脂肪酸氧化通量试剂盒。
3.6 谷氨酰胺代谢
实验目的:解析谷氨酰胺代谢对巨噬细胞的调控。
方法细节:通过细胞实验(LPS/IL-4刺激BMDMs)、代谢组学(13C/15N标记谷氨酰胺)分析谷氨酰胺的代谢流向。
结果解读:M1通过谷氨酰胺代谢产生琥珀酸(GABA shunt途径),稳定HIF-1α;M2通过谷氨酰胺代谢补充TCA循环,产生UDP-GlcNAc促进糖基化,支持M2标志物(CD206、RELMα)表达;谷氨酰胺酶抑制剂CB-839可抑制M2极化。
产品关联:文献提到谷氨酰胺酶抑制剂CB-839,领域常规使用GLS抗体、谷氨酰胺代谢试剂盒。
3.7 肿瘤相关巨噬细胞(TAMs)的代谢特征
实验目的:探讨TAMs的代谢异常及促肿瘤机制。
方法细节:通过临床样本(乳腺癌、胶质瘤)、动物模型(肿瘤异种移植小鼠)分析TAMs的代谢特征。
结果解读:TAMs代谢异常包括糖酵解增强(HK2上调)、脂肪酸积累(CD36摄取)、谷氨酰胺代谢改变,通过分泌VEGF、Arg1促进肿瘤生长、血管生成及免疫抑制;靶向TAMs代谢(如抑制HK2、CD36)可抑制肿瘤进展。
产品关联:文献提到TAMs代谢标志物HK2、CD36,领域常规使用TAMs分离试剂盒(如CD11b+磁珠)、肿瘤异种移植模型。
3.8 代谢靶向的癌症治疗策略
实验目的:总结代谢靶向治疗的潜力与挑战。
方法细节:综合临床前研究(细胞、动物模型)和临床试验(如2-DG、DCA)结果。
结果解读:靶向代谢通路的药物(如iNOS抑制剂、糖酵解抑制剂、FAO抑制剂)在临床前模型中显示抗肿瘤活性,但需解决特异性(如正常细胞与肿瘤细胞代谢重叠)、毒性(如2-DG的脱靶效应)及异质性(如TAMs代谢异质性)问题;联合治疗(如代谢抑制剂+免疫检查点抑制剂)可能提高疗效。
产品关联:文献提到临床试验药物2-DG(NCT01386632)、DCA(NCT00540176)、CB-839(NCT03910530),领域常规使用临床样本库、临床试验设计工具。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本文涉及的Biomarker主要为代谢相关的酶或代谢物,包括:
1. M1表型标志物:iNOS(精氨酸代谢)、HK1、PFKFB3、PKM2(糖酵解);
2. M2表型标志物:Arg1(精氨酸代谢)、CPT1A(脂肪酸氧化)、GLS(谷氨酰胺代谢);
3. TAMs标志物:HK2(糖酵解)、CD36(脂肪酸摄取)。
筛选/验证逻辑:通过“细胞实验→动物模型→临床样本”的递进验证。例如,iNOS作为M1标志物,先通过LPS刺激BMDMs验证其表达上调,再通过自身免疫性脑炎小鼠模型验证其促炎功能,最后通过临床炎症样本验证其与疾病活动度的关联。
研究过程与核心成果
- iNOS(M1标志物):来源为LPS/IFN-γ刺激的BMDMs或临床炎症组织,验证方法为qRT-PCR、WB、免疫组化,特异性为M1高表达,敏感性为在LPS刺激后1-6小时内上调(n=3,P<0.05);可作为炎症活动度的Biomarker,与自身免疫病(如多发性硬化)的疾病进展相关。
- Arg1(M2标志物):来源为IL-4刺激的BMDMs或临床修复组织,验证方法为qRT-PCR、酶活性测定,特异性为M2高表达,敏感性为在IL-4刺激后24小时内上调(n=3,P<0.01);可作为组织修复的Biomarker,与伤口愈合、纤维化相关。
- HK2(TAMs标志物):来源为肿瘤提取物刺激的BMDMs或临床肿瘤组织,验证方法为WB、免疫组化,特异性为TAMs高表达,敏感性为与肿瘤大小正相关(n=50,HR=2.1,P<0.003);可作为肿瘤进展的Biomarker,与乳腺癌患者总生存期缩短相关(n=100,P<0.01)。
创新性与临床意义
本文的Biomarker研究创新在于将代谢通路与巨噬细胞表型/疾病进展关联,为疾病诊断(如炎症活动度、肿瘤分期)和治疗(如代谢靶向)提供了新型生物标志物。例如,TAMs中的HK2高表达提示患者对免疫治疗反应差,可作为筛选免疫治疗获益人群的Biomarker;Arg1高表达提示组织处于修复状态,可用于监测伤口愈合或纤维化的治疗效果。
结语
本文系统总结了巨噬细胞代谢重编程的最新进展,强调了代谢通路与巨噬细胞功能的紧密关联,为深入理解巨噬细胞在炎症、肿瘤中的作用提供了理论基础。未来研究需聚焦代谢异质性(不同来源/刺激的巨噬细胞)、代谢物翻译后修饰(如琥珀酰化)及代谢靶向治疗的特异性,以推动代谢重编程研究从基础向临床转化。
