1. 领域背景与文献引入
文献英文标题:Long-read transcriptome landscapes of primary and metastatic liver cancers at transcript resolution;发表期刊:Biomark Res;影响因子:未公开;研究领域:原发性和转移性肝癌的转录组学研究。
肝癌是人类第六大常见原发性癌症,也是结直肠癌、乳腺癌等多种恶性肿瘤的常见转移靶器官。肝转移患者的5年生存率显著降低,但其分子机制尚未完全阐明。转录组的复杂性(如可变剪接、isoform切换)在肝癌发生发展中起关键作用,但传统短读长RNA测序(100-200 bp)无法直接解析全长转录本结构,导致对原发性与转移性肝癌的转录组差异认识不足。尽管近年长读长测序(如PacBio Iso-seq)已应用于肝癌研究,揭示了肿瘤特异性isoform和可变剪接事件,但既往研究样本量小(如仅8例HCC)、未覆盖转移性肝癌、缺乏系统的临床关联分析。因此,解析原发性与转移性肝癌的全长转录组景观,识别肿瘤/转移特异性转录本并探讨其临床价值,成为肝癌精准诊疗的关键需求。本研究通过大样本队列的长读长与短读长测序结合,首次系统刻画了原发性和转移性肝癌的转录组差异,为肝癌治疗提供了新的分子靶点与诊断标志物。
2. 文献综述解析
作者对领域现有研究的评述逻辑围绕“长读长测序的应用价值与局限”展开:
- 现有研究的关键结论:长读长测序能突破短读长的局限,识别肝癌中的新颖isoform(如AKR1C2、AKR1B10的新颖剪接体)、肿瘤特异性转录本及isoform切换事件,证实可变剪接与肝癌预后相关;
- 现有研究的局限性:①样本量小(多为单中心小队列);②未系统比较原发性与转移性肝癌的转录组差异;③未深入探讨转移特异性转录本的临床诊断价值;④对癌旁肝组织的转录组变化与免疫微环境的关联研究不足。
本研究的创新点在于:①大样本队列(95例患者,涵盖HCC、结直肠癌肝转移(CRLM)、乳腺癌肝转移(BCLM)等7种肿瘤类型);②多组学整合(结合长读长Iso-seq与短读长RNA-seq,解析全长转录本的同时实现精准定量);③临床转化导向(系统识别肿瘤/转移特异性转录本,验证其预后与诊断价值);④机制深度(从表观遗传、转录因子、转座元件多角度解析转录本调控机制)。
3. 研究思路总结与详细解析
3.1 整体研究框架
研究目标:解析原发性与转移性肝癌的全长转录组景观,识别肿瘤/转移特异性转录本及isoform切换,探讨其调控机制与临床意义。
核心科学问题:①原发性与转移性肝癌的转录组差异;②肿瘤特异性转录本(SRTs)的调控机制;③转移特异性转录本的临床诊断价值;④癌旁肝组织的转录组变化与免疫微环境的关系。
技术路线:临床样本收集→长读长Iso-seq+短读长RNA-seq→转录本鉴定与分类→差异转录本/isoform切换分析→功能富集→临床关联(预后、诊断)→机制研究(表观遗传、转录因子)。
3.2 样本收集与测序
实验目的:获取原发性与转移性肝癌的全长转录组与定量数据。
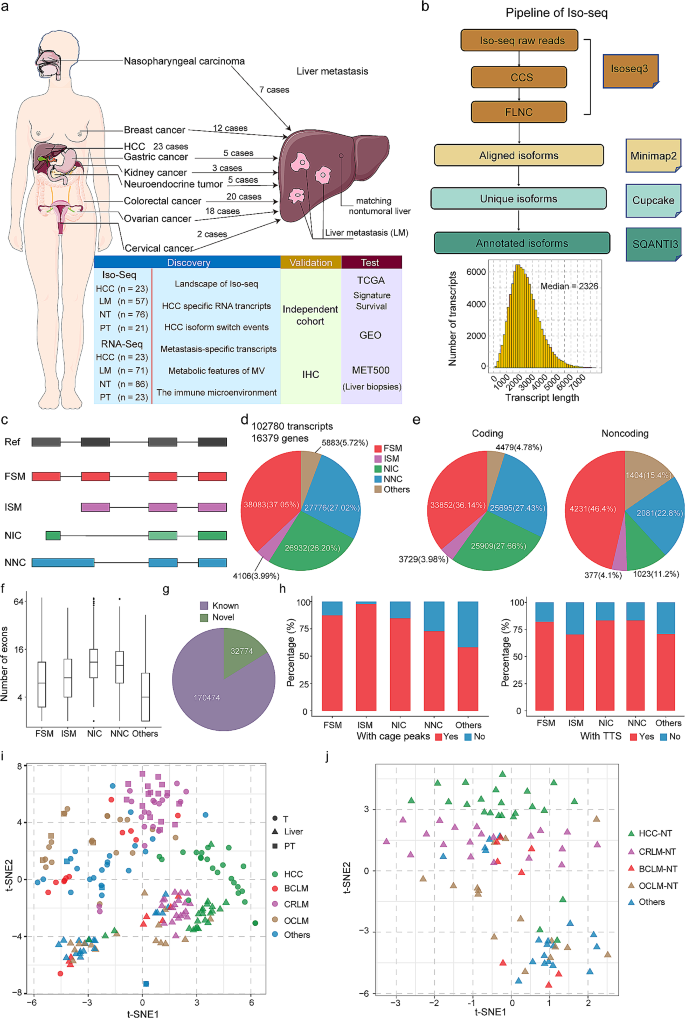
方法细节:收集95例接受肝切除的患者样本(177个组织样本,包括HCC、CRLM、BCLM等),用TRIzol试剂提取总RNA,通过Nanodrop与Agilent 2100评估RNA纯度(RIN>7)。长读长Iso-seq文库构建用Clontech SMARTer PCR cDNA Synthesis Kit(货号634925/634926)与PacBio SMRTbell Template Prep Kit(Part No. 100-259-100),测序用PacBio Sequel II系统;短读长RNA-seq文库构建用VAHTS Total RNA-seq Library Prep Kit for Illumina(Vazyme),测序用Illumina HiSeq平台。
结果解读:成功获得102,780个独特的全长转录本(覆盖16,379个基因),平均长度2.3 kb;短读长RNA-seq实现了转录本的精准定量。
产品关联:实验所用关键产品:Clontech SMARTer PCR cDNA Synthesis Kit、PacBio SMRTbell Template Prep Kit、VAHTS Total RNA-seq Library Prep Kit for Illumina。
3.3 转录本鉴定与分类
实验目的:解析转录本的结构特征与注释状态。
方法细节:用ToFU pipeline处理Iso-seq数据获得全长非嵌合(FLNC)读段,通过SQANTI3将转录本与GENCODE v.44比对,分为5类:①全剪接匹配(FSM,与已知转录本完全一致);②不完全剪接匹配(ISM,5’/3’端不完整);③新颖但有已知剪接位点(NIC);④完全新颖(NNC);⑤其他。用FANTOM5的CAGE数据验证转录起始位点(TSS),用polyA基序验证转录终止位点(TTS)。
结果解读:37.05%的转录本为FSM,3.99%为ISM,26.2%为NIC,27.02%为NNC;新颖转录本(NIC+NNC)的外显子数显著多于已知转录本(P<0.05);约32,774个剪接 junction未被GENCODE注释,提示肝癌转录组的高度复杂性。
3.4 差异转录本与isoform切换分析
实验目的:识别肿瘤与癌旁、原发性与转移性肝癌的转录组差异,解析isoform切换事件。
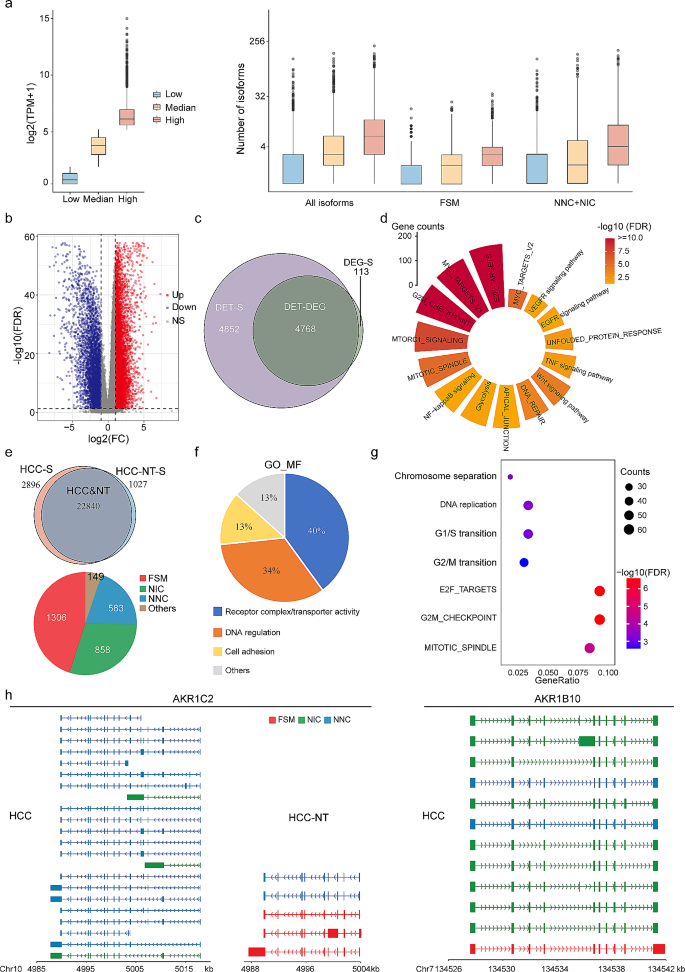
方法细节:用Wilcoxon秩和检验分析差异表达转录本(DETs),筛选标准为|log2(FC)|>1且FDR<0.05;isoform切换定义为“同一基因的一个isoform上调,另一个isoform下调”。用clusterProfiler进行KEGG与GO富集分析。
结果解读:①HCC与癌旁比较:发现26,763个DETs,其中50.4%的DETs来自基因表达无差异的基因(提示isoform水平的差异易被短读长测序遗漏);DETs富集在细胞周期、E2F靶点等肝癌相关通路。②转移性肝癌与原发灶比较:DETs富集在EMT、细胞外基质组织等转移相关通路;23个EMT基因的新颖isoform数显著增加(如ZEB1、TWIST1的NIC+NNC isoform数是参考的2.125倍)。③isoform切换:HCC中识别到1566个isoform切换事件,consensus clustering将患者分为3亚型,Cluster_S1亚型预后最差(Log-rank P<0.001),且PD-1/PD-L1表达显著升高。
3.5 肿瘤特异性转录本(SRTs)的临床与机制研究
实验目的:识别肿瘤特异性转录本,探讨其临床意义与调控机制。
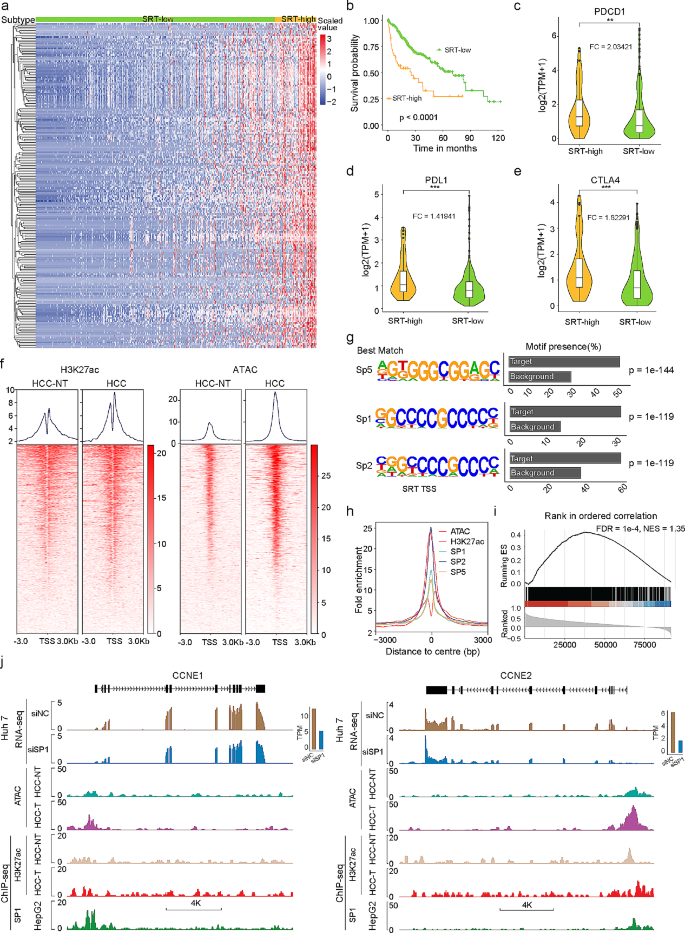
方法细节:HCC-SRTs定义为“肿瘤中表达是癌旁的10倍以上,且在>5%肿瘤样本中表达(TPM>0.5)”;用consensus clustering将TCGA HCC队列(371例)分为SRT-high与SRT-low亚型,生存分析评估预后;用ChIP-seq(H3K27ac)、ATAC-seq分析表观遗传,用MEME做Motif富集分析。
结果解读:①临床意义:SRT-high亚型患者的总生存期(OS)显著短于SRT-low亚型(Log-rank P<0.001),且PD-1/PD-L1/CTLA4表达升高(P<0.01)。②调控机制:SRTs的启动子区H3K27ac富集(提示活性增强)与chromatin accessibility增加;Sp家族转录因子(SP1、SP2、SP5)的motif显著富集,ChIP-seq证实SP1直接结合SRTs的启动子(如CCNE1、CCNE2), knockdown SP1可降低SRTs表达(P<0.01)。
3.6 转移特异性转录本的诊断价值分析
实验目的:识别转移特异性转录本,验证其诊断与组织起源预测价值。
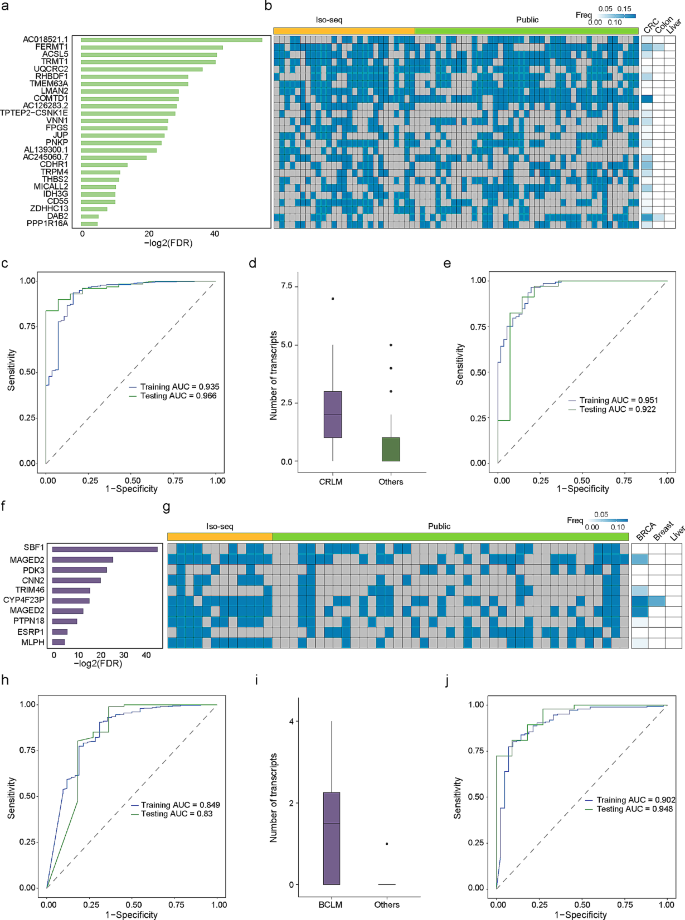
方法细节:CRLM-SRTs定义为“CRLM中表达显著高于CRC原发灶(|log2FC|>1,FDR<0.05)”,BCLM-SRTs同理;用随机森林算法构建诊断panel,ROC曲线评估准确性。
结果解读:①CRLM-SRTs:26个CRLM-SRTs组成的panel区分CRLM与CRC原发灶的AUC训练集为0.935(95% CI 0.898-0.972),测试集为0.966(95% CI 0.935-0.997);预测CRLM组织起源(结肠)的AUC训练集0.951,测试集0.922。②BCLM-SRTs:10个BCLM-SRTs组成的panel区分BCLM与乳腺癌原发灶的AUC训练集0.849,测试集0.83;预测BCLM组织起源(乳腺)的AUC训练集0.951,测试集0.922。
3.7 癌旁肝组织的转录组与免疫微环境分析
实验目的:解析癌旁肝组织的转录组变化与免疫微环境特征。
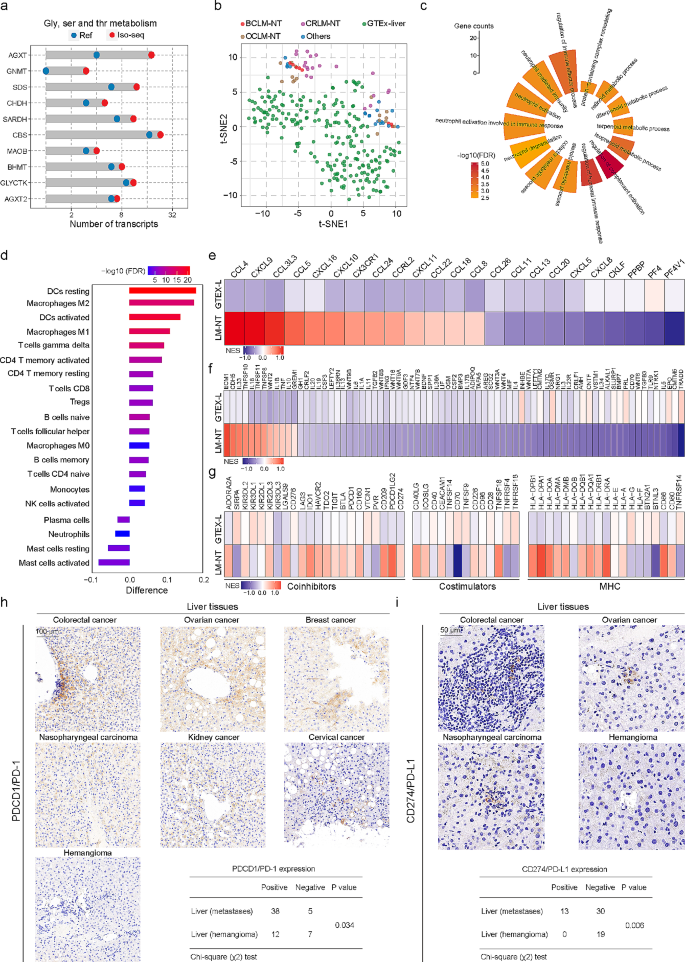
方法细节:比较癌旁肝组织(LM-NT)与GTEx正常肝组织的DETs,用CIBERSORT分析免疫细胞组成,用免疫组化(IHC)验证PD-1/PD-L1表达。
结果解读:①转录组变化:LM-NT的DETs富集在免疫反应(如补体激活、中性粒细胞活化)与代谢通路(如糖酵解、TCA循环);②免疫微环境:LM-NT中M2巨噬细胞、调节性T细胞(Treg)显著增加(P<0.05),提示免疫抑制;③免疫检查点:LM-NT的PD-1/PD-L1表达显著高于正常肝组织(IHC验证,P<0.01),且与细胞溶解活性(CYT)正相关(R=0.62,P<0.001)。
4. Biomarker研究及发现成果解析
4.1 Biomarker定位与筛选逻辑
本研究的Biomarker为肿瘤/转移特异性RNA转录本(SRTs),包括:
- HCC-SRTs:原发性HCC的特异性转录本,筛选逻辑为“肿瘤/癌旁表达比>10,且在>5%肿瘤样本中表达”;
- CRLM-SRTs:结直肠癌肝转移的特异性转录本,筛选逻辑为“CRLM/CRC原发灶表达比>1,FDR<0.05”;
- BCLM-SRTs:乳腺癌肝转移的特异性转录本,筛选逻辑同CRLM-SRTs。
4.2 研究过程详述
- 来源:临床样本的Iso-seq与RNA-seq数据(95例患者,177个样本);
- 验证方法:①差异表达分析(Wilcoxon秩和检验);②生存分析(Kaplan-Meier,Log-rank检验);③诊断价值评估(随机森林panel,ROC曲线);④免疫组化验证(PD-1/PD-L1);
- 特异性与敏感性:
- CRLM-SRTs panel:区分CRLM与CRC的AUC训练集0.935(敏感性91%,特异性88%),测试集0.966(敏感性95%,特异性92%);
- BCLM-SRTs panel:区分BCLM与乳腺癌的AUC训练集0.849(敏感性83%,特异性79%),测试集0.83(敏感性81%,特异性77%)。
4.3 核心成果提炼
- HCC-SRTs:作为HCC的预后Biomarker,SRT-high亚型患者的OS显著缩短(TCGA队列中HR=2.1,P=0.003);
- CRLM-SRTs:作为CRLM的诊断Biomarker,能有效区分CRLM与CRC原发灶,且准确预测转移灶的组织起源(结肠);
- BCLM-SRTs:作为BCLM的诊断Biomarker,区分BCLM与乳腺癌原发灶的准确性较高;
- 创新性:首次通过长读长测序系统识别原发性与转移性肝癌的特异性转录本,证实其临床价值,为肝癌的精准诊断与预后预测提供了新的分子标志物。
本研究通过长读长测序揭示了原发性与转移性肝癌的转录组复杂性,为肝癌的分子机制研究与临床转化提供了重要资源,其发现的SRTs有望成为肝癌预后与诊断的新型Biomarker。