1. 领域背景与文献引入
文献英文标题:Epigenetic reshaping through damage: promoting cell fate transition by BrdU and IdU incorporation;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:细胞重编程与表观遗传学
细胞重编程是再生医学领域的核心研究方向,自2006年山中伸弥团队成功诱导多能干细胞(iPSC)以来,化学小分子诱导重编程因无基因组整合风险、临床转化潜力高成为研究热点。然而,当前化学重编程存在效率低、重编程屏障机制不明确等核心问题,限制了其临床应用。现有研究发现胸苷类似物如BrdU、IdU可促进细胞重编程,但仅停留在表型观察层面,未深入解析其调控细胞命运转变的分子机制,尤其是DNA损伤修复通路与表观遗传重塑的关联尚未阐明。本研究针对这一领域空白,系统解析BrdU/IdU通过激活同源重组修复通路实现表观遗传重塑的具体机制,为优化细胞重编程策略提供了全新的理论依据。
2. 文献综述解析
作者对领域内现有研究的分类维度为“胸苷类似物的功能特性”与“细胞重编程机制的研究缺口”。现有研究显示,BrdU作为经典的增殖细胞标记物,可通过调控核架构重组促进化学诱导多能性;IdU则能引起基因表达随机波动,助力细胞突破重编程瓶颈,但这些研究仅关注表型变化,未揭示胸苷类似物如何调控DNA损伤修复通路,也未明确其与表观遗传修饰的关联。部分研究提出化学重编程需经历胚外内胚层(XEN)样中间状态,但未阐明该状态与DNA损伤修复的因果关系。本研究的创新价值在于首次提出“通过损伤的表观遗传重塑(ERD)”机制,将DNA损伤修复与基因组去甲基化、组蛋白乙酰化直接关联,阐明了胸苷类似物促进细胞命运转变的核心通路,弥补了现有研究在机制解析层面的空白,为细胞重编程的机制研究提供了新的范式。
3. 研究思路总结与详细解析
本研究的核心目标是阐明BrdU/IdU促进细胞重编程的分子机制,核心科学问题为胸苷类似物如何通过DNA损伤修复通路调控表观遗传修饰,实现细胞命运转变,技术路线遵循“表型观察→机制解析→多系统验证→安全性评估”的闭环逻辑。
3.1 化学诱导重编程中BrdU/IdU作用时间窗口优化
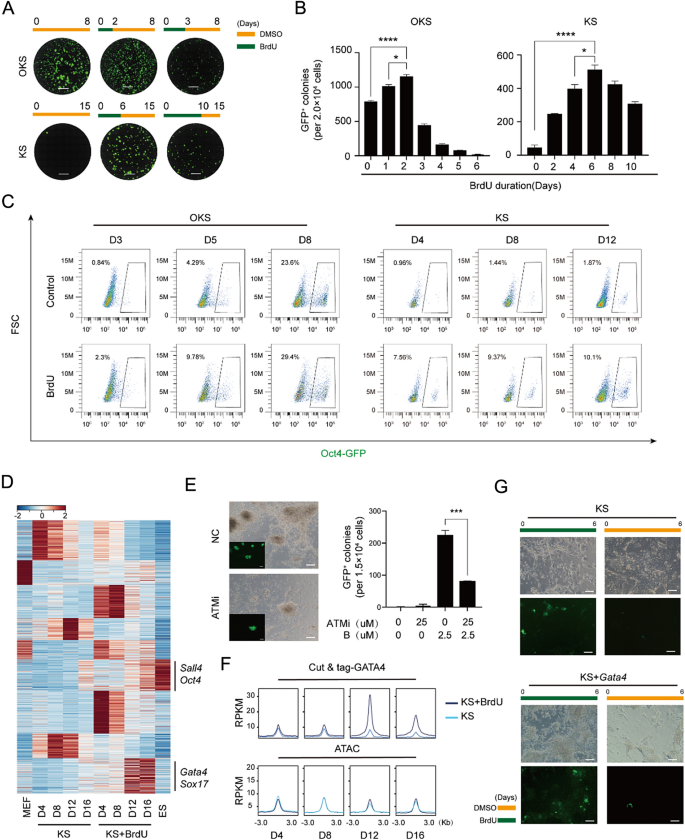
实验目的是确定BrdU/IdU克服重编程屏障的有效时间范围与剂量效应。研究采用小鼠胚胎成纤维细胞(MEFs)进行化学诱导多能干细胞(CiPSC)实验,设置不同BrdU处理时间梯度,通过检测Oct4-GFP阳性克隆形成情况评估重编程效率。结果显示,BrdU需在重编程启动后4天内开始处理,且持续处理至少6天才能有效突破重编程屏障;0-22天全程处理可使Oct4-GFP阳性克隆效率达1.2%(n=3,P<0.0001),而0-12天处理仅能获得约20个阳性克隆。同时,IdU可完全替代BrdU的功能,两者联用可进一步加速重编程进程,提高克隆纯度。
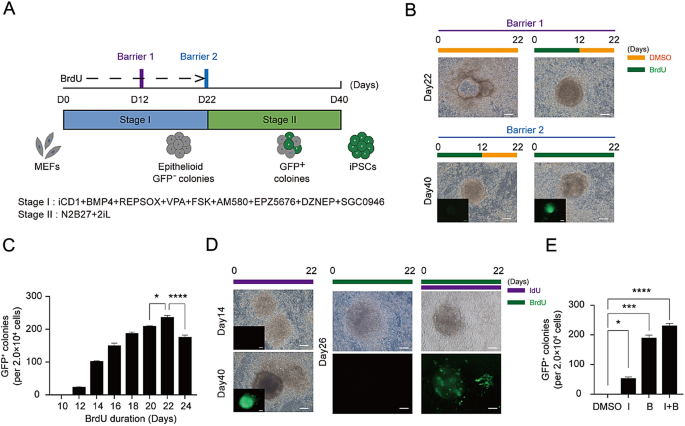
文献未提及具体实验产品,领域常规使用细胞培养试剂、荧光显微镜、流式细胞仪等。
3.2 转录组与染色质可及性动态分析
实验目的是解析BrdU/IdU调控的基因表达谱与染色质状态变化。研究对重编程不同时间点的细胞进行RNA-seq和ATAC-seq检测,结果显示,BrdU/IdU处理后,XEN样基因如Gata4、Sox17的表达随处理时间延长显著上调,且仅在胸苷类似物处理组中,XEN样基因与多能性基因(如Oct4、Tfcp2l1)的染色质区域呈现高可及性;两者联用可进一步增强染色质开放程度,加速细胞向多能态转变。生物信息学分析显示,BrdU/IdU处理可特异性激活GATA、KLF、SOX家族转录因子结合位点的染色质开放,为细胞命运转变提供了表观遗传基础。
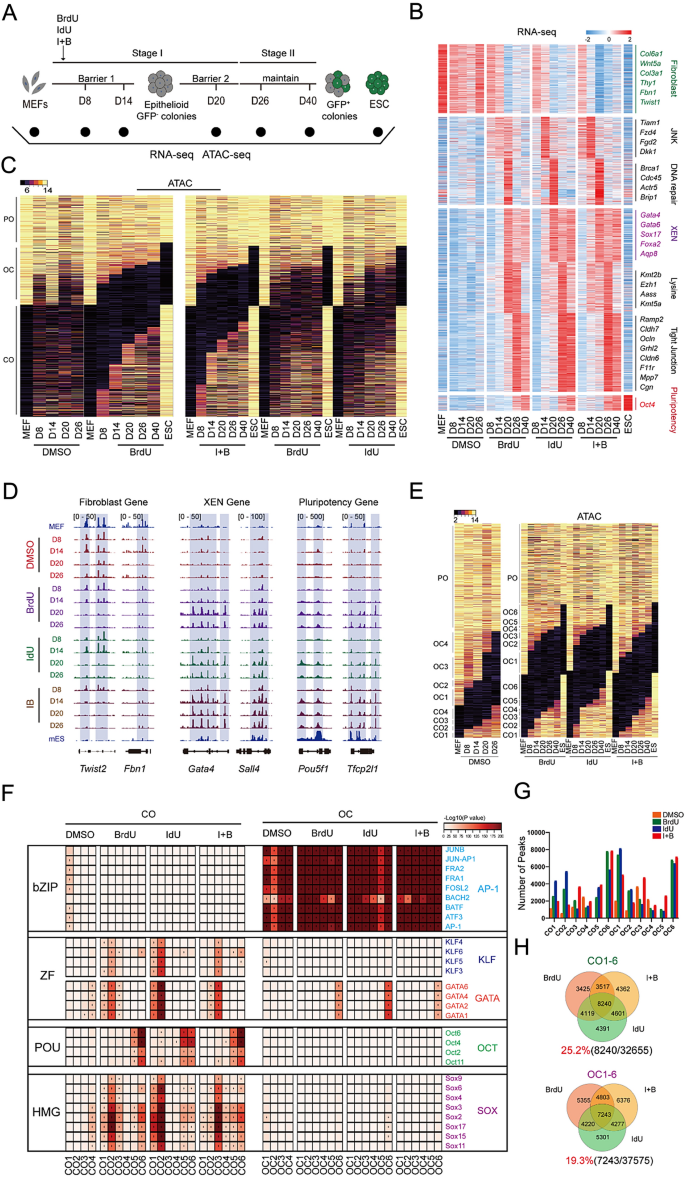
文献未提及具体实验产品,领域常规使用高通量测序平台、生物信息学分析软件等。
3.3 DNA损伤修复通路激活验证
实验目的是确认BrdU/IdU诱导DNA损伤修复的核心通路。通过RNA-seq功能富集分析发现,BrdU/IdU处理组中DNA修复相关基因显著上调,其中同源重组修复(HRR)通路基因Brca1、Brca2的表达随处理时间延长持续升高;碱性彗星实验显示,BrdU处理组细胞的橄榄尾矩显著增加(n=3,P<0.05),且在重编程第14天和第24天出现两个DNA损伤峰值,与重编程屏障时间窗口完全吻合;免疫荧光实验进一步证实BrdU与DNA双链断裂标记γ-H2AX共定位,表明BrdU/IdU通过掺入基因组诱导DNA损伤,进而激活HRR通路。
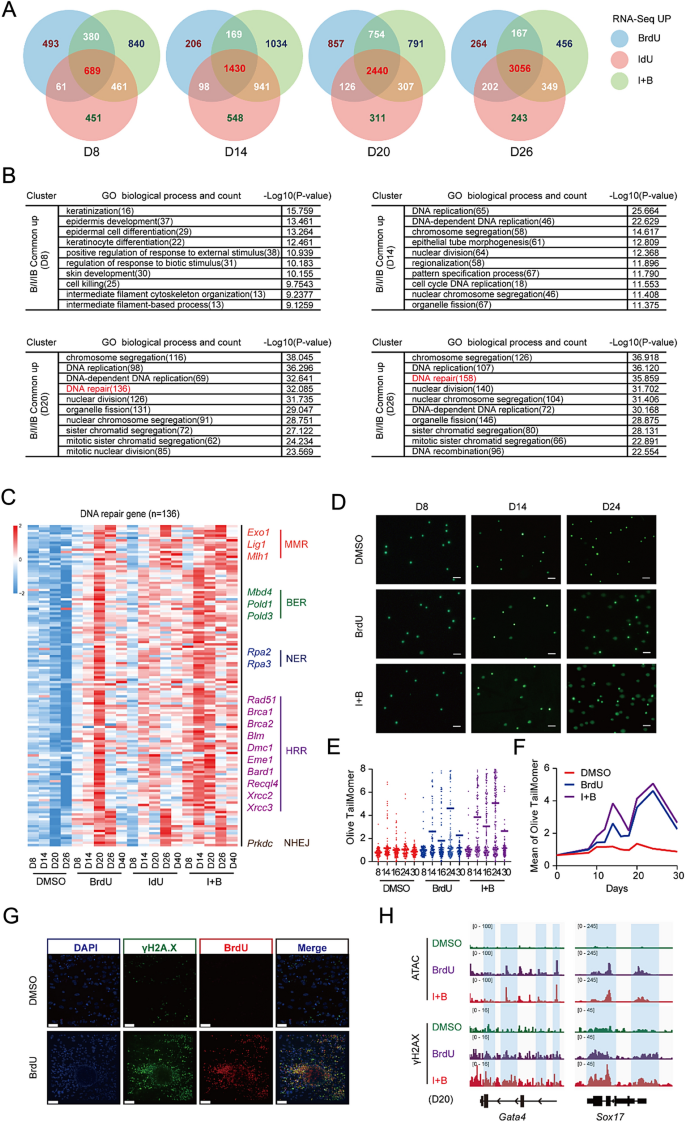
文献未提及具体实验产品,领域常规使用彗星检测试剂盒、免疫荧光抗体、共聚焦显微镜等。
3.4 表观遗传重塑机制解析
实验目的是阐明DNA损伤修复通路如何调控表观遗传修饰。研究使用ATM抑制剂KU-55933阻断DNA损伤修复通路后,BrdU无法促进重编程(n=3,P<0.01),表明ATM是介导BrdU功能的关键激酶;Cut&tag实验显示,BrdU/IdU处理可显著上调Gata4、Sox17等基因的H3K27ac、H3K9ac组蛋白乙酰化水平;全基因组甲基化分析(Gm-seq)显示,处理组细胞的CpG位点甲基化水平多集中在50%以下,而对照组则偏向50%以上,且多能性基因Sall4、Oct4的启动子区域呈现显著低甲基化状态。此外,抑制DNA甲基转移酶(DNMT)可加速重编程进程,且该效应依赖于BrdU的存在,证实DNA损伤修复通路通过组蛋白乙酰化和基因组去甲基化实现表观遗传重塑。
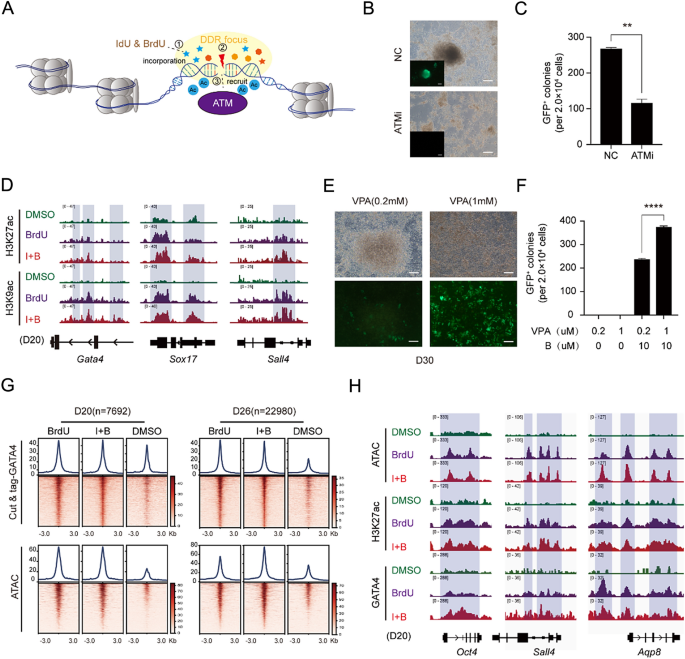
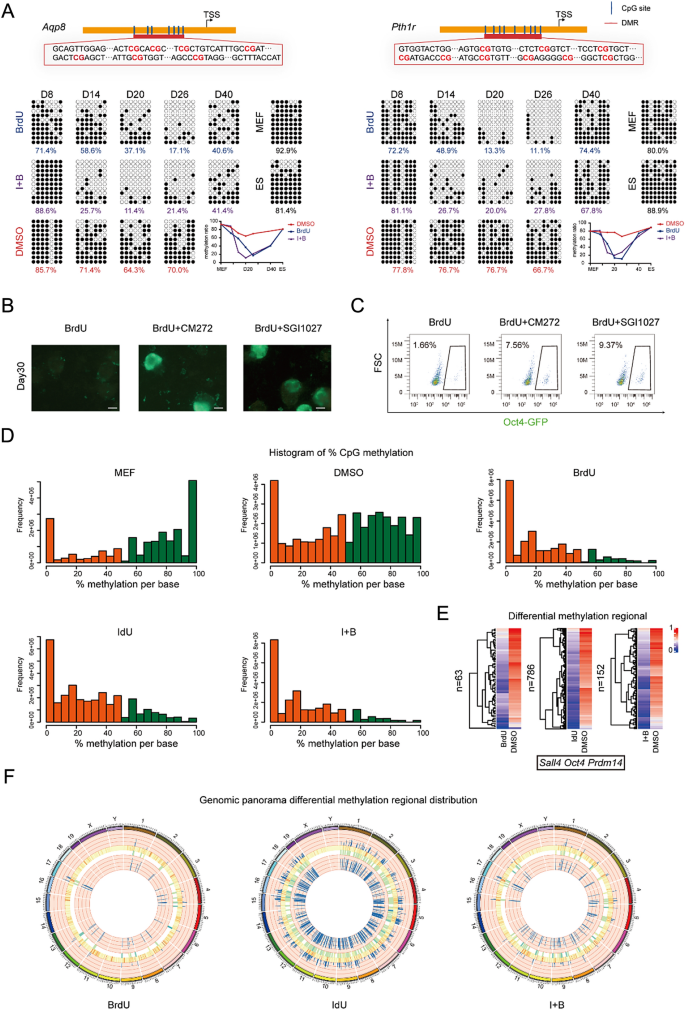
文献未提及具体实验产品,领域常规使用组蛋白修饰抗体、甲基化测序技术、表观遗传抑制剂等。
3.5 多系统验证与安全性评估
实验目的是验证BrdU/IdU作用的通用性与临床应用安全性。研究在OKS(Oct4、Klf4、Sox2)和KS(Klf4、Sox2)重编程系统中测试发现,BrdU可显著提高各系统的重编程效率,且在KS系统中可替代Oct4的功能;全基因组突变分析显示,BrdU/IdU处理组的单核苷酸多态性(SNP)、插入缺失(InDel)等突变水平与原代MEFs无显著差异,仅IdU处理组存在少量插入突变,表明合理剂量的BrdU/IdU可安全应用于细胞命运调控。
文献未提及具体实验产品,领域常规使用病毒转染系统、全基因组测序平台等。
4. Biomarker研究及发现成果
Biomarker定位与筛选逻辑
本研究涉及两类核心Biomarker:一是DNA损伤标记物γ-H2AX,二是XEN样状态标记物Gata4。筛选逻辑为:通过RNA-seq和ATAC-seq筛选差异表达基因与染色质开放区域,结合免疫荧光、Cut&tag实验验证标记物的特异性与功能关联性。
研究过程详述
γ-H2AX作为DNA双链断裂的特异性标记物,来源为重编程过程中的细胞样本,验证方法为免疫荧光共定位实验,结果显示BrdU处理组中γ-H2AX与BrdU的共定位率显著高于对照组,且在重编程第14天和第24天达到峰值(n=3,P<0.05),反映了DNA损伤的动态变化。Gata4作为XEN样状态的核心标记物,来源为细胞转录组与染色质可及性数据,验证方法为RNA-seq、Cut&tag实验与亚硫酸氢盐测序,结果显示BrdU/IdU处理后Gata4的表达水平上调5倍以上(n=3,P<0.01),其启动子区域染色质可及性提高3倍,下游基因Aqp8的甲基化水平降低40%(n=3,P<0.05),证实Gata4是介导表观遗传重塑的关键因子。
核心成果提炼
γ-H2AX可作为监测细胞重编程进程中DNA损伤程度的功能性Biomarker,其表达峰值与重编程屏障时间窗口高度吻合,为优化重编程时间提供了量化指标。Gata4作为BrdU/IdU调控细胞命运转变的关键下游因子,不仅是XEN样中间状态的标记物,还可响应DNA损伤修复通路,激活多能性基因的染色质开放,其创新性在于首次确立了Gata4在DNA损伤修复与表观遗传重塑之间的桥梁作用。此外,研究未发现Gata4作为预后Biomarker的相关数据,但其作为细胞命运转变的调控因子,为开发新型重编程小分子提供了靶点。
