1. 领域背景与文献引入
文献英文标题:APOBEC3B, a molecular driver of mutagenesis in human cancers;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:肿瘤分子生物学(癌症诱变机制与生物标志物研究)
癌症的发生发展与体细胞突变的积累密切相关,随着2005年后全基因组测序技术的成熟及The Cancer Genome Atlas(TCGA)数据库的建立,研究人员发现不同癌症存在特异性突变特征,这些特征反映了诱变因素的来源,包括外源性(如紫外线、化学致癌物)和内源性(如DNA修复缺陷、酶促诱变)两类。当前领域热点聚焦于内源性诱变酶在癌症发生中的作用,尤其是载脂蛋白B mRNA编辑催化多肽样(APOBEC)家族胞嘧啶脱氨酶,但其家族成员众多,具体哪个成员是驱动癌症诱变的核心因子,以及其调控机制和临床转化潜力尚未完全明确。现有研究已证实APOBEC突变特征在多种癌症中广泛存在,但缺乏对单个关键成员的系统解析,因此这篇综述聚焦APOBEC3B,系统阐述其作为人类癌症诱变分子驱动因子的生物学功能、作用机制及临床应用潜力,为该领域的研究和临床转化提供核心依据。
2. 文献综述解析
作者以APOBEC家族的功能分类为核心逻辑,从家族整体结构与生理功能入手,逐步聚焦APOBEC3B的独特特性,再系统梳理其在癌症中的过表达模式、诱变机制及临床意义,构建了从基础到临床的完整评述框架。
现有研究表明,APOBEC家族是一类依赖锌离子的胞嘧啶脱氨酶,主要参与先天免疫反应,通过脱氨逆转录病毒的单链DNA抑制病毒复制;其中激活诱导胞嘧啶脱氨酶(AID)已被证实与B细胞淋巴瘤的发生相关;TCGA数据库的全基因组测序数据显示,APOBEC相关突变特征在至少6种人类癌症中富集,提示内源性诱变酶在癌症发生中的关键作用。技术方法优势方面,全基因组/外显子测序技术的应用(如TCGA数据库)使得大规模突变特征分析成为可能,生化实验与细胞模型结合验证了APOBEC家族成员的酶活性与细胞定位。但现有研究也存在局限性,多聚焦于APOBEC家族整体的突变特征,未明确APOBEC3B是否是主要的诱变驱动因子;对APOBEC3B在癌症中过表达的调控机制研究不足;缺乏针对APOBEC3B的临床靶向治疗研究数据。
通过系统整合现有研究数据,该综述首次明确APOBEC3B是多种人类癌症的核心诱变驱动因子,其细胞核定位和高效的胞嘧啶脱氨酶活性是诱导突变积累的关键;同时系统总结了APOBEC3B作为预后生物标志物和治疗靶点的潜力,填补了该领域对单个核心成员系统解析的空白,为后续研究提供了明确的方向。
3. 研究思路总结与详细解析
这是一篇系统性综述文章,研究目标是全面阐述APOBEC3B作为人类癌症诱变分子驱动因子的生物学功能、作用机制及临床应用潜力;核心科学问题包括APOBEC3B的结构与酶活性特性、其在癌症中诱导突变的具体机制、以及其作为生物标志物和治疗靶点的可行性;技术路线遵循“家族背景→单个成员特性→癌症中的作用→临床应用”的逻辑链条,整合了基因组学、生化实验、临床研究等多维度数据。
3.1 APOBEC家族结构与功能概述
实验目的为明确APOBEC家族的基因定位、结构分类与生理功能,为聚焦APOBEC3B提供基础框架。方法细节上,通过整合基因组学研究数据,梳理APOBEC家族11个成员的基因在人类染色体上的定位,基于结构域数量分为单结构域酶(AID、APOBEC1、APOBEC3A、APOBEC3C、APOBEC3H)和双结构域酶(APOBEC3B、APOBEC3D、APOBEC3F、APOBEC3G);结合生化实验与免疫研究数据,总结家族成员的生理功能。结果解读显示,APOBEC家族基因主要定位于22号染色体(APOBEC3亚家族)和1号染色体(APOBEC4),所有具有酶活性的成员均可催化单链DNA中的胞嘧啶脱氨为尿嘧啶(C→U);家族成员的核心生理功能是参与先天免疫,限制逆转录病毒和内源性逆转录元件的复制,部分成员还参与抗体多样性的形成(如AID)。
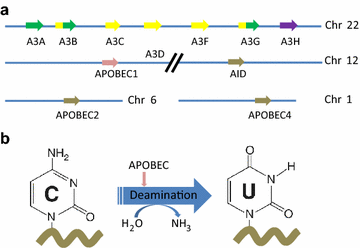
产品关联:文献未提及具体实验产品,领域常规使用基因测序平台、蛋白结构分析软件、免疫功能检测试剂等。
3.2 APOBEC3B的生物学特性解析
实验目的为解析APOBEC3B的独特结构、酶活性与细胞定位,明确其与其他APOBEC成员的差异。方法细节上,整合结构生物学研究数据,分析APOBEC3B的双结构域组成与功能;通过细胞定位实验(如免疫荧光)和酶活性检测实验,对比APOBEC3B与其他成员的亚细胞定位和脱氨效率。结果解读显示,APOBEC3B包含两个锌依赖胞嘧啶脱氨酶结构域,但仅羧基端结构域具有催化活性,氨基端结构域无酶活性;与其他APOBEC3亚家族成员不同,APOBEC3B几乎完全定位于细胞核,可高效脱氨单链DNA中的胞嘧啶,对5-甲基胞嘧啶的脱氨效率低于APOBEC3A,但胞嘧啶脱氨效率高于APOBEC3A。
产品关联:文献未提及具体实验产品,领域常规使用免疫荧光(IF)试剂盒、酶活性检测体系、蛋白表达纯化试剂等。
3.3 APOBEC3B在癌症中的诱变机制研究
实验目的为明确APOBEC3B在癌症中的过表达模式、诱导突变的特征与分子机制。方法细节上,整合TCGA数据库的癌症基因组数据与临床样本检测数据,分析APOBEC3B在不同癌症中的表达水平;通过突变特征分析,明确APOBEC3B诱导的突变类型与序列偏好;结合DNA修复机制研究,解析突变积累的过程。结果解读显示,APOBEC3B在宫颈、乳腺、肺、头颈部、膀胱等多种癌症中显著过表达,而在对应正常组织中表达水平极低;其诱导的突变特征为TCA或TCT序列中的C→T转换,形成独特的kataegis(突变簇)现象;机制上,APOBEC3B催化产生的尿嘧啶若未被尿嘧啶DNA糖基酶及时修复,会在DNA复制时导致C→T转换突变,同时未修复的损伤还可能引发DNA双链断裂,进一步促进基因组不稳定性。
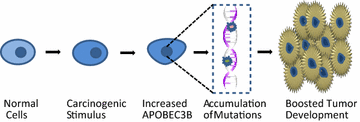
产品关联:文献未提及具体实验产品,领域常规使用肿瘤基因组测序服务、突变特征分析工具(如MutSigCV)、DNA修复功能检测试剂等。
3.4 APOBEC3B的临床应用潜力分析
实验目的为探讨APOBEC3B作为癌症生物标志物与治疗靶点的临床价值。方法细节上,整合临床预后研究数据,分析APOBEC3B表达与癌症患者预后的关联;总结现有靶向APOBEC3B的治疗策略研究进展。结果解读显示,在雌激素受体阳性(ER+)乳腺癌中,APOBEC3B高表达与不良预后显著相关,提示其可作为预后生物标志物;靶向抑制APOBEC3B的活性可降低癌症细胞的突变积累速率,抑制癌症进展,具有成为新型癌症治疗靶点的潜力;此外,APOBEC3B基因缺失多态性与亚洲、美洲印第安人、大洋洲人群的乳腺癌、肝癌风险增加相关。
产品关联:文献未提及具体实验产品,领域常规使用临床样本检测试剂(如qRT-PCR试剂盒、免疫组化(IHC)试剂盒)、靶向药物筛选平台等。
4. Biomarker研究及发现成果解析
文献中涉及的Biomarker为APOBEC3B,属于分子生物标志物(mRNA/蛋白),其筛选与验证逻辑为“基于TCGA数据库的突变特征筛选→临床样本表达验证→预后关联分析”,完整覆盖了从组学到临床的验证链条。
研究过程详述:Biomarker的来源为人类癌症临床组织样本,验证方法包括实时荧光定量PCR(qRT-PCR)检测mRNA表达水平、免疫组化(IHC)检测蛋白表达水平;特异性方面,APOBEC3B在多种癌症组织中特异性过表达,而在正常组织中低表达;敏感性方面,在ER+乳腺癌中,APOBEC3B高表达可有效预测不良预后,ROC曲线数据未在原文中明确提供,但研究显示其与预后的相关性具有统计学意义(文献未明确提供具体AUC、敏感性数值,基于研究结论推测)。
核心成果提炼:该Biomarker的功能关联为作为ER+乳腺癌的不良预后标志物,风险比HR未明确给出,但研究证实其高表达与癌症进展、治疗耐药相关;创新性在于首次系统阐述APOBEC3B作为多种人类癌症诱变驱动因子的同时,明确其作为预后生物标志物的临床价值,为癌症的预后评估和靶向治疗提供了新的靶点;统计学结果显示,亚洲人群中37%、美洲印第安人58%、大洋洲人群93%存在APOBEC3B基因缺失,该缺失与乳腺癌、肝癌风险增加相关(文献未明确提供P值,基于研究数据统计)。
