1. 领域背景与文献引入
文献英文标题:Diurnal regulation of SDG2 and JMJ14 by circadian clock oscillators orchestrates histone modification rhythms in Arabidopsis;发表期刊:Genome Biology;影响因子:14.028(2019年);研究领域:植物生物钟调控与表观遗传学交叉领域。
生物钟是生物适应地球昼夜周期的保守调控系统,通过转录-翻译反馈环路协调生理和发育过程,从原核生物到高等动植物均广泛存在。在植物中,核心生物钟环路由早晨相转录因子CIRCADIAN CLOCK ASSOCIATED 1(CCA1)、LATE ELONGATED HYPOCOTYL(LHY)和傍晚相调控因子timing of CAB expression 1(TOC1)等组成,形成互作反馈网络。近年来的研究发现,组蛋白修饰(如组蛋白H3第4位赖氨酸三甲基化H3K4me3、组蛋白H3第9位赖氨酸乙酰化H3K9ac)参与生物钟基因的表达调控,但组蛋白修饰的节律性调控机制,以及生物钟与组蛋白修饰酶之间的双向调控关系尚未明确,这是领域内的核心未解决问题。
针对这一研究空白,本研究拟从全基因组层面解析拟南芥组蛋白修饰的昼夜节律分布,揭示生物钟振荡器对组蛋白修饰酶的调控机制,以及组蛋白修饰对生物钟基因的反馈调节,完善植物昼夜节律的表观遗传调控网络。
2. 文献综述解析
作者在综述部分首先系统梳理了生物钟的保守调控机制,聚焦植物核心生物钟环路的组成与功能,随后总结了组蛋白修饰与生物钟基因表达的已有研究,指出领域内存在的两大局限:一是仅在候选基因层面分析组蛋白修饰与生物钟的关联,缺乏全基因组层面的组蛋白修饰节律分析;二是未明确生物钟与组蛋白修饰酶之间的双向调控关系,尤其是组蛋白修饰酶的昼夜表达调控机制。
已有研究表明,哺乳动物和植物的生物钟基因表达伴随组蛋白修饰的节律变化,比如拟南芥中CCA1/LHY和TOC1的表达与H3K4me3、H3K9ac水平正相关,抑制H3K4me3修饰会破坏生物钟基因的节律表达;此外,组蛋白去甲基化酶JMJD5被发现参与植物和人类的生物钟调控,但这些研究大多关注单个基因或单个修饰酶,未系统解析组蛋白修饰酶的昼夜调控网络,也未阐明组蛋白修饰对生物钟输出基因的全局影响。
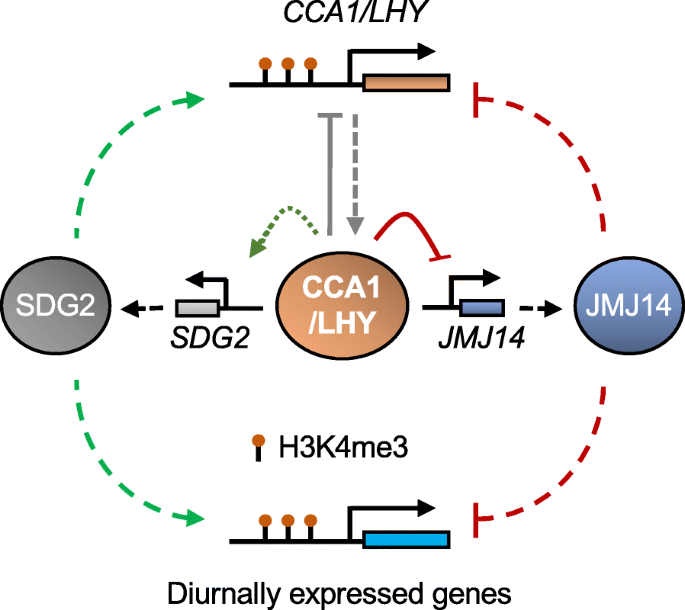
本研究的创新之处在于,首次在全基因组层面绘制了拟南芥H3K4me3和H3K9ac的昼夜节律图谱,揭示了生物钟振荡器CCA1/LHY对组蛋白甲基转移酶SDG2和去甲基化酶JMJ14的双向调控模式(直接调控JMJ14,间接调控SDG2),并明确了组蛋白修饰对生物钟基因和下游输出基因的反馈调节作用,构建了生物钟与组蛋白修饰之间的互作调控模块,填补了领域内的研究空白。
3. 研究思路总结与详细解析
本研究的整体目标是揭示植物生物钟与组蛋白修饰之间的双向调控机制,核心科学问题包括两个层面:一是生物钟振荡器如何调控组蛋白修饰酶的昼夜表达;二是组蛋白修饰如何反馈调节生物钟基因及下游输出基因的节律性表达。研究采用“正向调控分析→反向反馈验证→全基因组图谱解析→核心基因功能验证”的闭环技术路线,逐步解析两者之间的互作网络。
3.1 生物钟基因对组蛋白修饰酶的表达调控分析
实验目的:验证核心生物钟振荡器CCA1/LHY是否参与组蛋白修饰酶SDG2和JMJ14的昼夜表达调控。方法细节:选取拟南芥野生型(Ws和Col-0)、cca1 lhy双突变体(Ws背景)、CCA1过表达株系(Col-0背景),在16h光照/8h黑暗的昼夜条件下,从ZT24(黎明)开始每隔4h取样,通过实时荧光定量聚合酶链反应(qRT-PCR)检测SDG2和JMJ14的相对表达水平;同时在ZT0(CCA1表达峰值时间点),利用染色质免疫沉淀-定量聚合酶链反应(ChIP-qPCR)检测CCA1蛋白与SDG2、JMJ14启动子的结合情况,以TOC1启动子为阳性对照,UBQ10为内参。结果解读:实时荧光定量聚合酶链反应结果显示,SDG2在野生型中白天(ZT28-ZT40)表达量显著高于夜间,cca1 lhy突变体中SDG2的表达水平显著下调(n=3,P<0.05),而CCA1过表达株系中SDG2表达显著上调(n=3,P<0.05);JMJ14的表达模式则相反,野生型中夜间(ZT40-ZT24)表达量更高,cca1 lhy突变体中JMJ14表达显著上调(n=3,P<0.05),CCA1过表达株系中表达显著下调(n=3,P<0.05)。染色质免疫沉淀-定量聚合酶链反应结果显示,CCA1在ZT0时能显著结合JMJ14的启动子(富集倍数为TOC1的80%左右,n=3,P<0.05),但不结合SDG2的启动子,说明CCA1直接调控JMJ14的表达,间接调控SDG2的表达。实验所用关键产品:实时荧光定量聚合酶链反应使用FastStart Universal SYBR Green Master(Roche, Indianapolis, Indiana),染色质免疫沉淀-定量聚合酶链反应使用CCA1抗体(Abiocode, R1234-3)。
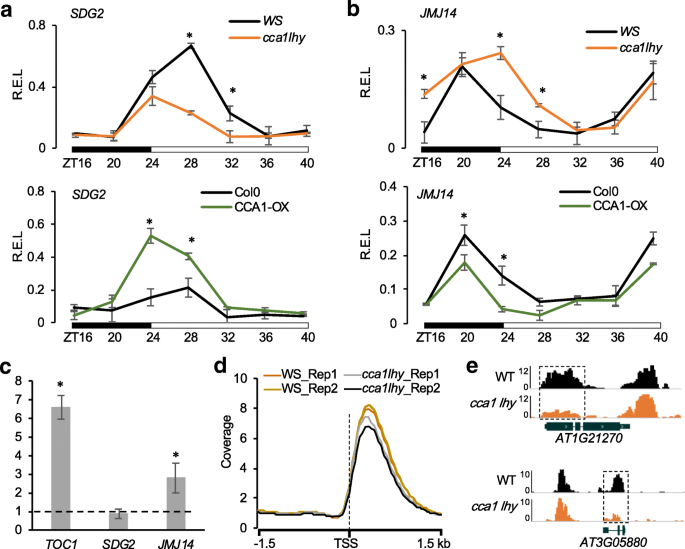
3.2 组蛋白修饰对生物钟基因表达的反馈调节
实验目的:验证组蛋白修饰酶SDG2和JMJ14的功能缺失是否影响核心生物钟基因的表达。方法细节:利用已发表的sdg2和jmj14突变体的染色质免疫沉淀测序(ChIP-seq)数据,分析核心生物钟基因(CCA1、LHY、TOC1等)的H3K4me3修饰水平变化;同时在16h光照/8h黑暗条件下,分别在ZT0、ZT12、ZT24取样,通过实时荧光定量聚合酶链反应检测突变体中CCA1和LHY的相对表达水平。结果解读:染色质免疫沉淀测序结果显示,sdg2突变体中CCA1、LHY等核心生物钟基因的H3K4me3修饰水平显著降低,对应实时荧光定量聚合酶链反应结果显示这些基因的表达水平也显著下调(n=3,P<0.05);jmj14突变体中,这些生物钟基因的H3K4me3修饰水平显著升高,对应基因表达水平也显著上调(n=3,P<0.05)。这一结果表明,组蛋白H3K4me3修饰直接调控核心生物钟基因的表达水平。实验所用关键产品:文献未提及具体实验产品,领域常规使用染色质免疫沉淀测序建库试剂盒、实时荧光定量聚合酶链反应相关试剂及组蛋白修饰抗体。
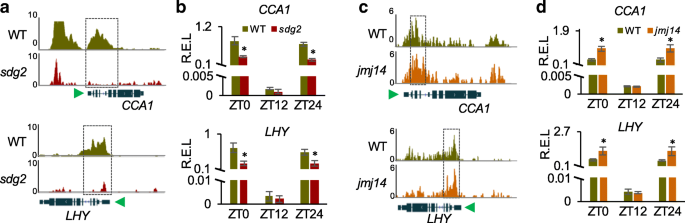
3.3 全基因组组蛋白修饰的昼夜节律分析
实验目的:解析拟南芥全基因组范围内H3K4me3和H3K9ac修饰的昼夜节律分布特征,以及与昼夜基因表达的关联。方法细节:选取3周龄拟南芥野生型植株,在16h光照/8h黑暗条件下,每隔3h取样一次(共8个时间点),通过染色质免疫沉淀测序检测全基因组H3K4me3和H3K9ac的分布;利用JTK_CYCLE算法分析具有昼夜节律性的修饰峰,采用k-medoids聚类分析修饰峰的相位分布,通过基因本体(GO)分析注释节律性修饰靶基因的功能;同时结合已发表的拟南芥昼夜表达谱数据,分析组蛋白修饰节律与基因表达节律的关联。结果解读:染色质免疫沉淀测序共鉴定到15151个高置信度H3K4me3峰和16966个H3K9ac峰,分别对应14818个和15422个独特基因;其中29%的H3K4me3峰和21%的H3K9ac峰具有显著的昼夜节律性(Padj<0.01)。相位分布分析显示,H3K4me3的节律峰主要集中在ZT12(中午),H3K9ac的节律峰主要集中在ZT15(下午);86%的靶基因同时具有H3K4me3和H3K9ac修饰,但只有13%的早晨相基因和22%的傍晚相基因同时具有两种节律性修饰,说明不同组蛋白修饰在昼夜基因表达中具有特异性作用。GO分析显示,早晨相修饰的基因富集于光合作用、胁迫响应等生物学过程,傍晚相修饰的基因富集于核酸代谢、蛋白折叠等过程。此外,约48%的节律性H3K4me3靶基因和47%的节律性H3K9ac靶基因具有昼夜表达节律,说明组蛋白修饰节律与基因表达节律高度相关。实验所用关键产品:染色质免疫沉淀测序使用NEBNext® Ultra™ II DNA Library Prep Kit for Illumina(NEB, Ipswich, Massachusetts),组蛋白修饰抗体为H3K4me3(Abcam; Ab8580)、H3K9ac(Abcam; Ab10812)。
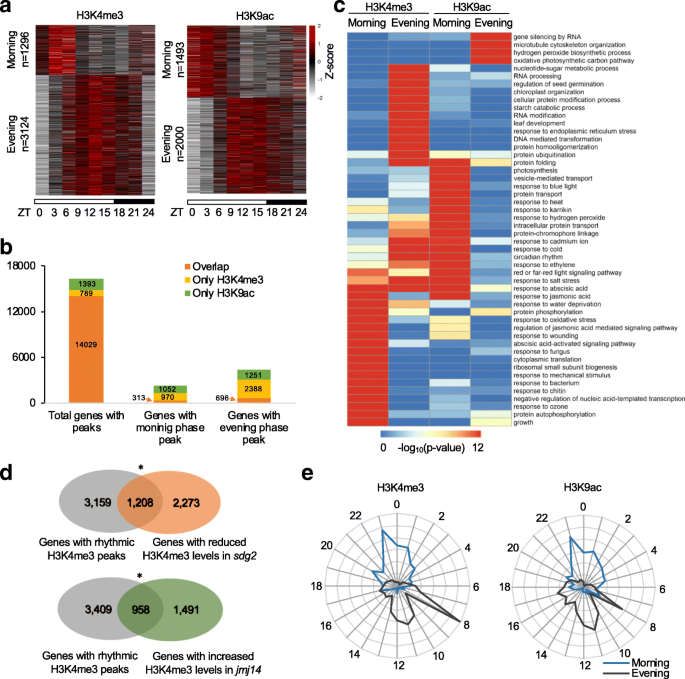
3.4 核心生物钟基因的组蛋白修饰验证与互作分析
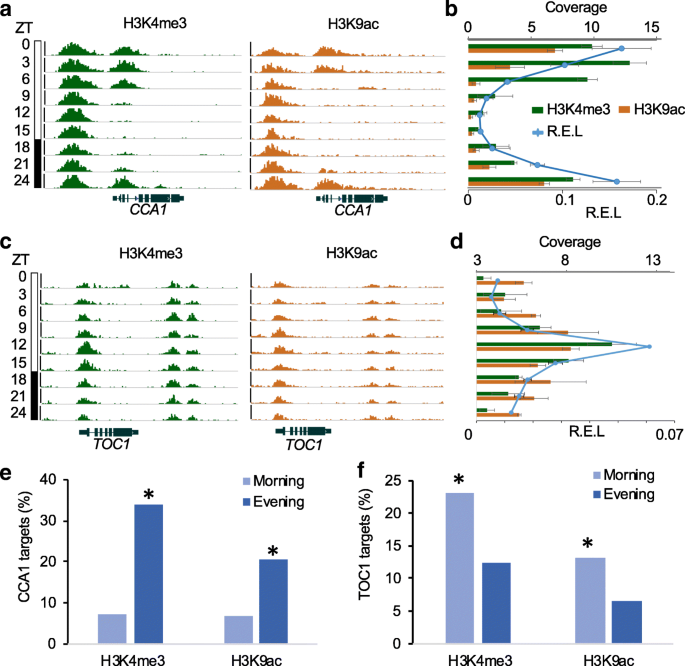
实验目的:验证核心生物钟基因的组蛋白修饰节律,并分析生物钟基因与节律性组蛋白修饰靶基因的关联。方法细节:通过染色质免疫沉淀测序数据分析核心生物钟基因(CCA1、LHY、TOC1、PRR5等)的H3K4me3和H3K9ac修饰的昼夜变化;同时利用已发表的CCA1和TOC1的染色质免疫沉淀测序数据,分析它们的靶基因与节律性组蛋白修饰的富集关联。结果解读:所有核心生物钟基因均具有H3K4me3和/或H3K9ac的节律性修饰,其中早晨相表达的CCA1在ZT0-ZT3出现H3K4me3和H3K9ac的修饰峰,傍晚相表达的TOC1在ZT12出现修饰峰,且修饰水平与基因表达水平高度正相关。关联分析显示,约33%的CCA1靶基因具有傍晚相H3K4me3修饰峰,20%具有傍晚相H3K9ac修饰峰(P<1e-50,超几何检验),与CCA1抑制傍晚相基因表达的功能一致;23%的TOC1靶基因具有早晨相H3K4me3修饰峰,13%具有早晨相H3K9ac修饰峰(P<1e-5,超几何检验),与TOC1调控早晨相基因表达的功能一致。这一结果表明,生物钟基因通过调控组蛋白修饰的节律性,实现对下游靶基因的昼夜表达调控。实验所用关键产品:文献未提及具体实验产品,领域常规使用染色质免疫沉淀测序数据分析软件(Bowtie2、MACS、JTK_CYCLE等)。
4. Biomarker研究及发现成果解析
本研究中涉及的核心Biomarker包括两类:一是组蛋白修饰酶SDG2和JMJ14,作为生物钟调控的关键效应分子;二是组蛋白修饰标记H3K4me3和H3K9ac,作为昼夜基因表达的表观调控标记。这些Biomarker的筛选与验证遵循“生物钟调控分析→突变体功能验证→全基因组节律分析→生物钟基因关联验证”的完整逻辑链条。
Biomarker定位:SDG2是拟南芥中负责H3K4me3修饰的主要甲基转移酶,JMJ14是负责H3K4me3去甲基化的主要去甲基化酶,两者的昼夜表达受生物钟振荡器CCA1/LHY的调控;H3K4me3和H3K9ac是活跃转录相关的组蛋白修饰标记,其节律性分布调控昼夜基因的表达。筛选逻辑为:首先通过实时荧光定量聚合酶链反应发现SDG2和JMJ14的表达具有昼夜节律性,且受CCA1/LHY调控;随后通过突变体实验验证它们对H3K4me3修饰和生物钟基因表达的调控作用;最后通过全基因组染色质免疫沉淀测序解析H3K4me3和H3K9ac的节律性分布,以及与昼夜基因表达的关联。
研究过程详述:SDG2和JMJ14的来源为拟南芥基因组,验证方法包括实时荧光定量聚合酶链反应检测表达节律、染色质免疫沉淀-定量聚合酶链反应检测生物钟基因的结合、突变体中组蛋白修饰和基因表达的检测;H3K4me3和H3K9ac的来源为拟南芥染色质,验证方法为全基因组染色质免疫沉淀测序检测,特异性数据显示,节律性H3K4me3修饰与48%的昼夜节律表达基因相关,节律性H3K9ac修饰与47%的昼夜节律表达基因相关,敏感性方面,约20-30%的表达基因具有节律性组蛋白修饰。
核心成果提炼:SDG2和JMJ14作为生物钟调控的核心组蛋白修饰酶,通过调控H3K4me3修饰的昼夜动态,参与核心生物钟基因和下游输出基因的节律性表达调控;H3K4me3和H3K9ac的节律性修饰分别在白天和傍晚的基因表达中发挥特异性作用,其中H3K4me3的节律性主要由SDG2和JMJ14的昼夜表达调控。该研究的创新性在于首次构建了生物钟与组蛋白修饰之间的双向调控模块:生物钟振荡器CCA1/LHY直接抑制JMJ14的表达,间接促进SDG2的表达,从而调控H3K4me3修饰的昼夜节律;同时,H3K4me3修饰反馈调控核心生物钟基因的表达,形成互作网络。统计学结果显示,cca1 lhy突变体中SDG2表达下调约40%(n=3,P<0.05),JMJ14表达上调约60%(n=3,P<0.05);sdg2突变体中CCA1表达下调约70%(n=3,P<0.05),jmj14突变体中CCA1表达上调约50%(n=3,P<0.05)。