1. 领域背景与文献引入
文献英文标题:Significant transcriptomic changes are associated with differentiation of bone marrow-derived mesenchymal stem cells into neural progenitor-like cells in the presence of bFGF and EGF;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:干细胞与神经再生(骨髓间充质干细胞向神经前体细胞分化的转录组调控)
干细胞治疗是神经退行性疾病、脊髓损伤等神经系统疾病的潜在治疗策略,其中骨髓间充质干细胞(MSCs)因来源广泛、伦理争议小、多向分化潜能强等优势,成为该领域的研究热点。领域发展关键节点包括2000年前后证实MSCs可向神经谱系分化,2009年明确部分MSCs起源于神经嵴,为其神经分化潜能提供了发育学依据;当前研究热点集中于优化MSCs向神经谱系的分化效率、解析分化过程的分子调控机制,未解决的核心问题是MSCs向神经前体细胞(NPCs)分化早期阶段的转录组调控网络不清晰,缺乏特异性生物标志物用于鉴定分化阶段,且难以精准调控分化过程以提高分化效率和细胞功能。
针对上述研究空白,本研究聚焦MSCs向NPCs分化的早期阶段(诱导第3天),通过高通量mRNA测序系统解析转录组差异,鉴定差异表达基因、关键调控通路及转录因子,旨在为NPCs分化阶段的标志物鉴定、分化策略优化提供系统性的分子依据,填补早期分化阶段转录组调控研究的空白。
2. 文献综述解析
作者对领域内现有研究的分类维度为MSCs神经分化潜能的来源、体外分化方法的分类、现有研究的局限性三个层面。
现有研究的核心支持观点包括:MSCs具有向神经谱系分化的潜能,部分MSCs起源于神经嵴,这是其神经分化潜能的发育学基础;体外诱导MSCs向神经谱系分化的方法主要分为两类,一类是先诱导为NPCs再进一步分化为神经元或胶质细胞,另一类是直接诱导MSCs分化为神经细胞,其中先诱导为NPCs的方法因获得的细胞更适合悬浮移植,在细胞治疗应用中更具优势。现有研究的技术方法优势在于证实了MSCs向神经谱系分化的可行性,部分研究通过添加生长因子(如IGF-1)优化了分化条件,提高了细胞存活率和分化效率;但局限性也较为明显,多数研究仅聚焦于分化终末阶段的细胞功能验证,对早期分化阶段的转录组调控网络解析不足,缺乏系统性的差异基因分析,且对关键转录因子的调控作用研究不深入,难以明确分化过程的核心调控机制。
通过对比现有研究的不足,本研究的创新价值凸显:首次系统解析了MSCs向NPCs分化第3天的转录组差异,鉴定出3252个差异表达基因及149个差异表达转录因子,填补了早期分化阶段分子机制研究的空白;同时通过生物信息学分析全面解析了分化过程中的关键通路和调控网络,为后续鉴定分化阶段特异性标志物、优化分化策略提供了全面的转录组数据支持,具有重要的学术必要性。
3. 研究思路总结与详细解析
本研究的整体框架为:以具有多向分化潜能的大鼠骨髓MSCs为研究对象,诱导其分化为NPCs并验证细胞特性,通过mRNA测序解析MSCs与NPCs的转录组差异,结合生物信息学分析鉴定关键调控基因、通路及转录因子,最后通过qPCR验证测序结果的可靠性,形成“细胞模型构建→诱导分化与鉴定→转录组测序与分析→结果验证”的完整研究闭环。研究目标是解析MSCs向NPCs分化早期的转录组变化,鉴定关键调控分子与通路;核心科学问题是明确MSCs向NPCs分化过程中差异表达基因的功能及转录因子的调控作用。
3.1 大鼠骨髓MSCs的分离培养与鉴定
实验目的:获取具有典型多向分化潜能的大鼠骨髓MSCs,为后续分化实验提供合格的细胞模型。
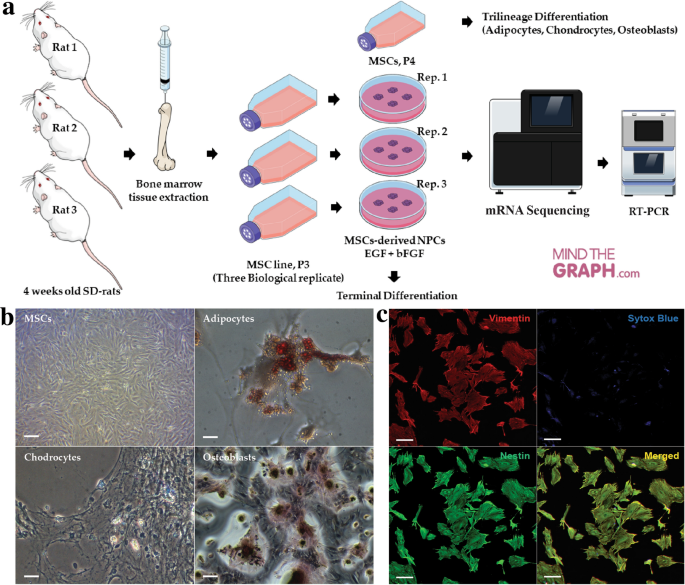
方法细节:从3只4周龄SD大鼠的股骨和胫骨中提取骨髓组织,通过Ficoll密度梯度离心分离单个核细胞,接种培养至第3代;将第4代MSCs分别诱导分化为脂肪细胞、软骨细胞、成骨细胞,采用油红O、阿利新蓝、茜素红S染色法鉴定分化结果;通过免疫细胞化学(ICC)检测巢蛋白(nestin)和波形蛋白(vimentin)的共表达情况,结合流式细胞术检测细胞表面标志物(CD90、CD44、纤连蛋白、vimentin、nestin、CD11b)的表达。
结果解读:染色结果显示MSCs可成功分化为脂肪、软骨、成骨细胞,证实其多向分化潜能(图1);免疫细胞化学结果显示nestin与vimentin在MSCs中共表达,流式细胞术数据显示MSCs阳性表达CD90(86.8%)、CD44(35.4%)、纤连蛋白(98.3%)、vimentin(90.9%)、nestin(85.6%),阴性表达巨噬细胞标志物CD11b(2.0%),符合典型MSCs的表型特征。
产品关联:实验所用关键产品:Ficoll-Paque PREMIUM梯度溶液(GE Healthcare Bioscience)、TrypLE™ Express稳定胰蛋白酶替代酶(Life Technologies)、StemPro®脂肪/软骨/成骨分化试剂盒(Gibco, Life Technologies)、Sytox® blue核酸染料(Life Technologies)、共聚焦显微镜配套Pascal 5成像软件等。
3.2 MSCs向NPCs的诱导与功能鉴定
实验目的:诱导MSCs分化为NPCs并验证其神经前体细胞特性,确定转录组分析的最佳取样时间点。
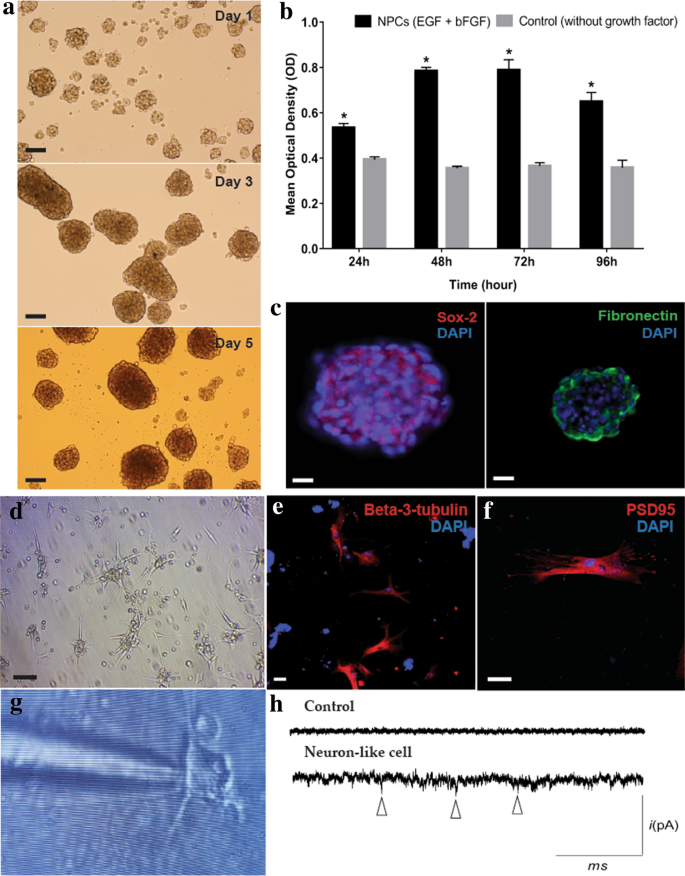
方法细节:将第3代MSCs接种于超低吸附板,使用添加20ng/ml bFGF、20ng/ml EGF的NeuroCult® NS-A增殖培养基诱导分化,每日观察细胞形态变化,每2天补充一次生长因子;通过MTS法检测诱导后1-4天的细胞活力,流式细胞术检测nestin和Sox2的表达水平,免疫细胞化学鉴定NPCs标志物;将诱导第3天的NPCs接种于聚-D-赖氨酸包被的培养皿,使用NeuroCult™ NS-A分化培养基诱导分化为神经元样细胞,通过免疫细胞化学检测成熟神经元标志物β-III微管蛋白和突触后标志物PSD-95,采用全细胞膜片钳技术检测神经元样细胞的电生理功能。
结果解读:诱导24小时后MSCs脱离培养表面形成悬浮神经球,第3天细胞活力达到峰值(n=3,P<0.05),第5天神经球中心出现凋亡核心(图2);流式细胞术显示nestin表达率从对照组的53.4%升至NPCs的94.0%,Sox2表达率从18.5%升至47.6%;神经元样细胞表达β-III微管蛋白和PSD-95,且可记录到微小兴奋性突触后电流(mEPSC),证实其具有功能性神经元的电生理特征,同时确定诱导第3天为转录组分析的最佳取样时间点。
产品关联:实验所用关键产品:NeuroCult® NS-A增殖培养基(STEMCELL Technologies)、bFGF(BioVision)、EGF(Gibco, Life Technologies)、Accutase®细胞分离溶液(Merck Millipore)、全细胞膜片钳配套pClamp程序等。
3.3 转录组测序与生物信息学分析
实验目的:系统解析MSCs与NPCs之间的转录组差异,鉴定分化过程中的关键调控基因、通路及转录因子。
方法细节:提取3例MSCs和3例诱导第3天NPCs的总RNA,采用miRNeasy mini试剂盒纯化RNA,使用TruSeq® Stranded mRNA样本制备试剂盒构建cDNA文库,通过NextSeq®500测序系统进行高通量测序;使用DESeq2 R包进行差异基因分析,筛选差异倍数≥2、校正P值≤0.05的基因;通过ClueGO插件进行基因本体(GO)富集分析,采用GSEA进行通路富集分析,结合TFcheckpoint数据库和ChEA3工具进行转录因子富集分析。
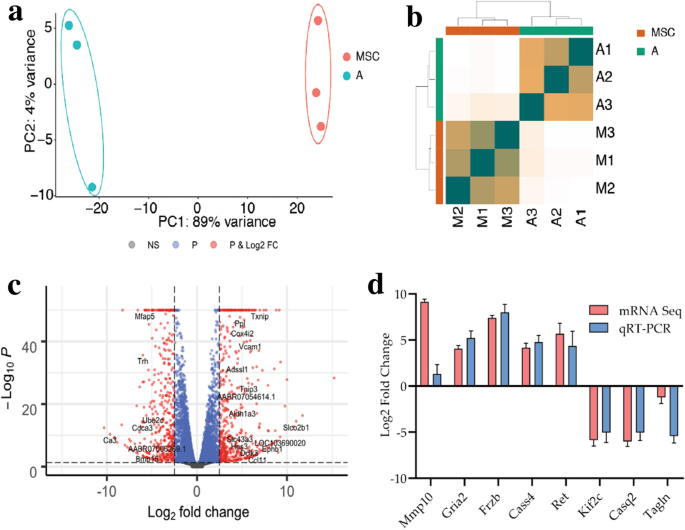
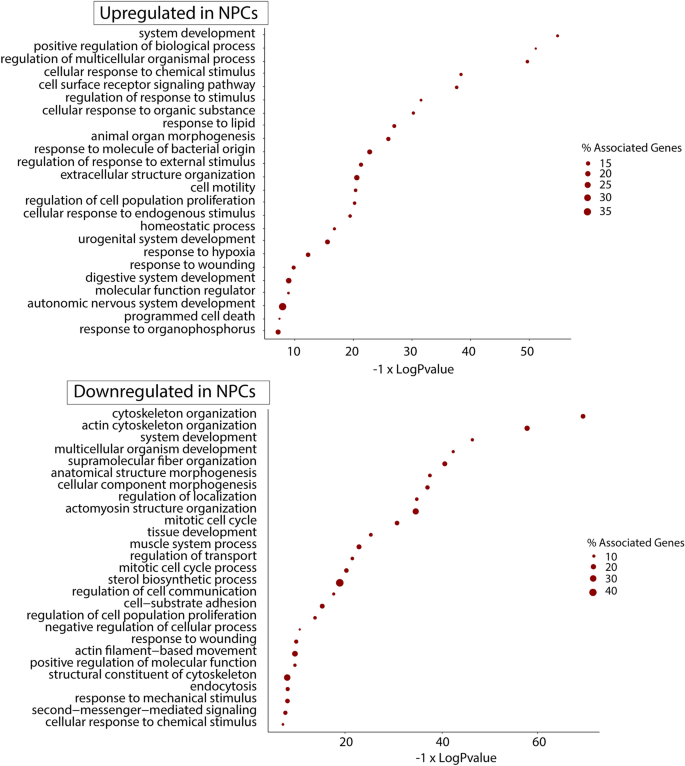
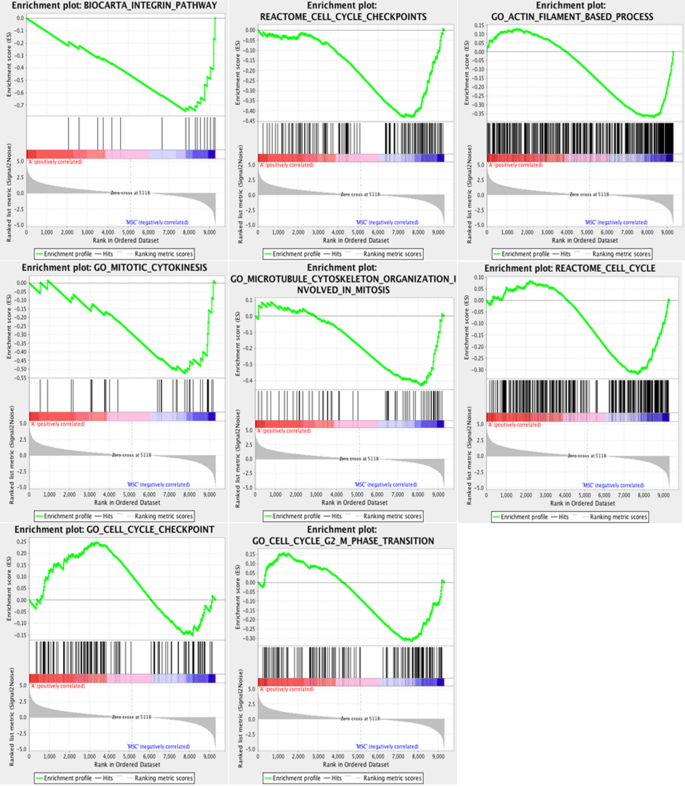
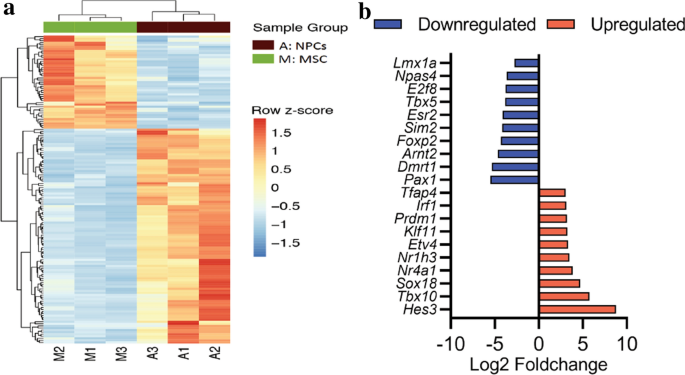
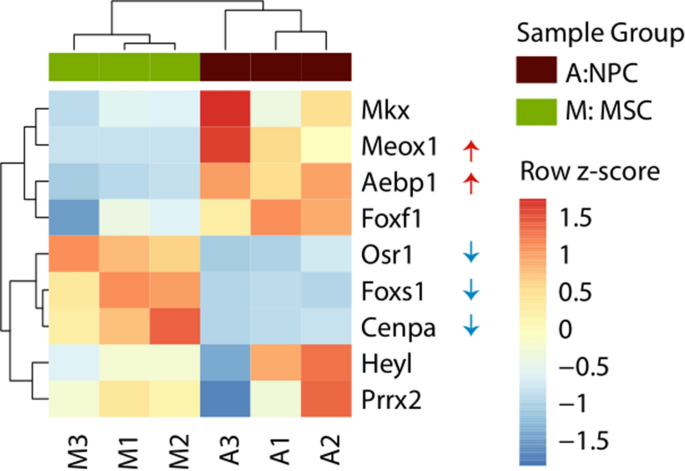
结果解读:测序质量控制显示96%的reads通过过滤标准,97%的reads比对到大鼠参考基因组(rn6);PCA和层次聚类分析显示MSCs与NPCs的转录组样本明显分离,组内重复性良好(图3);共鉴定出3252个差异表达基因,其中1771个在NPCs中上调,1481个下调;GO富集分析显示NPCs上调基因富集于自主神经系统、细胞表面受体信号通路、细胞外结构组织、程序性细胞死亡等与神经发生相关的通路,MSCs上调基因富集于细胞骨架组织、有丝分裂细胞周期等维持干细胞增殖的通路(图4);GSEA分析显示MSCs中整合素通路、细胞骨架组织、细胞周期相关通路显著富集(图5);转录因子分析显示104个转录因子在NPCs中上调,45个下调,其中Hes3、Tbx10等上调转录因子与神经发育直接相关,ChEA3分析显示Foxs1(下调)抑制MSCs向NPCs分化,HEYL(上调)促进分化(图6、7)。
产品关联:实验所用关键产品:miRNeasy mini试剂盒(Qiagen)、TruSeq® Stranded mRNA样本制备试剂盒(Illumina)、NextSeq®500测序系统(Illumina)、Cytoscape ClueGO插件、ChEA3数据库等。
3.4 差异表达基因的qPCR验证
实验目的:验证转录组测序结果的可靠性,确认关键差异基因的表达趋势。
方法细节:从差异表达基因中选取8个基因(5个上调基因:Mmp10、Gria2、Frzb、Cass4、Ret;3个下调基因:Kif2c、Tagln、Casq2),采用RT² Profiler PCR Arrays进行实时定量PCR(qPCR)验证;以B2m、Hprt1、Rplp1为内参基因,通过ddCt法计算基因的相对表达量,每个样本设置3个生物学重复和技术重复。
结果解读:qPCR结果显示,8个基因的表达变化趋势与转录组测序结果完全一致,其中Ret、Frzb等神经发生相关基因在NPCs中显著上调,Kif2c、Tagln等细胞周期相关基因在MSCs中显著上调(图3d),证实了转录组测序数据的可靠性。
产品关联:实验所用关键产品:RT² Profiler PCR Arrays(Exiqon)、QIAGEN RT² First Strand Kit(Qiagen)、qPCR配套RT² qPCR master mix等。
4. Biomarker研究及发现成果解析
核心信息段
本研究围绕MSCs向NPCs分化的早期阶段,鉴定出两类生物标志物:一类是用于鉴定分化阶段的细胞表面及转录水平标志物,另一类是调控分化过程的关键转录因子标志物;通过“转录组测序筛选→生物信息学富集分析→qPCR/流式细胞术验证”的完整逻辑链条,明确了标志物的表达特征与功能关联。
Biomarker定位:本研究鉴定的Biomarker包括转录水平差异表达基因和转录因子,其中细胞表型标志物为巢蛋白(nestin)、Sox2,转录水平标志物包括Ret、Frzb、Mmp10等上调基因,以及Kif2c、Tagln等下调基因,转录因子标志物包括Hes3、Tbx10、Foxs1、HEYL等;筛选与验证逻辑为:先通过转录组测序筛选差异表达基因,再通过GO富集、GSEA分析锁定与神经发生相关的基因,最后通过qPCR、流式细胞术验证标志物的表达特异性与敏感性。
研究过程详述:标志物来源为MSCs和诱导第3天NPCs的转录组及蛋白表达数据;验证方法包括qPCR验证基因转录水平、免疫细胞化学与流式细胞术验证蛋白表达水平;特异性与敏感性数据显示,nestin在NPCs中的表达率为94.0%(n=3,P<0.05),较MSCs的53.4%显著升高,Sox2表达率为47.6%(n=3,P<0.05),较MSCs的18.5%显著升高;差异基因Ret在NPCs中的表达倍数为(文献未明确提供具体倍数,基于图表趋势推测),Frzb的表达倍数为(文献未明确提供具体倍数,基于图表趋势推测),均具有显著统计学差异。
核心成果提炼:该Biomarker的功能关联包括:nestin和Sox2可作为NPCs分化阶段的鉴定标志物,Ret参与神经系统发育的信号通路,Frzb参与Wnt信号通路调控神经干细胞增殖,Hes3、Tbx10等转录因子直接调控神经发生过程;创新性在于首次系统解析了MSCs向NPCs分化早期的转录组差异,鉴定出149个差异表达转录因子,其中Foxs1抑制分化、HEYL促进分化的调控作用为该领域首次报道;统计学结果显示,3252个差异表达基因的校正P值≤0.05,差异倍数≥2(n=3),转录因子富集分析的结果具有显著统计学意义(ChEA3分析MeanRank评分靠前)。
