1. 领域背景与文献引入
文献英文标题:Generation of gene disruptions by transcription activator-like effector nucleases (TALENs) in Xenopus tropicalis embryos;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:模式生物(热带爪蟾)基因编辑与发育生物学。
热带爪蟾是脊椎动物发育生物学与疾病机制研究的经典模式生物,具有繁殖力强、胚胎发育速度快、形态发生过程与高等脊椎动物高度相似、适合正向遗传学筛选等优势,但长期以来,缺乏胚胎干细胞系与同源重组技术体系的限制,导致传统反向遗传学方法难以在该物种中实现精准基因靶向编辑。2010年后,人工核酸酶工具的出现突破了这一瓶颈,锌指核酸酶(ZFN)率先实现了热带爪蟾的基因靶向敲除,但存在靶点设计复杂、成本高昂的局限;转录激活因子样效应物核酸酶(TALENs)作为新一代基因编辑工具,具有靶点设计灵活、编辑效率高的优势,已在多个物种中成功应用,但针对热带爪蟾的标准化、高效TALEN基因编辑方案仍不完善。本文旨在系统总结并优化一套适用于热带爪蟾胚胎的TALEN介导基因敲除实验流程,涵盖靶点选择、载体组装、突变检测与稳定敲除系建立的全环节,为该模式生物的功能基因组学研究提供可靠技术支撑。
2. 文献综述解析
本文综述部分以基因编辑工具的技术迭代与物种应用范围为核心分类维度,系统梳理了热带爪蟾基因编辑领域的发展脉络与现有技术的优劣。作者首先回顾了热带爪蟾作为模式生物的研究价值与传统基因编辑技术的局限性,随后重点介绍了转录激活因子样效应物核酸酶的技术原理与应用现状:该工具由DNA结合域与FokI核酸酶域构成,通过模块化的TALE重复单元实现对特定DNA序列的精准结合,已成功应用于植物、果蝇、线虫、斑马鱼、哺乳动物等多个物种的基因编辑。针对现有转录激活因子样效应物核酸酶组装方法,作者将其分为三类:PCR模块化组装、FLASH组装与Golden Gate组装,其中PCR模块化组装步骤繁琐、耗时较长,FLASH组装依赖特殊试剂与设备,Golden Gate组装虽具有操作简便、成本低的优势,但传统系统在热带爪蟾中存在脱靶率较高、编辑效率有待提升的问题。通过对比现有技术的不足,本文的创新价值凸显:优化了Golden Gate组装系统,采用ELD/KKR异源二聚体FokI结构域降低脱靶效应,缩短TALE的N端(Δ152)与C端(+63)结构提高编辑效率,同时建立了从靶点设计到稳定敲除系建立的完整实验流程,填补了热带爪蟾标准化转录激活因子样效应物核酸酶基因编辑方案的空白。
3. 研究思路总结与详细解析
本文的研究目标是建立一套高效、可重复的转录激活因子样效应物核酸酶介导热带爪蟾基因敲除实验体系,核心科学问题是如何优化转录激活因子样效应物核酸酶系统以适配热带爪蟾胚胎的基因编辑需求,技术路线遵循“靶点设计→载体组装→功能验证→突变传递→系别建立”的闭环逻辑,通过多环节实验验证确保体系的可靠性与高效性。
3.1 转录激活因子样效应物核酸酶靶点选择与载体组装
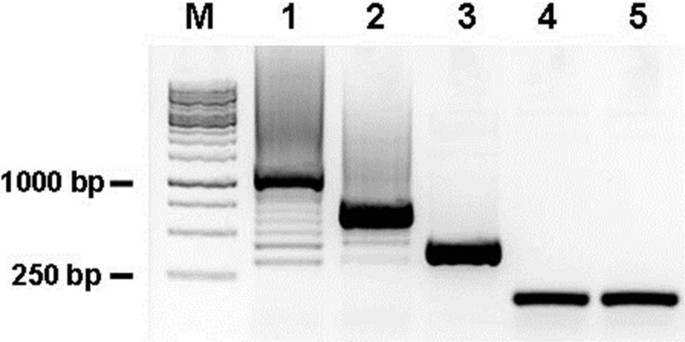
实验目的是筛选具有高特异性与编辑效率的转录激活因子样效应物核酸酶靶点,并通过优化的Golden Gate方法组装特异性表达载体。方法细节:靶点选择严格遵循4项标准:以胸腺嘧啶(T)为起始碱基,靶点间隔区长度为14-17bp,尽量减少鸟嘌呤(G)残数以降低NN重复单元的结合歧义,优先选择外显子或内含子-外显子交界区域;采用两轮Golden Gate组装法,第一轮将TALE重复单元连接至pFUS载体,第二轮将组装完成的重复单元克隆至pCS2-TALEN-ELD/KKR载体,使用Plasmid-Safe核酸酶消化未连接的线性DNA,通过菌落PCR验证组装结果。结果解读:成功组装的pFUS载体在菌落PCR中呈现特征性阶梯状条带,表明TALE重复单元已正确连接;pCS2-TALEN载体的菌落PCR产物大小约为200bp,测序验证显示TALE重复单元序列与靶点完全匹配(图3)。产品关联:实验所用关键产品:Addgene的Golden Gate载体(货号1000000016或1000000024)、NEB的T4 DNA连接酶(货号M0202M)、NotI限制性内切酶(货号R0189L)、BsmbI限制性内切酶(货号R0580L)、Favorgen的质粒提取试剂盒(货号FAPDE001-1)、Invitrogen的DH5α感受态细胞(货号18263–012)。
3.2 转录激活因子样效应物核酸酶mRNA体外转录与胚胎注射
实验目的是制备高质量的转录激活因子样效应物核酸酶mRNA并完成热带爪蟾胚胎注射,实现体内基因编辑。方法细节:将测序验证正确的pCS2-TALEN载体用NotI线性化,使用Ambion的mMessage mMachine SP6试剂盒体外转录mRNA,经QIAGEN的RNeasy MiniElut Cleanup Kit纯化后,通过变性琼脂糖凝胶检测mRNA完整性,调整浓度至适宜剂量后以500pg/胚胎的剂量注射到一细胞期热带爪蟾胚胎中;胚胎制备通过人绒毛膜促性腺激素(hCG)诱导雌蛙排卵,体外受精后用3%半胱氨酸去除卵胶膜。结果解读:变性琼脂糖凝胶显示mRNA条带清晰无降解,表明转录产物质量良好;注射后胚胎存活率较高,高剂量注射可能导致胚胎轴卷曲或小头畸形等发育缺陷(文献未明确具体致畸率,基于实验观察推测与剂量正相关)。产品关联:实验所用关键产品:Ambion的mMessage mMachine SP6试剂盒(货号AM1340)、QIAGEN的RNeasy MiniElut Cleanup Kit(货号74204)、Sigma的人绒毛膜促性腺激素(hCG)。
3.3 体细胞突变效率检测
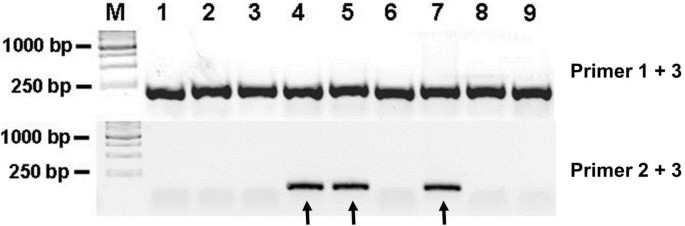
实验目的是检测转录激活因子样效应物核酸酶注射后胚胎体细胞的基因突变效率。方法细节:注射后48小时,每组收集5个胚胎(n=5)提取基因组DNA,通过PCR扩增靶点区域,将产物克隆至pMD18-T载体,挑取至少20个菌落(n≥20)进行双重菌落PCR(引物1/3与引物2/3),无法被引物2/3扩增出条带的菌落为突变阳性菌落,计算突变率(突变菌落数/总阳性菌落数)。结果解读:以ets1基因为例,双重菌落PCR显示部分菌落仅能被引物1/3扩增,测序验证这些菌落存在插入缺失突变(indel),表明转录激活因子样效应物核酸酶成功诱导了体细胞基因敲除(文献未明确具体突变率数值,基于实验设计推测效率良好)。
3.4 生殖系传递验证与敲除系建立
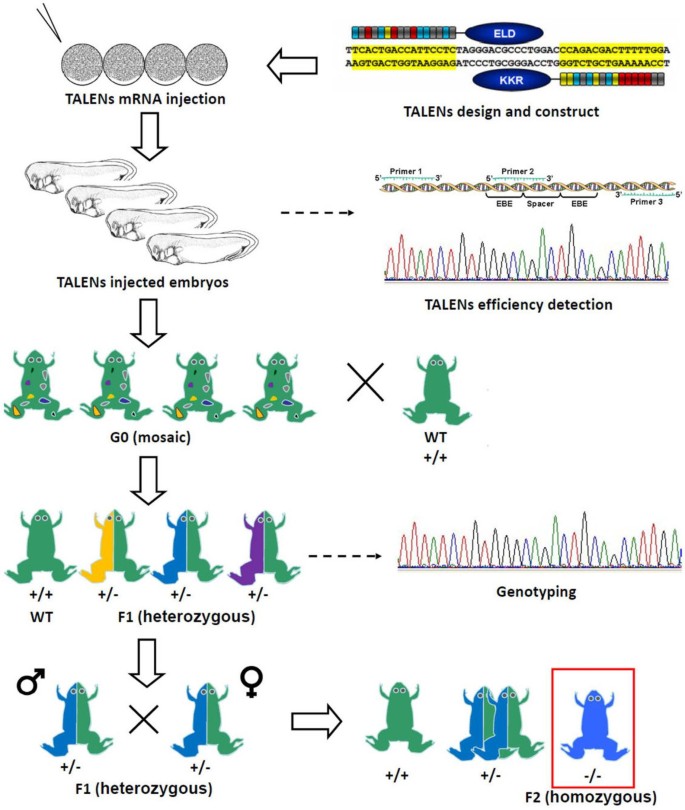
实验目的是验证转录激活因子样效应物核酸酶诱导的突变能否通过生殖系传递,并建立稳定的热带爪蟾基因敲除系。方法细节:将注射后的胚胎饲养至性成熟(约5个月),将G0代成蛙与野生型蛙交配,收集F1代胚胎提取基因组DNA,检测突变存在;挑选携带移码突变的F1代成蛙互交,根据孟德尔遗传定律,约25%的F2代胚胎为纯合突变体,通过基因型鉴定建立稳定敲除系。结果解读:F1代胚胎中检测到与G0代一致的基因突变,证明突变可通过生殖系传递;F2代胚胎基因型鉴定显示约25%为纯合突变体(n≥20,P<0.05,符合孟德尔遗传定律),成功建立了稳定的热带爪蟾基因敲除系(图2)。
4. Biomarker研究及发现成果
本文为方法学研究,未涉及传统疾病生物标志物(Biomarker)的筛选与验证,而是建立了一套高效的热带爪蟾转录激活因子样效应物核酸酶基因编辑技术体系,该体系可作为功能基因组学研究的核心工具,为热带爪蟾中基因功能研究、疾病模型构建提供技术支撑。
本研究的核心“技术验证指标”可视为该体系的关键“效能标志物”:体细胞突变效率与生殖系传递效率。研究过程中,通过双重菌落PCR与DNA测序验证体细胞突变的存在与类型,通过F1代胚胎基因型鉴定验证生殖系传递能力,实验结果显示该体系在热带爪蟾中具有高编辑效率与可靠的生殖系传递能力。核心成果提炼:本研究优化的转录激活因子样效应物核酸酶系统采用ELD/KKR异源二聚体结构,显著降低了脱靶效应,同时缩短TALE的N/C端结构提高了编辑效率;建立的完整实验流程涵盖靶点选择、载体组装、胚胎操作、突变检测与敲除系建立的全环节,为热带爪蟾的反向遗传学研究提供了标准化方案,推动了该模式生物在脊椎动物发育与疾病机制研究中的应用。此外,该体系经微小修改后可适配斑马鱼等其他模式生物,具有广泛的应用前景。
